课时2 硫酸及硫酸根离子的检验
一、刷基础
1.工业上制硫酸涉及如图三个装置。下列有关说法错误的是( )
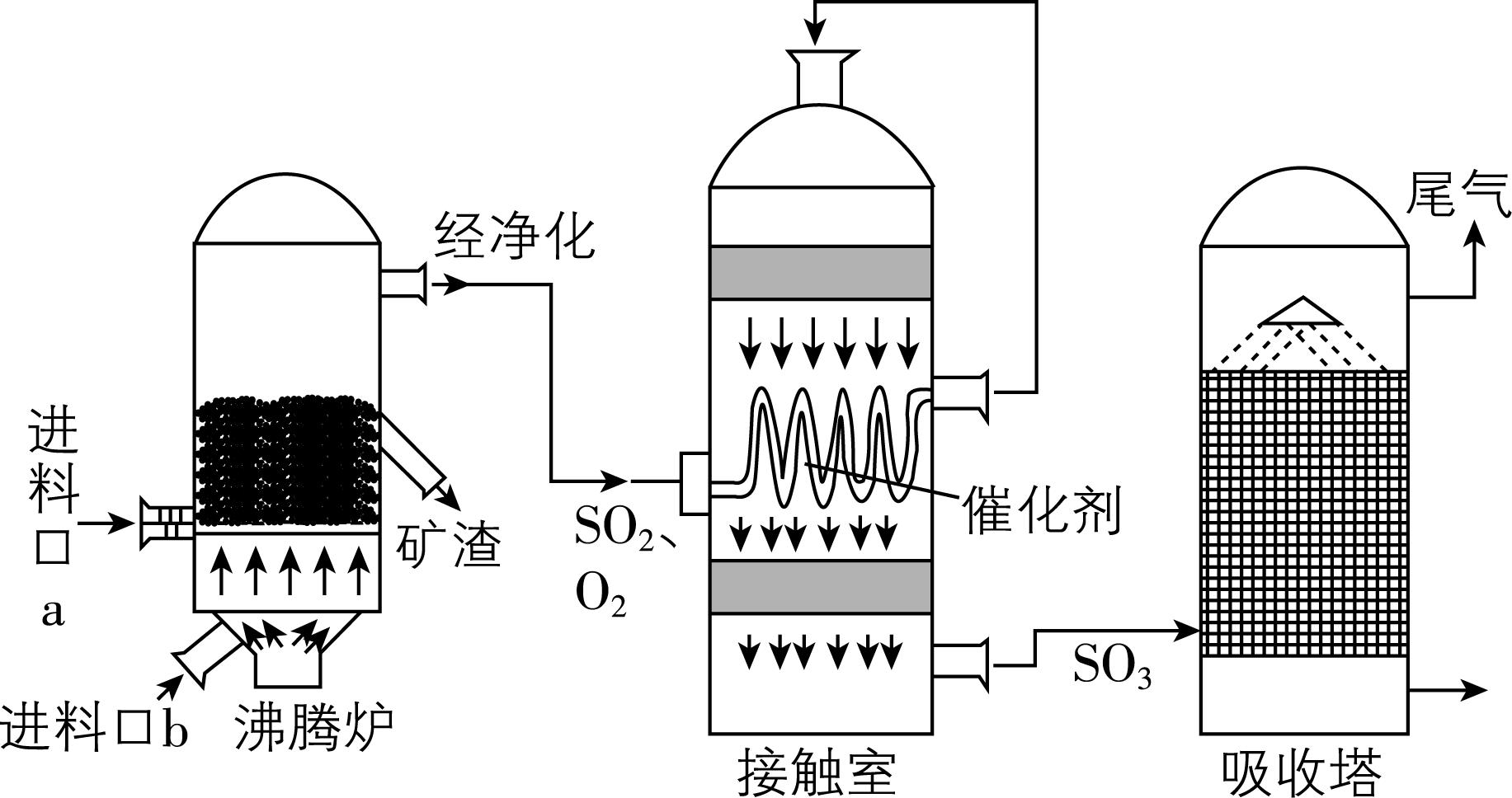
A. 硫在过量的空气中燃烧生成 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $
B. 接触室中的反应主要为 $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{△}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $
C. 吸收塔中不用水吸收 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ 的原因是 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ 溶于水时放出大量的热,从而形成酸雾,降低吸收效率
D. 在浓硫酸使蔗糖变黑面包的实验中,浓硫酸表现脱水性和氧化性
答案:A
解析:硫在过量的空气中燃烧生成 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,无法直接生成 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{A}} $ 错误;接触室内发生的反应为二氧化硫与氧气发生催化氧化反应生成三氧化硫,该反应为可逆反应,反应的化学方程式为 $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{△}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{B}} $ 正确;三氧化硫与水反应放出大量的热,若用蒸馏水吸收三氧化硫会形成酸雾,降低吸收效率, $ {\rm \mathrm{C}} $ 正确;浓硫酸使蔗糖变黑面包实验中,浓硫酸使蔗糖中的 $ {\rm \mathrm{H}} $ 、 $ {\rm \mathrm{O}} $ 原子以 $ 2:1 $ 的比例脱去,表现脱水性,同时有刺激性气味气体产生,为碳与浓硫酸发生氧化还原反应生成的二氧化硫气体,体现浓硫酸的氧化性, $ {\rm \mathrm{D}} $ 正确。
2.硫酸是重要的化工原料,工业制硫酸的原理示意图如下。
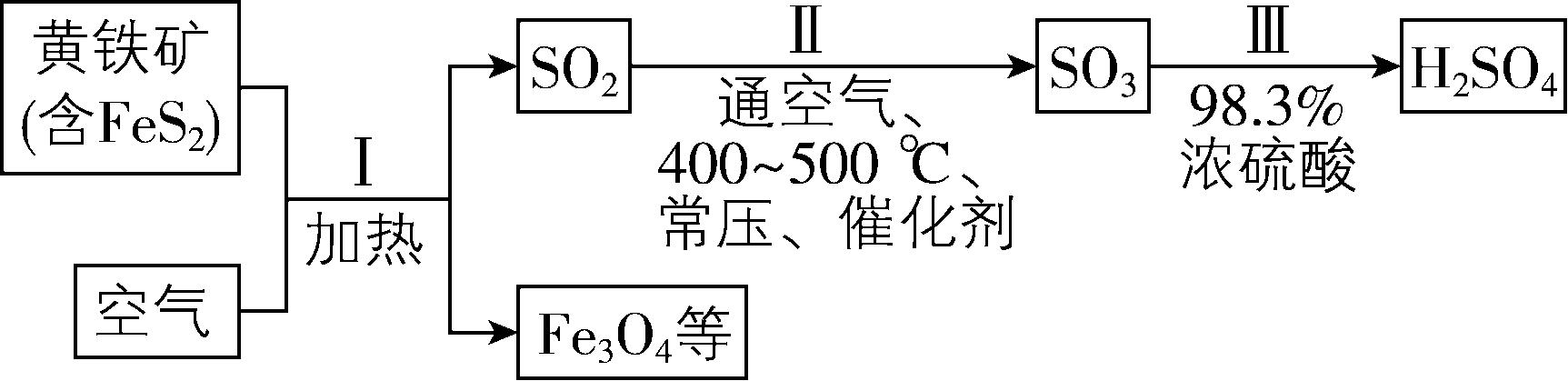
(1) $ {\rm {\mathrm{F}\mathrm{e}\mathrm{S}}_{2}} $ 中 $ {\rm \mathrm{F}\mathrm{e}} $ 为 $ +2 $ 价, $ {\rm \mathrm{S}} $ 的化合价为 。
(2) 将Ⅰ中反应的化学方程式补充完整: $ {\rm {\mathrm{F}\mathrm{e}\mathrm{S}}_{2}+} $ $ \xlongequal{△} $ $ {\rm {\mathrm{F}\mathrm{e}}_{3}{\mathrm{O}}_{4}+} $ $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $
若反应中消耗了 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{F}\mathrm{e}\mathrm{S}}_{2}} $ ,则生成 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的物质的量为 。
(3) Ⅱ中反应的化学方程式为 。
(4) 为避免制备硫酸时尾气中的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 污染环境,可使用尿素 $ {\rm [\mathrm{C}\mathrm{O} ({\mathrm{N}\mathrm{H}}_{2})_{2} ]/{\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液吸收尾气。
① 将尿素/ $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液吸收 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的化学方程式补充完整:
$ {\rm {\mathrm{S}\mathrm{O}}_{2}+\mathrm{C}\mathrm{O}({\mathrm{N}\mathrm{H}}_{2})_{2}+{\mathrm{H}}_{2}{\mathrm{O}}_{2}+} $ $ {\rm \xlongequal{}({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{S}\mathrm{O}}_{4}+} $
② 使用尿素/ $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液吸收 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,一般选择在 $ 50\sim 70℃ $ 下进行。过高的温度会导致相同时间内的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 去除率下降,原因是 。
答案:(1) $ -1 $
(2) 3;8; $ {\rm {\mathrm{O}}_{2}} $ ;0;6; $ 2\mathrm{m}\mathrm{o}\mathrm{l} $
(3) $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{400\sim 500{℃}}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $
(4) ① $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ ; $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $
② 温度过高, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 在溶液中的溶解度降低且 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 分解速率大,浓度显著降低
解析:(1) 化学式中各元素化合价的代数和等于 $ {\rm 0, {\mathrm{F}\mathrm{e}\mathrm{S}}_{2}} $ 中 $ {\rm \mathrm{F}\mathrm{e}} $ 为 $ +2 $ 价,故 $ {\rm \mathrm{S}} $ 的化合价为 $ -1 $ 。
(2) 由题图结合元素守恒分析,Ⅰ中反应的另一反应物为 $ {\rm {\mathrm{O}}_{2}} $ ,反应过程中 $ {\rm \mathrm{F}\mathrm{e}} $ 、 $ {\rm \mathrm{S}} $ 化合价升高, $ {\rm \mathrm{O}} $ 化合价降低,根据氧化还原反应配平可得,Ⅰ中反应的化学方程式为 $ {\rm 3{\mathrm{F}\mathrm{e}\mathrm{S}}_{2}+8{\mathrm{O}}_{2}\xlongequal{△}{\mathrm{F}\mathrm{e}}_{3}{\mathrm{O}}_{4}+6{\mathrm{S}\mathrm{O}}_{2}} $ ;由上述反应的化学方程式可知,若反应中消耗了 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{F}\mathrm{e}\mathrm{S}}_{2}} $ ,则生成 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的物质的量为 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 。
(3) 由题图可知,Ⅱ中反应是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 被催化氧化为 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ ,化学方程式为 $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{400\sim 500{℃}}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $ 。
(4) ① 反应中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的 $ {\rm \mathrm{S}} $ 由 $ +4 $ 价升高到 $ +6 $ 价, $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 中 $ {\rm \mathrm{O}} $ 由 $ -1 $ 价降低到 $ -2 $ 价,尿素中各元素化合价均未改变,其中 $ {\rm \mathrm{N}} $ 元素转化为铵根离子, $ {\rm \mathrm{C}} $ 转化为 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 气体,则用尿素/ $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液吸收 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的化学方程式为 $ {\rm {\mathrm{S}\mathrm{O}}_{2}+\mathrm{C}\mathrm{O}({\mathrm{N}\mathrm{H}}_{2})_{2}+{\mathrm{H}}_{2}{\mathrm{O}}_{2}+{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{S}\mathrm{O}}_{4}+{\mathrm{C}\mathrm{O}}_{2}} $ 。
② $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 受热易分解,故使用尿素/ $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液吸收 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 时,温度过高, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 在溶液中的溶解度降低且 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 分解速率大,浓度显著降低,从而导致相同时间内的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 去除率下降。
3.在如图所示的实验装置中,实验开始一段时间后,对实验现象及结论的叙述均不正确的是( )
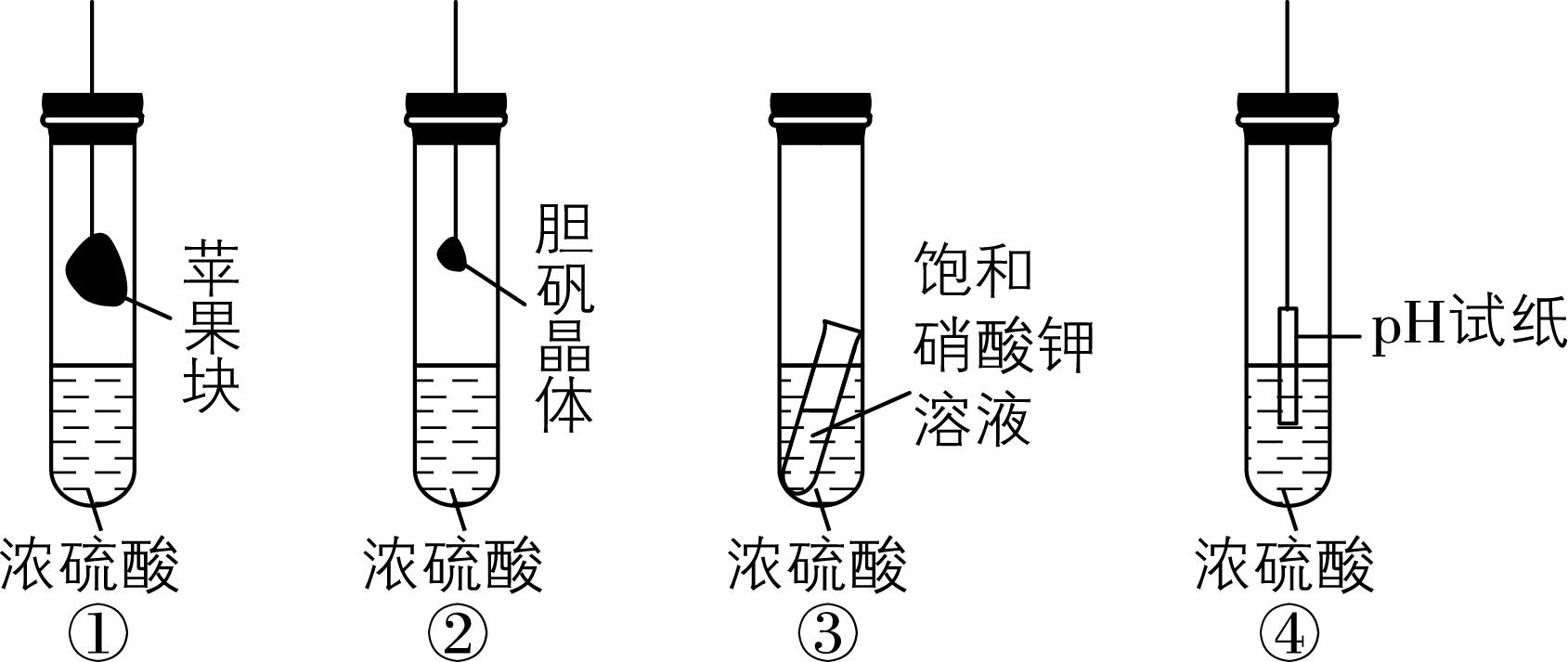
选项 | 装置 | 现象 | 结论 |
A | ① | 苹果块会干瘪 | 浓硫酸具有强氧化性 |
B | ② | 胆矾晶体表面有“白斑” | 浓硫酸具有脱水性 |
C | ③ | 小试管内无明显现象 | 浓硫酸具有吸水性 |
D | ④ | $ {\rm \mathrm{p}\mathrm{H}} $ 试纸会变红 | 浓硫酸具有酸性 |
解析:①中苹果块会干瘪,体现了浓硫酸的吸水性, $ {\rm \mathrm{A}} $ 不符合题意;②中胆矾晶体失去结晶水后变白,体现了浓硫酸的吸水性, $ {\rm \mathrm{B}} $ 不符合题意;③中小试管内有固体析出,体现了浓硫酸的吸水性, $ {\rm \mathrm{C}} $ 不符合题意;④中 $ {\rm \mathrm{p}\mathrm{H}} $ 试纸脱水炭化而变黑,体现了浓硫酸的脱水性, $ {\rm \mathrm{D}} $ 符合题意。
4.下列对浓硫酸的叙述正确的是( )
A. 常温下,浓硫酸与铁、铝不反应,所以铁制、铝制容器能盛放浓硫酸
B. 浓硫酸具有强氧化性, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 、 $ {\rm \mathrm{C}\mathrm{O}} $ 具有还原性,故浓硫酸不能干燥 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 、 $ {\rm \mathrm{C}\mathrm{O}} $
C. 浓硫酸和铜片加热反应中铜是还原剂
D. 浓硫酸与亚硫酸钠反应制取 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 时,浓硫酸表现出强氧化性
答案:C
解析:常温下, $ {\rm \mathrm{F}\mathrm{e}} $ 、 $ {\rm \mathrm{A}\mathrm{l}} $ 遇浓硫酸发生钝化,钝化过程中发生了化学反应, $ {\rm \mathrm{A}} $ 错误;浓硫酸与 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 、 $ {\rm \mathrm{C}\mathrm{O}} $ 不反应,可以干燥 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 、 $ {\rm \mathrm{C}\mathrm{O}} $ , $ {\rm \mathrm{B}} $ 错误;铜与浓硫酸在加热条件下发生反应,部分 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 被还原,生成 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,作氧化剂,铜作还原剂, $ {\rm \mathrm{C}} $ 正确;实验室中用浓硫酸与亚硫酸钠反应制取二氧化硫,其原理是用强酸制弱酸,因而在此反应中浓硫酸表现的是酸性, $ {\rm \mathrm{D}} $ 错误。
5.蔗糖与浓硫酸发生反应的过程如图所示。
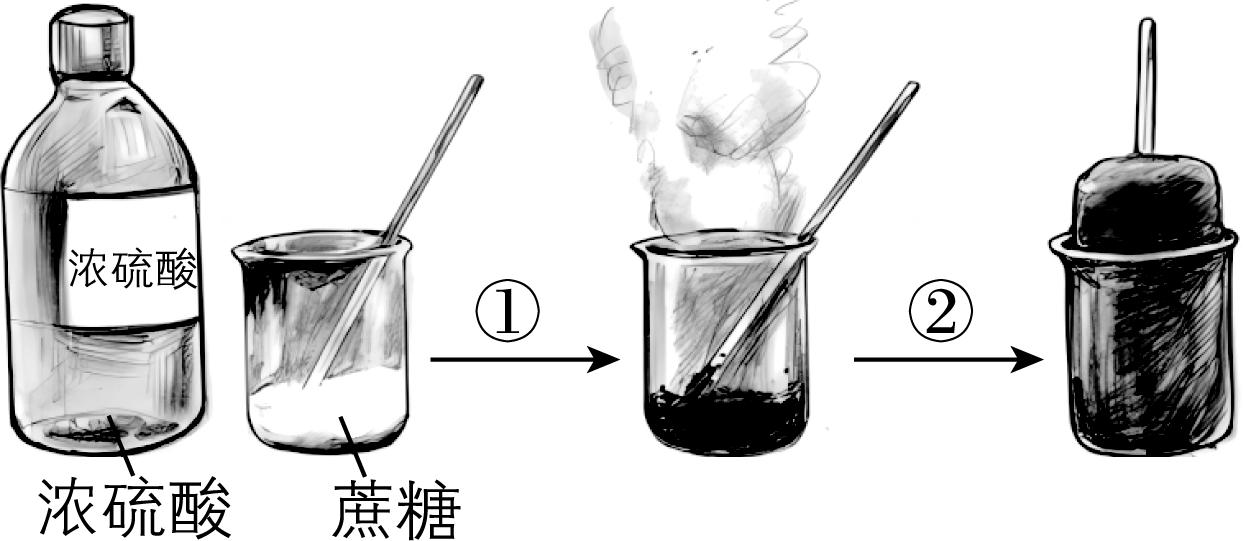
下列关于该过程的分析不正确的是( )
A. 过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
B. 过程①白色固体变黑,主要体现了浓硫酸的脱水性
C. 过程②固体体积膨胀,与产生的大量气体有关
D. 过程中蔗糖分子发生了化学键的断裂
答案:A
解析:浓硫酸与蔗糖脱水形成的炭黑反应生成的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 能使品红溶液褪色,体现浓硫酸的强氧化性, $ {\rm \mathrm{A}} $ 符合题意;浓硫酸具有脱水性,能将蔗糖中的 $ {\rm \mathrm{H}} $ 原子和 $ {\rm \mathrm{O}} $ 原子按 $ 2:1 $ 的比例脱除,蔗糖中加入浓硫酸,白色固体变黑,体现浓硫酸的脱水性, $ {\rm \mathrm{B}} $ 不符合题意;浓硫酸脱水过程中会释放大量热,发生反应: $ {\rm \mathrm{C}+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}(浓)\xlongequal{△}{\mathrm{C}\mathrm{O}}_{2}↑+2{\mathrm{S}\mathrm{O}}_{2}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ ,产生大量气体,使固体体积膨胀, $ {\rm \mathrm{C}} $ 不符合题意;该过程中,蔗糖发生化学反应,发生了化学键的断裂, $ {\rm \mathrm{D}} $ 不符合题意。
6.某学习小组设计如图所示的装置对浓硫酸与木炭的反应进行实验探究(部分夹持装置略)。下列说法不正确的是( )
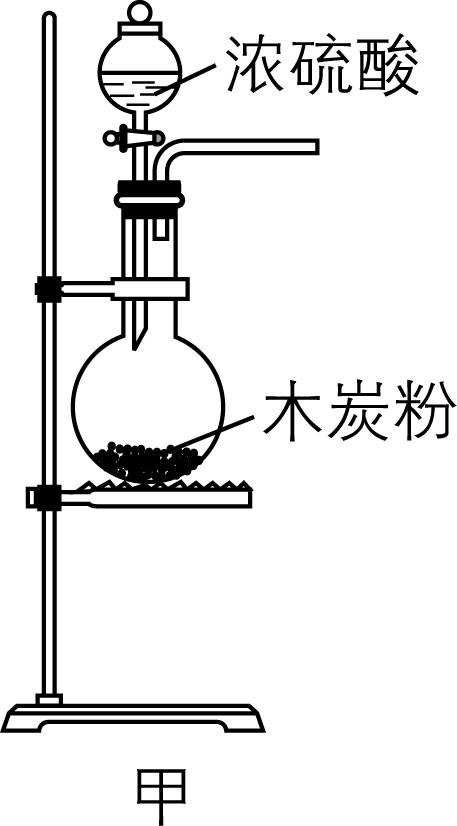
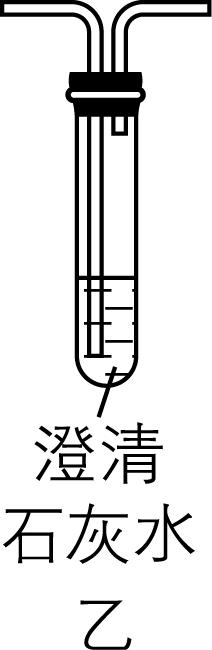
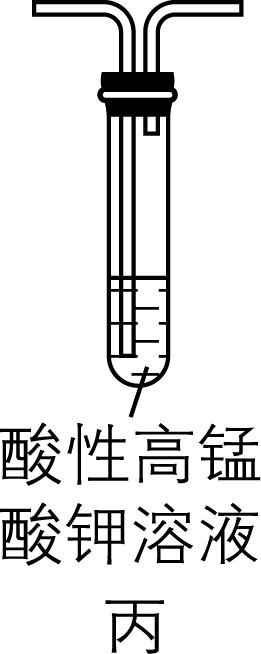
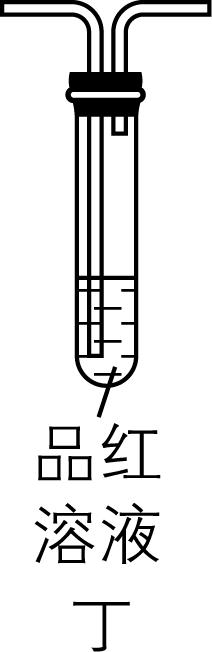
A. 甲装置中还缺少加热仪器
B. 用丙或丁装置均可探究 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的漂白性
C. 按甲 $ \to $ 丁 $ \to $ 丙顺序连接装置,可证明浓硫酸的还原产物是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $
D. 按甲 $ \to $ 丁 $ \to $ 丙 $ \to $ 乙顺序连接装置(丙中溶液未变为无色),可证明木炭的氧化产物是 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $
答案:B
解析:浓硫酸与木炭的反应需要在加热条件下进行,故甲装置中还缺少加热仪器, $ {\rm \mathrm{A}} $ 正确;用丙装置探究 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的还原性,用丁装置探究 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的漂白性, $ {\rm \mathrm{B}} $ 错误;按甲 $ \to $ 丁 $ \to $ 丙顺序连接装置,若丁装置中的品红溶液褪色,证明反应有 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 生成,丙装置可进一步检验并吸收 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ , $ {\rm \mathrm{C}} $ 正确;按甲 $ \to $ 丁(检验二氧化硫) $ \to $ 丙(除去二氧化硫,溶液颜色变浅) $ \to $ 乙(澄清石灰水变浑浊)顺序连接装置,可证明木炭的氧化产物是 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ , $ {\rm \mathrm{D}} $ 正确。
7.下列区分浓硫酸和稀硫酸的方法中既绿色环保又简单可行的是( )
A. 取样,分别放入质量相同的铜片
B. 取样,分别滴入紫色石蕊溶液中,观察颜色
C. 用玻璃棒各蘸取少许涂在纸上
D. 加入锌粒,观察是否有气体生成
答案:C
解析:常温下,浓硫酸、稀硫酸和 $ {\rm \mathrm{C}\mathrm{u}} $ 都不反应, $ {\rm \mathrm{A}} $ 错误;少量的浓硫酸、稀硫酸滴入紫色石蕊溶液中都能使紫色石蕊溶液变红, $ {\rm \mathrm{B}} $ 错误;浓硫酸具有脱水性,浓硫酸能使纸炭化变黑, $ {\rm \mathrm{C}} $ 正确;浓硫酸与 $ {\rm \mathrm{Z}\mathrm{n}} $ 反应生成有毒的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 气体,不符合绿色环保的要求, $ {\rm \mathrm{D}} $ 错误。
8.取少量试样,进行下列实验,能判断溶液中一定含有 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 的操作是( )
A. 滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀
B. 滴加盐酸酸化的 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀
C. 滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀,加稀盐酸沉淀不溶解
D. 加入稀盐酸酸化,无明显现象,加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,有白色沉淀生成
答案:D
解析:滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀,该沉淀可能是 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ ,也可能是 $ {\rm \mathrm{A}\mathrm{g}\mathrm{C}\mathrm{l}} $ 、 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}} $ 等,所以不能确定溶液中一定含有 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ , $ {\rm \mathrm{A}} $ 错误;滴加盐酸酸化的 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀,同样不能排除 $ {\rm {\mathrm{A}\mathrm{g}}^{+}} $ 的干扰,因为 $ {\rm {\mathrm{A}\mathrm{g}}^{+}} $ 与 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 在酸性条件下也会生成 $ {\rm \mathrm{A}\mathrm{g}\mathrm{C}\mathrm{l}} $ 白色沉淀, $ {\rm \mathrm{B}} $ 错误;滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀,加稀盐酸沉淀不溶解,还是不能排除 $ {\rm \mathrm{A}\mathrm{g}\mathrm{C}\mathrm{l}} $ 沉淀的可能 $ {\rm (\mathrm{A}\mathrm{g}\mathrm{C}\mathrm{l}} $ 沉淀不溶于酸 $ ) $ , $ {\rm \mathrm{C}} $ 错误;加入盐酸酸化,无明显现象,排除了 $ {\rm {\mathrm{C}\mathrm{O}}_{3}^{2-}({\mathrm{C}\mathrm{O}}_{3}^{2-}} $ 与 $ {\rm {\mathrm{H}}^{+}} $ 反应会产生二氧化碳气体 $ ) $ 、 $ {\rm {\mathrm{S}\mathrm{O}}_{3}^{2-}({\mathrm{S}\mathrm{O}}_{3}^{2-}} $ 与 $ {\rm {\mathrm{H}}^{+}} $ 反应会产生二氧化硫气体 $ ) $ 和 $ {\rm {\mathrm{A}\mathrm{g}}^{+}({\mathrm{A}\mathrm{g}}^{+}} $ 与 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 反应会生成沉淀 $ ) $ 等的干扰,再加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,有白色沉淀生成,此沉淀只能是 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ ,所以能判断溶液中一定含有 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ , $ {\rm \mathrm{D}} $ 正确。
9.某工业废水中存在大量的 $ {\rm {\mathrm{N}\mathrm{a}}^{+}} $ 、 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 、 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ 、 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,欲除去其中的 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ 、 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,设计工艺流程如下所示:
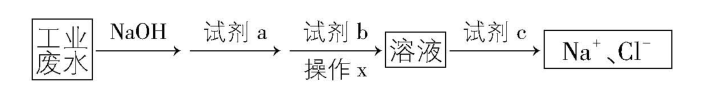
下列有关说法错误的是( )
A. $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 的作用是除去 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $
B. 试剂 $ \mathrm{a} $ 为 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ ,试剂 $ \mathrm{b} $ 为 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $
C. 操作 $ \mathrm{x} $ 为过滤,试剂 $ \mathrm{c} $ 为稀盐酸
D. 检验 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 是否除尽,可取适量待测溶液,先加入盐酸,再加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液
答案:B
解析:废水中只有 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ 可以和 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 反应, $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 的作用是除去 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ , $ {\rm \mathrm{A}} $ 正确;试剂 $ \mathrm{a} $ 为 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ ,试剂 $ \mathrm{b} $ 为 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ ,碳酸钠用于除去过量钡离子, $ {\rm \mathrm{B}} $ 错误;题给流程图中操作 $ \mathrm{x} $ 为过滤,滤液中含 $ {\rm {\mathrm{N}\mathrm{a}}^{+}} $ 、 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 、 $ {\rm {\mathrm{C}\mathrm{O}}_{3}^{2-}} $ 、 $ {\rm {\mathrm{O}\mathrm{H}}^{-}} $ ,试剂 $ \mathrm{c} $ 为稀盐酸,可除去 $ {\rm {\mathrm{C}\mathrm{O}}_{3}^{2-}} $ 、 $ {\rm {\mathrm{O}\mathrm{H}}^{-}} $ , $ {\rm \mathrm{C}} $ 正确;检验 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 是否除尽,可取适量待测溶液,先加入盐酸,再加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,如果没有白色沉淀生成,说明已经除尽, $ {\rm \mathrm{D}} $ 正确。
10.下列关于硫酸盐说法错误的是( )
A. 美术教室里的各种塑像,主要是用硫酸钙制作完成的
B. 进行消化系统 $ {\rm \mathrm{X}} $ 射线检查前,服用的“钡餐”中含有硫酸钡
C. 检验无水酒精中是否真的没有水,常用胆矾晶体
D. 船员打上来的黄河水比较浑浊,常加明矾使杂质沉降
答案:C
解析:硫酸钙(熟石膏)常用于制作塑像,因其与水混合后很快凝固成型, $ {\rm \mathrm{A}} $ 正确。硫酸钡不溶于水和酸,且不容易被 $ {\rm \mathrm{X}} $ 射线透过,在医疗上可用作检查消化系统的内服药剂,俗称“钡餐”, $ {\rm \mathrm{B}} $ 正确。检验水分常用无水硫酸铜(白色粉末),无水 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ 遇水转化为蓝色的胆矾 $ {\rm ({\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}\cdot 5{\mathrm{H}}_{2}\mathrm{O})} $ ,胆矾本身无法检验水, $ {\rm \mathrm{C}} $ 错误。明矾 $ {\rm [\mathrm{K}\mathrm{A}\mathrm{l} ({\mathrm{S}\mathrm{O}}_{4})_{2}\cdot 12{\mathrm{H}}_{2}\mathrm{O} ]} $ 溶于水后会生成 $ {\rm \mathrm{A}\mathrm{l}(\mathrm{O}\mathrm{H})_{3}} $ 胶体,可以吸附水中的悬浮物和杂质使其聚集而沉降,达到净水目的, $ {\rm \mathrm{D}} $ 正确。
11.将铜丝插入热的浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )
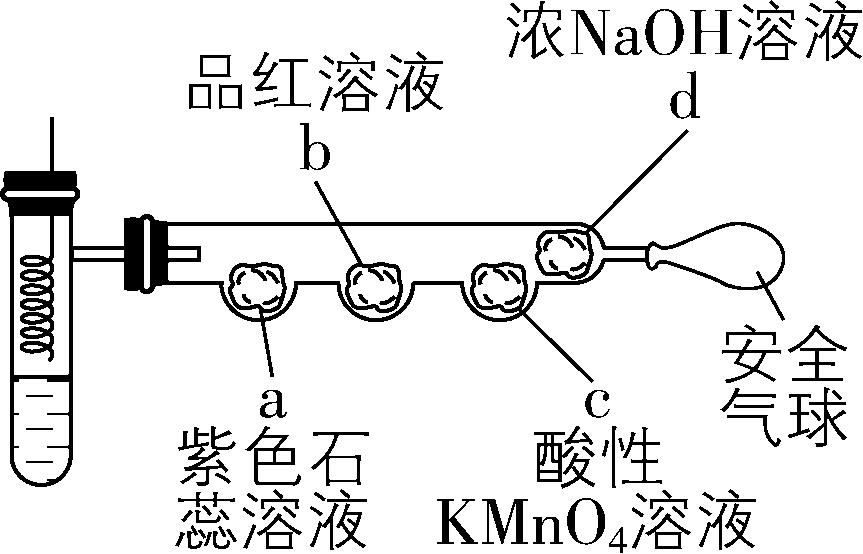
A. $ {\rm \mathrm{C}\mathrm{u}} $ 与浓硫酸反应,体现浓 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 的酸性和强氧化性
B. $ \mathrm{a} $ 处变红,说明 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 具有挥发性
C. $ \mathrm{b} $ 或 $ \mathrm{c} $ 处褪色,均说明 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 具有漂白性
D. 试管底部出现白色固体,说明浓硫酸具有脱水性
答案:A
解析:铜和浓硫酸反应过程中,生成 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ 体现浓硫酸的酸性,生成 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 体现浓硫酸的强氧化性, $ {\rm \mathrm{A}} $ 正确; $ \mathrm{a} $ 处的紫色石蕊溶液变红,其原因是反应生成的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 溶于水生成了 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 溶液显酸性,使紫色石蕊变红,硫酸是难挥发性酸, $ {\rm \mathrm{B}} $ 错误; $ \mathrm{b} $ 处品红溶液褪色,其原因是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 具有漂白性,而 $ \mathrm{c} $ 处酸性高锰酸钾溶液褪色,其原因是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 发生氧化还原反应, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 体现还原性, $ {\rm \mathrm{C}} $ 错误;实验过程中试管底部出现白色固体,其成分为无水 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ ,体现浓硫酸的吸水性, $ {\rm \mathrm{D}} $ 错误。
二、刷提升
1.如图是某硫酸试剂瓶标签上的部分内容。下列说法中正确的是( )
硫酸 化学纯 $ {\rm (\mathrm{C}\mathrm{P})} $ $ {\rm (500\mathrm{m}\mathrm{L})} $ 品名:硫酸 化学式: $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 相对分子质量:98 密度: $ 1.84\mathrm{g}\cdot {\mathrm{c}\mathrm{m}}^{-3} $ 质量分数: $ 98\% $ |
A. 该硫酸可以用来干燥硫化氢气体
B. $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{Z}\mathrm{n}} $ 与该硫酸完全反应能产生 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 气体
C. 若不小心将该硫酸溅到皮肤上,应立即用 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液冲洗
D. 实验室需要 $ {\rm 180\mathrm{m}\mathrm{L}4.6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 的稀硫酸,配制时应量取该硫酸 $ {\rm 45.0\mathrm{m}\mathrm{L}} $
答案:B
解析:该硫酸是质量分数为 $ 98\% $ 的浓硫酸,具有强氧化性,而硫化氢具有还原性,两者会反应,故该硫酸不可以用来干燥硫化氢气体, $ {\rm \mathrm{A}} $ 错误;在该反应中,硫酸过量, $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{Z}\mathrm{n}} $ 与该硫酸完全反应,转移 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 电子,不论生成二氧化硫还是氢气,生成气体的总物质的量都是 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ , $ {\rm \mathrm{B}} $ 正确;若不小心将该硫酸溅到皮肤上,应立即用大量水冲洗,然后用 $ 3\%\sim 5\% $ 的 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶液冲洗, $ {\rm \mathrm{C}} $ 错误;该硫酸的物质的量浓度 $ {\rm c=\dfrac{1.84×1000×98{\%}}{98}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}=18.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,实验室需要 $ {\rm 180\mathrm{m}\mathrm{L}4.6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 的稀硫酸,实际要配制 $ {\rm 250\mathrm{m}\mathrm{L}} $ ,则需量取该硫酸的体积 $ {\rm V=\dfrac{250\mathrm{m}\mathrm{L}×4.6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}}{18.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}}=62.5\mathrm{m}\mathrm{L}} $ , $ {\rm \mathrm{D}} $ 错误。
2.把一定量的锌与 $ {\rm 100\mathrm{m}\mathrm{L}18.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 浓硫酸充分反应后,锌完全溶解,同时生成气体 $ {\rm \mathrm{Y}33.6\mathrm{L}} $ (在标准状况下)。将反应后的溶液稀释到 $ {\rm 1\mathrm{L}} $ ,测得溶液中 $ {\rm c({\mathrm{H}}^{+})=0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 。下列叙述不正确的是( )
A. 气体 $ {\rm \mathrm{Y}} $ 是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}} $ 的混合物
B. 反应中共消耗锌 $ 78\mathrm{g} $
C. 气体 $ {\rm \mathrm{Y}} $ 中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}} $ 的体积之比为 $ 1:4 $
D. 反应中共转移 $ 3\mathrm{m}\mathrm{o}\mathrm{l} $ 电子
答案:B
解析:浓硫酸与锌反应生成二氧化硫气体,随着反应的进行,硫酸的浓度逐渐降低,继续与锌反应生成氢气,气体 $ {\rm \mathrm{Y}} $ 的物质的量为 $ {\rm \dfrac{33.6\mathrm{L}}{22.4\mathrm{L}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}=1.5\mathrm{m}\mathrm{o}\mathrm{l}} $ ,溶液稀释至 $ {\rm 1\mathrm{L}} $ ,测得溶液中 $ {\rm c({\mathrm{H}}^{+})=0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,所以剩余 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 的物质的量 $ {\rm n({\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4})=\dfrac{1}{2}n({\mathrm{H}}^{+})=0.05\mathrm{m}\mathrm{o}\mathrm{l}} $ ,参加反应的 $ {\rm n({\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4})=0.1\mathrm{L}×18.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}-0.05\mathrm{m}\mathrm{o}\mathrm{l}=1.8\mathrm{m}\mathrm{o}\mathrm{l}} $ ,设反应生成 $ {\rm x\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm y\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}} $ ,则
$ {\rm\hspace{-0.5em} \begin{array} {l} \rm\hspace{-0.5em} \begin{array}{ccccccccc}\mathrm{Z}\mathrm{n}& +& 2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}\left(浓\right)& \xlongequal{}& {\mathrm{Z}\mathrm{n}\mathrm{S}\mathrm{O}}_{4}& +& {\mathrm{S}\mathrm{O}}_{2}↑& +& 2{\mathrm{H}}_{2}\mathrm{O}\\ x& & 2x& & & & x& & \end{array} \hspace{-0.5em}\end{array} \hspace{-0.5em} } $
$ {\rm\hspace{-0.5em} \begin{array} {l} \rm\hspace{-0.5em} \begin{array}{ccccccc}\mathrm{Z}\mathrm{n}& +& {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}& \xlongequal{}& {\mathrm{Z}\mathrm{n}\mathrm{S}\mathrm{O}}_{4}& +& {\mathrm{H}}_{2}↑\\ y& & y& & & & y\end{array} \hspace{-0.5em}\end{array} \hspace{-0.5em} } $
则有 $ x+y=1.5 $ , $ 2x+y=1.8 $ ,解得 $ x=0.3 $ , $ y=1.2 $ ,所以反应生成 $ {\rm 0.3\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm 1.2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}} $ 。气体 $ {\rm \mathrm{Y}} $ 是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}} $ 的混合物, $ {\rm \mathrm{A}} $ 正确;反应中共消耗锌的物质的量为 $ (x+y)\mathrm{m}\mathrm{o}\mathrm{l}=1.5\mathrm{m}\mathrm{o}\mathrm{l} $ ,质量为 $ 1.5\mathrm{m}\mathrm{o}\mathrm{l}×65\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}=97.5\mathrm{g} $ , $ {\rm \mathrm{B}} $ 错误;同温同压下,气体体积之比等于物质的量之比,气体 $ {\rm \mathrm{Y}} $ 中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}} $ 的体积比为 $ 0.3:1.2=1:4 $ , $ {\rm \mathrm{C}} $ 正确; $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{Z}\mathrm{n}} $ 反应转移 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 电子,转移电子共 $ 1.5\mathrm{m}\mathrm{o}\mathrm{l}×2=3\mathrm{m}\mathrm{o}\mathrm{l} $ , $ {\rm \mathrm{D}} $ 正确。
3.硫酸是工、农业生产的重要化工原料。某工厂以黄铁矿(主要成分为 $ {\rm {\mathrm{F}\mathrm{e}\mathrm{S}}_{2}} $ )为原料,采用接触氧化法生产 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 的流程如图所示。
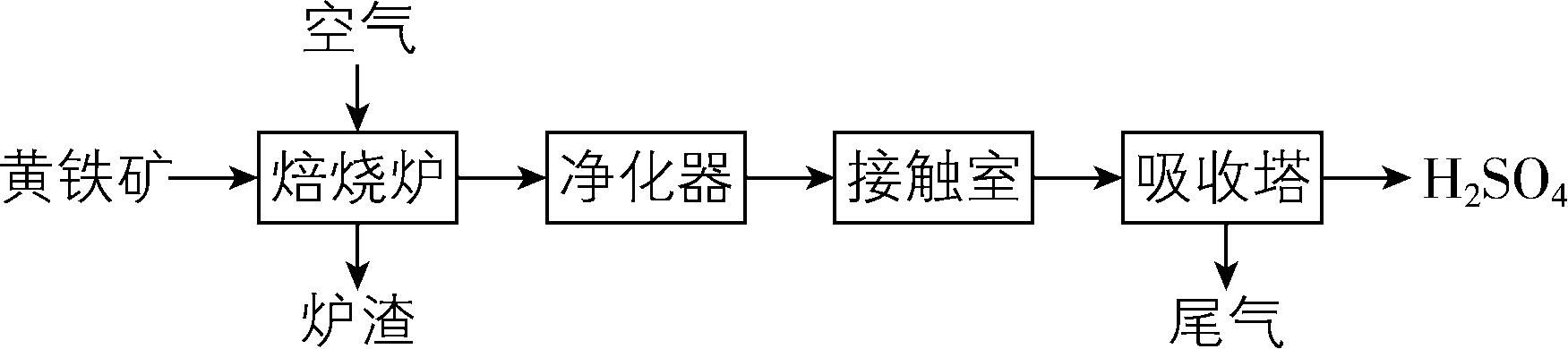
(1) 在接触室发生反应的化学方程式为 。
(2) 下列说法不正确的是 (填序号)。
A. 焙烧前需将黄铁矿粉碎,目的是增大反应物接触面积,加快反应速率
B. 吸收塔中选用 $ 98.3\% $ 的浓硫酸作吸收剂
C. 图中每一步含硫物质均发生氧化反应
(3) 硫酸工业尾气经处理后排空。空气中二氧化硫的简易测定方法如图所示。
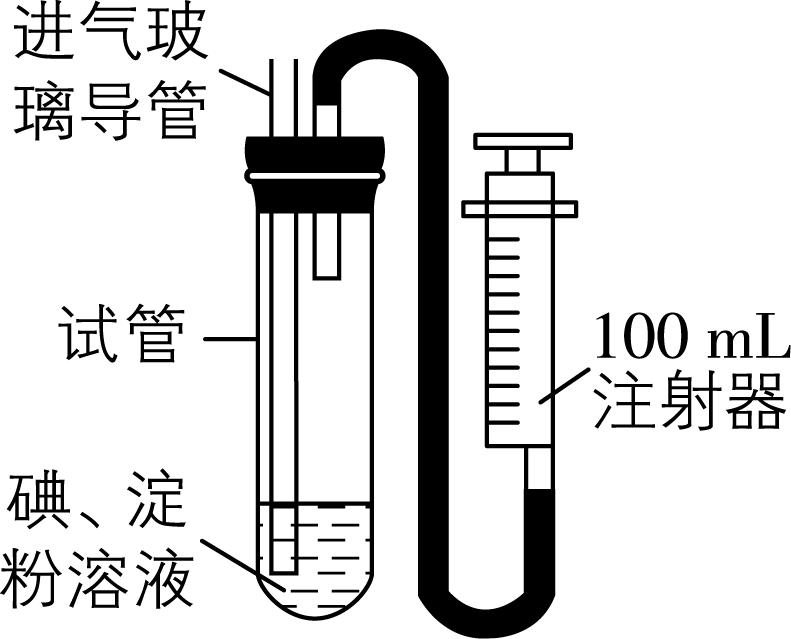
①准确移取 $ {\rm 5\mathrm{m}\mathrm{L}5×{10}^{-4}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 碘溶液,注入测定装置的试管中,加入 $ 2~3 $ 滴淀粉溶液。
②连接仪器,在测定地点慢慢抽气,每次抽气 $ {\rm 100\mathrm{m}\mathrm{L}} $ ,直到溶液的颜色全部褪尽为止,共抽气 $ n $ 次。
$ \mathrm{a} $ .抽气时溶液褪色,反应的化学方程式是 。
$ \mathrm{b} $ .空气中二氧化硫的含量为 $ {\rm \mathrm{m}\mathrm{g}\cdot {\mathrm{L}}^{-1}} $ 。
$ \mathrm{c} $ .若空气中二氧化硫的允许含量为 $ {\rm 0.02\mathrm{m}\mathrm{g}\cdot {\mathrm{L}}^{-1}} $ ,则抽气次数 $ n⩾ $ 才符合标准,否则超标。
答案:(1) $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{△}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $
(2) C
(3) $ {\rm \mathrm{a}.{\mathrm{I}}_{2}+{\mathrm{S}\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}2\mathrm{H}\mathrm{I}+{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ ; $ \mathrm{b} $ . $ \dfrac{1.6}{n} $ ; $ \mathrm{c}.80 $
解析:(1) 在接触室内二氧化硫转化为三氧化硫,发生反应的化学方程式为 $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{△}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $ 。
(2) 将黄铁矿粉碎,目的是增大反应物接触面积,加快反应速率, $ {\rm \mathrm{A}} $ 正确;为了避免形成酸雾,吸收塔中可选用 $ 98.3\% $ 的浓硫酸作吸收剂, $ {\rm \mathrm{B}} $ 正确;吸收塔中发生的反应为 $ {\rm {\mathrm{S}\mathrm{O}}_{3}+{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ ,含硫物质没有发生氧化反应, $ {\rm \mathrm{C}} $ 错误。
(3) 准确移取 $ {\rm 5\mathrm{m}\mathrm{L}5×{10}^{-4}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 碘溶液,注入测定装置的试管中,加入 $ 2~3 $ 滴淀粉溶液,单质碘遇淀粉变为蓝色,则此时溶液呈蓝色;连接仪器,在测定地点慢慢抽气,每次抽气 $ {\rm 100\mathrm{m}\mathrm{L}} $ ,直到溶液的颜色全部褪尽为止,共抽气 $ n $ 次。 $ \mathrm{a} $ .抽气时溶液褪色,则二氧化硫和单质碘反应生成硫酸和氢碘酸,反应的化学方程式是 $ {\rm {\mathrm{I}}_{2}+{\mathrm{S}\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}2\mathrm{H}\mathrm{I}+{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 。 $ \mathrm{b} $ .空气中二氧化硫的含量为 $ {\rm \dfrac{5×{10}^{-4}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}×5×{10}^{-3}\mathrm{L}×64×{10}^{3}\mathrm{m}\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}{100n×{10}^{-3}\mathrm{L}}=\dfrac{1.6}{n}\mathrm{m}\mathrm{g}\cdot {\mathrm{L}}^{-1}} $ 。 $ \mathrm{c} $ .若空气中二氧化硫的允许含量为 $ {\rm 0.02\mathrm{m}\mathrm{g}\cdot {\mathrm{L}}^{-1}} $ ,即 $ {\rm \dfrac{1.6}{n}\mathrm{m}\mathrm{g}\cdot {\mathrm{L}}^{-1}⩽ 0.02\mathrm{m}\mathrm{g}\cdot {\mathrm{L}}^{-1}} $ ,解得 $ n⩾ 80 $ ,则 $ n⩾ 80 $ 才符合标准,否则超标。
4.同学们探究不同金属和浓硫酸的反应,向三等份浓硫酸中分别加入相同大小的不同金属片,加热,用生成气体进行如表所示实验并记录实验现象。
实验操作 | 实验现象 |
铜片 | 锌片 | 铝片 |
点燃 | 不燃烧 | 燃烧 | 燃烧 |
通入酸性 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液 | 褪色 | 褪色 | 褪色 |
通入 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ 溶液 | 无明显变化 | 无明显变化 | 出现黑色沉淀 |
通入品红溶液 | 褪色 | 褪色 | 不褪色 |
注: $ {\rm {\mathrm{H}}_{2}\mathrm{S}+{\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}\xlongequal{}\mathrm{C}\mathrm{u}\mathrm{S}↓+{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}(\mathrm{C}\mathrm{u}\mathrm{S}} $ 为黑色固体, $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 可燃 $ ) $ 。
下列说法不正确的是( )
A. 加入铜片的实验中,使酸性 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液褪色的是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $
B. 加入铝片的实验中,燃烧现象能证明生成的气体中一定含 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $
C. 加入锌片的实验中,生成的气体一定是混合气体
D. 金属与浓硫酸反应的还原产物与金属活动性强弱有关
答案:B
解析:铜片实验中,生成的气体不燃烧,但能使酸性 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液和品红溶液褪色,说明该气体具有还原性、漂白性,则该气体为 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ , $ {\rm \mathrm{A}} $ 正确;铝片实验中,燃烧现象可能由 $ {\rm {\mathrm{H}}_{2}} $ 或 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 引起,不能仅通过燃烧现象断言 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 一定存在, $ {\rm \mathrm{B}} $ 错误;锌片实验中,气体使品红褪色说明含 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,再根据燃烧及通入 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ 溶液无现象推知,随着反应的进行,浓硫酸变稀, $ {\rm \mathrm{Z}\mathrm{n}} $ 与稀硫酸反应有 $ {\rm {\mathrm{H}}_{2}} $ 生成,则生成的气体必为混合气体, $ {\rm \mathrm{C}} $ 正确;不同金属与浓硫酸反应的还原产物 $ {\rm ({\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 等 $ ) $ 不同,证明还原产物与金属活动性强弱相关, $ {\rm \mathrm{D}} $ 正确。








