课时3 不同价态含硫物质的转化
一、刷基础
1.下列有关硫及其化合物的说法正确的是( )
A. $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 均具有还原性,故浓 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 均能氧化 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $
B. 金属单质与硫通过化合反应可以制得 $ {\rm \mathrm{F}\mathrm{e}\mathrm{S}} $ 或 $ {\rm \mathrm{C}\mathrm{u}\mathrm{S}} $
C. 向溶液中加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液后滴加硝酸(具有强氧化性),若产生不溶于硝酸的白色沉淀,则原溶液必含 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $
D. 常温下,铁块与足量冷浓硫酸混合会发生化学反应,但最终铁块仍有剩余
答案:D
解析: $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 中硫为 $ +4 $ 价,浓 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 中硫为 $ +6 $ 价,价态相邻,不能发生氧化还原反应,浓 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 不能氧化 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{A}} $ 错误;铁与硫加热生成 $ {\rm \mathrm{F}\mathrm{e}\mathrm{S}} $ ,铜与硫加热生成 $ {\rm {\mathrm{C}\mathrm{u}}_{2}\mathrm{S}} $ ,无法通过化合反应直接制得 $ {\rm \mathrm{C}\mathrm{u}\mathrm{S}} $ , $ {\rm \mathrm{B}} $ 错误;加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 后滴加硝酸,若原溶液含 $ {\rm {\mathrm{S}\mathrm{O}}_{3}^{2-}} $ 或 $ {\rm {\mathrm{A}\mathrm{g}}^{+}} $ 等,可能生成 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}} $ (后被硝酸氧化为 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ )或 $ {\rm \mathrm{A}\mathrm{g}\mathrm{C}\mathrm{l}} $ 沉淀,无法确定原溶液一定含 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ , $ {\rm \mathrm{C}} $ 错误;常温下铁遇冷浓 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 发生钝化,表面生成致密薄膜阻止反应进行,最终铁块仍有剩余, $ {\rm \mathrm{D}} $ 正确。
2.黄铁矿的主要成分为 $ {\rm {\mathrm{F}\mathrm{e}\mathrm{S}}_{2}(\mathrm{S}} $ 为 $ -1 $ 价 $ ) $ ,是生产硫黄和硫酸的主要原料,黄铁矿在硫酸酸化的条件下发生催化氧化的反应历程如图所示,下列说法错误的是( )
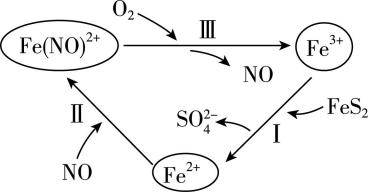
A. 反应Ⅰ后溶液的酸性增强
B. 反应Ⅱ中 $ {\rm {\mathrm{F}\mathrm{e}}^{2+}} $ 被 $ {\rm \mathrm{N}\mathrm{O}} $ 氧化
C. 反应Ⅲ中每生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}} $ 分子,转移 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 电子
D. 该过程的总反应为 $ {\rm 4{\mathrm{F}\mathrm{e}\mathrm{S}}_{2}+15{\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}{{\underline{ \underline { \rm{~ \mathrm{N}\mathrm{O}、{\mathrm{F}\mathrm{e}}^{3+} ~} } }} \atop{~{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}}}2{\mathrm{F}\mathrm{e}}_{2}({\mathrm{S}\mathrm{O}}_{4})_{3}+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $
答案:B
解析:由图可知,反应Ⅰ的离子方程式为 $ {\rm 14{\mathrm{F}\mathrm{e}}^{3+}+{\mathrm{F}\mathrm{e}\mathrm{S}}_{2}+8{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}15{\mathrm{F}\mathrm{e}}^{2+}+2{\mathrm{S}\mathrm{O}}_{4}^{2-}+16{\mathrm{H}}^{+}} $ ,有氢离子生成,反应后溶液的酸性增强, $ {\rm \mathrm{A}} $ 正确;反应Ⅱ为 $ {\rm {\mathrm{F}\mathrm{e}}^{2+}+\mathrm{N}\mathrm{O}\xlongequal{}\mathrm{F}\mathrm{e}(\mathrm{N}\mathrm{O})^{2+}} $ ,反应Ⅱ中铁元素化合价不变, $ {\rm {\mathrm{F}\mathrm{e}}^{2+}} $ 没有被 $ {\rm \mathrm{N}\mathrm{O}} $ 氧化, $ {\rm \mathrm{B}} $ 错误;反应Ⅲ的离子方程式为 $ {\rm 4\mathrm{F}\mathrm{e}(\mathrm{N}\mathrm{O})^{2+}+{\mathrm{O}}_{2}+4{\mathrm{H}}^{+}\xlongequal{}4{\mathrm{F}\mathrm{e}}^{3+}+4\mathrm{N}\mathrm{O}+2{\mathrm{H}}_{2}\mathrm{O}} $ ,可知每生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}} $ 分子,同时生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{F}\mathrm{e}}^{3+}} $ ,铁元素化合价由 $ +2 $ 升高为 $ +3 $ ,转移 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 电子, $ {\rm \mathrm{C}} $ 正确;根据反应历程图, $ {\rm {\mathrm{F}\mathrm{e}\mathrm{S}}_{2}} $ 被氧气氧化为 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 和 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,根据得失电子守恒、原子守恒可得总反应方程式为 $ {\rm 4{\mathrm{F}\mathrm{e}\mathrm{S}}_{2}+15{\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}{{\underline{ \underline { \rm{~ \mathrm{N}\mathrm{O}、{\mathrm{F}\mathrm{e}}^{3+} ~} } }} \atop{~{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}}}2{\mathrm{F}\mathrm{e}}_{2}({\mathrm{S}\mathrm{O}}_{4})_{3}+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ , $ {\rm \mathrm{D}} $ 正确。
3.某研究小组为探究 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 晶体在空气中变质后的产物,进行实验并记录现象如下:
①取 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 样品加水溶解,得到澄清溶液 $ \mathrm{a} $ ;
②取少量溶液 $ \mathrm{a} $ 加入过量盐酸,有臭鸡蛋气味的气体放出,且出现黄色浑浊;
③将②中浊液过滤,向滤液中加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀。
资料: $ {\rm ⅰ.{\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 在空气中潮解生成 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{x}} $ , $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{x}} $ 与酸反应生成 $ {\rm \mathrm{S}} $ 和 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ (有臭鸡蛋气味);
$ {\rm ⅱ.\mathrm{B}\mathrm{a}\mathrm{S}} $ 易溶于水。
下列说法不正确的是( )
A. ②中黄色浑浊可能是 $ {\rm {\mathrm{S}}_{x}^{2-}} $ 与 $ {\rm {\mathrm{H}}^{+}} $ 反应产生的
B. ①和②说明该 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 样品中含有 $ {\rm \mathrm{S}} $
C. ③中白色沉淀是 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $
D. 该 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 样品中可能含有 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $
答案:B
解析:由题给资料信息ⅰ可知,②中黄色浑浊可能是 $ {\rm {\mathrm{S}}_{x}^{2-}} $ 与 $ {\rm {\mathrm{H}}^{+}} $ 反应产生的 $ {\rm \mathrm{S}} $ 单质, $ {\rm \mathrm{A}} $ 正确; $ {\rm \mathrm{S}} $ 难溶于水,而①取 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 样品加水溶解,得到澄清溶液 $ \mathrm{a} $ ,则说明该 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 样品中不可能含有 $ {\rm \mathrm{S}} $ , $ {\rm \mathrm{B}} $ 错误;③将②中浊液过滤,滤液中含有过量的 $ {\rm \mathrm{H}\mathrm{C}\mathrm{l}} $ ,向滤液中加入 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,产生白色沉淀,该白色沉淀是 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ , $ {\rm \mathrm{C}} $ 正确;由于 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}+2\mathrm{H}\mathrm{C}\mathrm{l}\xlongequal{}2\mathrm{N}\mathrm{a}\mathrm{C}\mathrm{l}+{\mathrm{H}}_{2}\mathrm{S}↑} $ , $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+2\mathrm{H}\mathrm{C}\mathrm{l}\xlongequal{}2\mathrm{N}\mathrm{a}\mathrm{C}\mathrm{l}+{\mathrm{H}}_{2}\mathrm{O}+{\mathrm{S}\mathrm{O}}_{2}↑} $ , $ {\rm 2{\mathrm{H}}_{2}\mathrm{S}+{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}3\mathrm{S}↓+2{\mathrm{H}}_{2}\mathrm{O}} $ ,故该 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 样品中可能含有 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{D}} $ 正确。
4.物质的类别和核心元素的化合价是研究
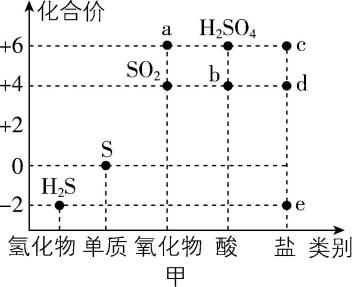
物质性质的两个重要维度。图甲是硫及其部分化合物的“价—类”二维图。
(1) 据图中信息,写出物质 $ \mathrm{a} $ 和 $ \mathrm{b} $ 的化学式: $ \mathrm{a} $ ; $ \mathrm{b} $ 。
(2) $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{5}} $ 和 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 在化工生产中应用广泛,若将 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{5}} $ 归入图中,应置于图中的 (填图中对应的字母)点。已知: $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}+{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}\xlongequal{}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}+{\mathrm{S}\mathrm{O}}_{2}↑+\mathrm{S}↓+{\mathrm{H}}_{2}\mathrm{O}} $ ,此反应中的物质没有涉及的类别是 (填序号)。
A.单质 B.酸性氧化物 C.酸 D.碱 E.盐
(3) 将 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 通入以下溶液,溶液均会发生颜色变化,其中能说明 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 具有还原性的是 (填序号)。
A. 溴水B. 品红溶液
C. 滴有酚酞的氢氧化钠溶液D. $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 溶液
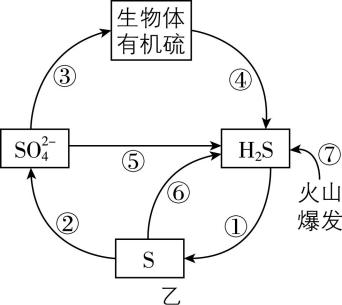
(4) 部分含 $ {\rm \mathrm{S}} $ 物质的转化如图乙所示。过程①可利用克劳斯法实现,该法先将部分 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 通过燃烧转化为 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,再将 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与剩余的 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 混合。为实现硫的最大回收,燃烧的 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 和剩余的 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 物质的量之比应为 。过程②宜在土壤的 (填“富氧”或“缺氧”)区实现。
答案:(1) $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ ; $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $
(2) $ \mathrm{d} $ ;D
(3) A
(4) $ 1:2 $ ;富氧
解析:(1) 根据题图甲可知 $ \mathrm{a} $ 是 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ , $ \mathrm{b} $ 是 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ 。
(2) $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{5}} $ 中钠元素为 $ +1 $ 价,氧元素为 $ -2 $ 价,依据化合物中各元素化合价代数和为零的原则,硫元素的平均化合价为 $ +4 $ 价,又因其是钠盐,所以应置于图中 $ \mathrm{d} $ 点。题给反应中 $ {\rm \mathrm{S}} $ 为单质, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 为酸性氧化物, $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 为酸, $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 为盐,故选 $ {\rm \mathrm{D}} $ 。
(3) $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 可以和溴水发生氧化还原反应生成 $ {\rm \mathrm{H}\mathrm{B}\mathrm{r}} $ 和 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ ,溴水褪色,说明二氧化硫具有还原性; $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 使品红溶液褪色,说明二氧化硫具有漂白性; $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 可以和 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 反应生成 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ ,使滴有酚酞的氢氧化钠溶液褪色,说明二氧化硫具有酸性氧化物的性质; $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 反应生成黄色浑浊 $ {\rm \mathrm{S}} $ ,说明二氧化硫具有氧化性。所以选 $ {\rm \mathrm{A}} $ 。
(4) $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 发生反应: $ {\rm {\mathrm{S}\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{S}\xlongequal{}3\mathrm{S}+2{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 完全反应时物质的量之比应为 $ 1:2 $ ,所以燃烧的 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 和剩余的 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 物质的量之比应为 $ 1:2 $ ;由题图乙可知,过程②中 $ {\rm \mathrm{S}} $ 转化为 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,增加了氧元素,根据元素守恒知,过程②在土壤的富氧区能够实现。
二、刷提升
1.硫元素及其化合物之间存在如图所示的转化关系,下列说法正确的是( )
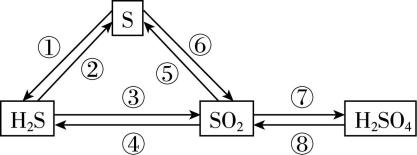
A. 反应③可以在氧气不足的情况下实现
B. 反应⑥可以在加入过量酸性高锰酸钾溶液的情况下实现
C. 反应⑦只需与水化合就能实现
D. 反应⑧可以通过复分解反应实现
答案:D
解析: $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 完全燃烧生成 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,氧气不足时, $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 会被氧气氧化为硫单质, $ {\rm \mathrm{A}} $ 错误;酸性高锰酸钾溶液具有强氧化性,过量的酸性高锰酸钾溶液会将 $ {\rm \mathrm{S}} $ 直接氧化为硫酸根离子, $ {\rm \mathrm{B}} $ 错误;二氧化硫需被氧化剂氧化为 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ 后再与水反应才能生成 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ , $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和水反应生成 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{C}} $ 错误;硫酸和亚硫酸钠发生复分解反应生成硫酸钠、二氧化硫和水, $ {\rm \mathrm{D}} $ 正确。
2.某硫酸厂废气中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的回收利用方案如图所示,下列说法错误的是( )
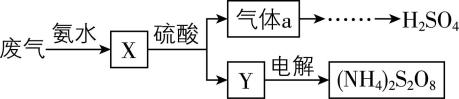
A. $ {\rm \mathrm{X}} $ 可能含有2种盐
B. $ \mathrm{a} $ 是 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $
C. $ {\rm \mathrm{Y}} $ 可能含有 $ {\rm ({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{S}\mathrm{O}}_{4}} $
D. 可用热的 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液和湿润的红色石蕊试纸检验 $ {\rm ({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{8}} $ 中的 $ {\rm {\mathrm{N}\mathrm{H}}_{4}^{+}} $
答案:B
解析:废气中的二氧化硫与氨水反应生成亚硫酸铵或亚硫酸氢铵, $ {\rm \mathrm{A}} $ 正确;亚硫酸铵或亚硫酸氢铵与硫酸反应生成气体 $ \mathrm{a} $ ,则气体 $ \mathrm{a} $ 为二氧化硫,而不是三氧化硫, $ {\rm \mathrm{B}} $ 错误; $ {\rm \mathrm{X}} $ 和硫酸反应生成硫酸铵或硫酸氢铵, $ {\rm \mathrm{C}} $ 正确;可用热的 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液和湿润的红色石蕊试纸检验 $ {\rm ({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{8}} $ 中的 $ {\rm {\mathrm{N}\mathrm{H}}_{4}^{+}} $ ,现象是红色石蕊试纸变蓝, $ {\rm \mathrm{D}} $ 正确。
3.大气污染物 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 易溶于水,通常表现出较强的还原性,对人体的呼吸系统和中枢神经系统等均有毒性作用。认识和了解 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的性质可有效防治 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 对环境的污染,并实现 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的综合利用。某研究团队提出的 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 烟气脱硫工艺流程如下,该流程中脱硫剂可循环利用,实现对烟气中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的持续脱除。已知:脱硫塔中发生的主要反应为 $ {\rm 2\mathrm{C}\mathrm{a}\mathrm{S}+3{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}2{\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}+3\mathrm{S}} $ , $ {\rm 2{\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}+{\mathrm{O}}_{2}\xlongequal{}2{\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ 。
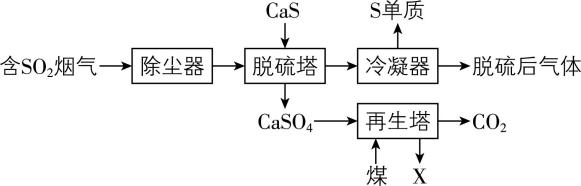
下列有关说法正确的是( )
A. 脱硫塔中反应生成的 $ {\rm \mathrm{S}} $ 为还原产物
B. 经冷凝器得到的几种单质 $ {\rm {\mathrm{S}}_{2}} $ 、 $ {\rm {\mathrm{S}}_{4}} $ 、 $ {\rm {\mathrm{S}}_{6}} $ 和 $ {\rm {\mathrm{S}}_{8}} $ 互为同位素
C. 将 $ {\rm {\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ 和煤粉碎混合,再投入再生塔,有利于反应充分进行
D. 再生塔中得到的 $ {\rm \mathrm{X}} $ 主要成分为 $ {\rm {\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}} $
答案:C
解析:脱硫塔中发生反应: $ {\rm 2\mathrm{C}\mathrm{a}\mathrm{S}+3{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}2{\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{3}+3\mathrm{S}} $ ,反应中 $ {\rm \mathrm{C}\mathrm{a}\mathrm{S}\to \mathrm{S}} $ 、 $ {\rm {\mathrm{S}\mathrm{O}}_{2}\to \mathrm{S}} $ ,根据价态规律, $ {\rm \mathrm{S}} $ 既是氧化产物又是还原产物, $ {\rm \mathrm{A}} $ 错误; $ {\rm {\mathrm{S}}_{2}} $ 、 $ {\rm {\mathrm{S}}_{4}} $ 、 $ {\rm {\mathrm{S}}_{6}} $ 和 $ {\rm {\mathrm{S}}_{8}} $ 为 $ {\rm \mathrm{S}} $ 的不同单质,互为同素异形体, $ {\rm \mathrm{B}} $ 错误;将 $ {\rm {\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ 和煤粉碎混合,增大反应物间的接触面积,有利于反应充分进行, $ {\rm \mathrm{C}} $ 正确;再生塔中煤与 $ {\rm {\mathrm{C}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ 反应生成 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 和 $ {\rm \mathrm{X}} $ ,根据原子守恒和得失电子守恒,并结合题干信息“脱硫剂可循环利用”,可判断 $ {\rm \mathrm{X}} $ 为 $ {\rm \mathrm{C}\mathrm{a}\mathrm{S}} $ , $ {\rm \mathrm{D}} $ 错误。
4. $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性环境下易分解生成 $ {\rm \mathrm{S}} $ 和 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 。某小组设计了如图实验装置制备 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ (夹持及加热仪器略)。回答下列问题:
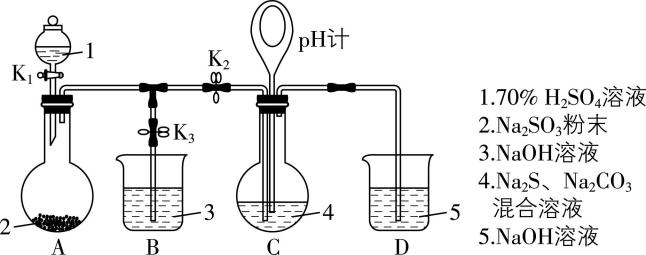
(1) 装置A的作用是制备 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,反应的化学方程式为 。
(2) 完成如表实验过程:
操作步骤 | 装置C中实验现象 | 解释原因 |
检查装置气密性后,添加药品 | $ {\rm \mathrm{p}\mathrm{H}} $ 计读数约为13 | $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ 混合溶液呈碱性 |
打开 $ {\rm {\mathrm{K}}_{2}} $ ,关闭 $ {\rm {\mathrm{K}}_{3}} $ ,调节 $ {\rm {\mathrm{K}}_{1}} $ 使硫酸缓慢匀速滴下 | ⅰ.导管口有气泡冒出,① 。 $ {\rm ⅱ.\mathrm{p}\mathrm{H}} $ 计读数逐渐② | 反应分步进行: $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}+{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+{\mathrm{C}\mathrm{O}}_{2}} $ ; $ {\rm 2{\mathrm{N}\mathrm{a}}_{2}\mathrm{S}+3{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}2{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+3\mathrm{S}↓} $ ; $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+\mathrm{S}\xlongequal{}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ (较慢) |
当 $ {\rm \mathrm{p}\mathrm{H}} $ 计读数接近7时,立即停止通 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,操作是③ | — | 必须立即停止通 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的原因:④ |
(3) 该实验以 $ {\rm n({\mathrm{N}\mathrm{a}}_{2}\mathrm{S}):n({\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3})=2:1} $ 反应并生成 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ ,写出制备 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 的总反应的化学方程式: 。
(4) $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 有还原性,可作脱氯剂。向 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 溶液中通入少量 $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $ ,某同学预测 $ {\rm {\mathrm{S}}_{2}{\mathrm{O}}_{3}^{2-}} $ 转化为 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ ,设计实验验证该预测:取少量反应后的溶液于试管中, 。
答案:(1) $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}(浓)\xlongequal{}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}+{\mathrm{S}\mathrm{O}}_{2}↑+{\mathrm{H}}_{2}\mathrm{O}} $
(2) 溶液出现黄色浑浊,然后逐渐澄清(或浑浊减少);减小;关闭 $ {\rm {\mathrm{K}}_{1}} $ 、 $ {\rm {\mathrm{K}}_{2}} $ ,同时打开 $ {\rm {\mathrm{K}}_{3}} $ ; $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 过量会使溶液呈酸性,产物分解,产率降低
(3) $ {\rm 2{\mathrm{N}\mathrm{a}}_{2}\mathrm{S}+{\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}+4{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}3{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}+{\mathrm{C}\mathrm{O}}_{2}} $
(4) 加入过量盐酸,充分反应后,静置,向上层清液中滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,有白色沉淀生成
解析:(1) 根据装置 $ {\rm \mathrm{A}} $ 中原料,可知装置 $ {\rm \mathrm{A}} $ 中发生反应的化学方程式为 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}(浓)\xlongequal{}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}+{\mathrm{S}\mathrm{O}}_{2}↑+{\mathrm{H}}_{2}\mathrm{O}} $ 。
(2) ①根据反应分步进行的化学方程式: $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}+{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+{\mathrm{C}\mathrm{O}}_{2}} $ , $ {\rm 2{\mathrm{N}\mathrm{a}}_{2}\mathrm{S}+3{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}2{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+3\mathrm{S}↓} $ , $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{3}+\mathrm{S}\xlongequal{}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ (较慢),可知随 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的通入,有黄色沉淀产生,溶液变浑浊,然后生成的 $ {\rm \mathrm{S}} $ 被逐渐消耗,溶液逐渐变澄清。② $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 是酸性气体,反应消耗 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}({\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 的混合溶液呈碱性 $ ) $ ,生成 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 和 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ ,溶液 $ {\rm \mathrm{p}\mathrm{H}} $ 减小,故 $ {\rm \mathrm{p}\mathrm{H}} $ 计读数逐渐减小。③当 $ {\rm \mathrm{p}\mathrm{H}} $ 计读数接近7时,立即停止通 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,操作是关闭 $ {\rm {\mathrm{K}}_{1}} $ 、 $ {\rm {\mathrm{K}}_{2}} $ ,同时打开 $ {\rm {\mathrm{K}}_{3}} $ ,用 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液吸收过量 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 。④已知 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 在中性或碱性环境中稳定,在酸性环境下易分解生成 $ {\rm \mathrm{S}} $ 和 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,若 $ {\rm \mathrm{p}\mathrm{H}} $ 接近7时继续通入 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,会使溶液呈酸性, $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 分解,产率降低。
(3) 以 $ {\rm n({\mathrm{N}\mathrm{a}}_{2}\mathrm{S}):n({\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3})=2:1} $ 反应生成 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ ,故制备 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 的总反应的化学方程式为 $ {\rm 2{\mathrm{N}\mathrm{a}}_{2}\mathrm{S}+{\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}+4{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}3{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}+{\mathrm{C}\mathrm{O}}_{2}} $ 。
(4) 检验 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 时要先加盐酸酸化,再滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,由于通入的氯气少量,而过量的 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 与盐酸反应会产生 $ {\rm \mathrm{S}} $ (黄色浑浊),不利于观察 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{S}\mathrm{O}}_{4}} $ 白色沉淀,故要先除去 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ ;因此具体操作是取少量反应后的溶液于试管中,加入过量盐酸,充分反应后,静置,向上层清液中滴加 $ {\rm {\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,有白色沉淀生成。






