课时3 硝酸
一、刷基础
1.关于硝酸的说法正确的是( )
A. $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 溶于水生成硝酸,所以 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 是酸性氧化物
B. 冷的稀硝酸可以保存在铝、铁制成的容器中
C. 浓硝酸久置会变黄是因为硝酸分解产生的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 溶于其中
D. 硝酸与铜的反应中,硝酸只表现氧化性
答案:C
解析:酸性氧化物与碱反应只能生成一种盐和水,二氧化氮与 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 反应生成 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}} $ 和水,生成了两种盐,所以二氧化氮不是酸性氧化物, $ {\rm \mathrm{A}} $ 错误;稀硝酸具有强氧化性,能与铝、铁反应,所以冷的稀硝酸不能保存在铝、铁制成的容器中, $ {\rm \mathrm{B}} $ 错误;浓硝酸具有不稳定性,久置易分解生成二氧化氮、氧气和水,分解生成的二氧化氮溶于浓硝酸会使溶液变为黄色, $ {\rm \mathrm{C}} $ 正确;铜与硝酸反应时,氮元素的化合价部分降低被还原,部分不变形成 $ {\rm \mathrm{C}\mathrm{u}({\mathrm{N}\mathrm{O}}_{3})_{2}} $ ,硝酸表现酸性和氧化性, $ {\rm \mathrm{D}} $ 错误。
2.下列有关硝酸化学性质的叙述中,正确的是( )
A. 紫色石蕊试纸遇稀硝酸先变红后褪色
B. 稀硝酸能与 $ {\rm \mathrm{F}\mathrm{e}\mathrm{O}} $ 反应,只表现氧化性
C. 浓硝酸保存在棕色玻璃试剂瓶中
D. 硝酸可与 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 反应制得 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 气体
答案:C
解析:紫色石蕊试纸遇稀硝酸变红,不会褪色, $ {\rm \mathrm{A}} $ 错误;稀硝酸能与 $ {\rm \mathrm{F}\mathrm{e}\mathrm{O}} $ 反应生成硝酸铁、 $ {\rm \mathrm{N}\mathrm{O}} $ 和水,表现氧化性和酸性, $ {\rm \mathrm{B}} $ 错误;浓硝酸见光易分解,需要保存在棕色玻璃试剂瓶中, $ {\rm \mathrm{C}} $ 正确; $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 具有还原性,硝酸属于氧化性酸,硝酸与 $ {\rm {\mathrm{N}\mathrm{a}}_{2}\mathrm{S}} $ 反应不能得到 $ {\rm {\mathrm{H}}_{2}\mathrm{S}} $ 气体, $ {\rm \mathrm{D}} $ 错误。
3.一定温度下,探究铜与稀 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 反应过程如图,下列说法错误的是( )
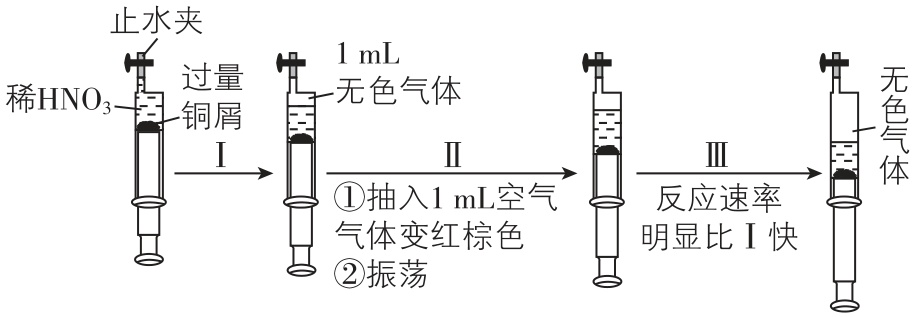
A. 产生无色气体的离子方程式是 $ {\rm 3\mathrm{C}\mathrm{u}+8{\mathrm{H}}^{+}+2{\mathrm{N}\mathrm{O}}_{3}^{-}\xlongequal{}3{\mathrm{C}\mathrm{u}}^{2+}+2\mathrm{N}\mathrm{O}↑+4{\mathrm{H}}_{2}\mathrm{O}} $
B. 步骤Ⅲ反应速率比Ⅰ快的原因是 $ {\rm 3{\mathrm{N}\mathrm{O}}_{2}+{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}2{\mathrm{H}\mathrm{N}\mathrm{O}}_{3}+\mathrm{N}\mathrm{O}} $ ,使 $ {\rm c({\mathrm{H}\mathrm{N}\mathrm{O}}_{3})} $ 增大
C. 无色气体变红棕色的化学方程式是 $ {\rm 2\mathrm{N}\mathrm{O}+{\mathrm{O}}_{2}\xlongequal{}2{\mathrm{N}\mathrm{O}}_{2}} $
D. 当活塞不再移动时,再抽入空气,铜会继续溶解
答案:B
解析: $ {\rm \mathrm{C}\mathrm{u}} $ 和稀 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 反应的离子方程式为 $ {\rm 3\mathrm{C}\mathrm{u}+8{\mathrm{H}}^{+}+2{\mathrm{N}\mathrm{O}}_{3}^{-}\xlongequal{}3{\mathrm{C}\mathrm{u}}^{2+}+2\mathrm{N}\mathrm{O}↑+4{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm \mathrm{A}} $ 正确; $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 转化为 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 后,稀硝酸的浓度仍小于原稀硝酸浓度,对比Ⅰ和Ⅲ的不同知,步骤Ⅲ反应速率比Ⅰ快的原因是二氧化氮对反应具有催化作用, $ {\rm \mathrm{B}} $ 错误;一氧化氮与氧气反应生成二氧化氮,二氧化氮为红棕色,化学方程式为 $ {\rm 2\mathrm{N}\mathrm{O}+{\mathrm{O}}_{2}\xlongequal{}2{\mathrm{N}\mathrm{O}}_{2}} $ , $ {\rm \mathrm{C}} $ 正确;当活塞不再移动时,再抽入空气, $ {\rm \mathrm{N}\mathrm{O}} $ 与氧气、水反应生成硝酸,因此铜可以继续溶解, $ {\rm \mathrm{D}} $ 正确。
4.某中学化学兴趣小组用足量的铜与一定量的浓硝酸充分反应,得到 $ {\rm 0.3\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}\mathrm{O}}_{2}} $ 与 $ {\rm \mathrm{N}\mathrm{O}} $ 的混合气体,这些气体与一定体积的 $ {\rm {\mathrm{O}}_{2}} $ 混合后通入水中,恰好被完全吸收生成硝酸。该兴趣小组又向所得硝酸铜溶液中加 $ {\rm 100\mathrm{m}\mathrm{L}6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液, $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ 恰好沉淀完全。下列说法正确的是( )
A. 参加反应的 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 的物质的量是 $ 0.75\mathrm{m}\mathrm{o}\mathrm{l} $
B. 消耗氧气的体积为 $ {\rm 6.72\mathrm{L}} $ (标准状况下)
C. 混合气体中含 $ {\rm 1.12\mathrm{L}\mathrm{N}\mathrm{O}} $ (标准状况下)
D. 此反应过程中转移了 $ 0.6\mathrm{m}\mathrm{o}\mathrm{l} $ 的电子
答案:D
解析:由思路导引可知,参加反应的硝酸的物质的量为 $ 0.9\mathrm{m}\mathrm{o}\mathrm{l} $ , $ {\rm \mathrm{A}} $ 错误;消耗氧气的物质的量为 $ 0.15\mathrm{m}\mathrm{o}\mathrm{l} $ ,则标准状况下氧气的体积为 $ {\rm 0.15\mathrm{m}\mathrm{o}\mathrm{l}×22.4\mathrm{L}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}=3.36\mathrm{L}} $ , $ {\rm \mathrm{B}} $ 错误;混合气体中一氧化氮的物质的量为 $ 0.15\mathrm{m}\mathrm{o}\mathrm{l} $ ,则标准状况下一氧化氮的体积为 $ {\rm 0.15\mathrm{m}\mathrm{o}\mathrm{l}×22.4\mathrm{L}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}=3.36\mathrm{L}} $ , $ {\rm \mathrm{C}} $ 错误;反应消耗铜的物质的量为 $ 0.3\mathrm{m}\mathrm{o}\mathrm{l} $ ,则反应转移电子的物质的量为 $ 0.3\mathrm{m}\mathrm{o}\mathrm{l}×2=0.6\mathrm{m}\mathrm{o}\mathrm{l} $ , $ {\rm \mathrm{D}} $ 正确。
5.某稀硫酸和稀硝酸的混合溶液 $ {\rm 200\mathrm{m}\mathrm{L}} $ ,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解 $ 19.2\mathrm{g} $ 铜(已知硝酸只被还原为 $ {\rm \mathrm{N}\mathrm{O}} $ 气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是( )
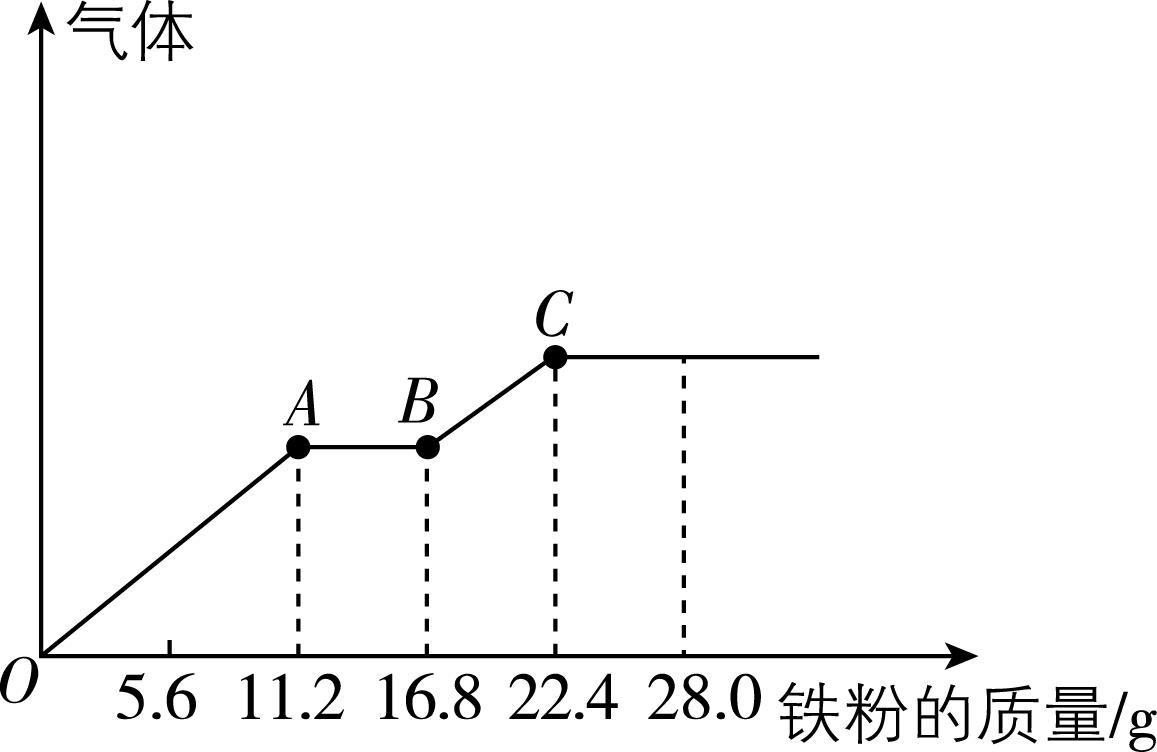
A. 原混合溶液中 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 物质的量为 $ 0.4\mathrm{m}\mathrm{o}\mathrm{l} $
B. $ {\rm AB} $ 段发生的离子反应为 $ {\rm \mathrm{F}\mathrm{e}+2{\mathrm{F}\mathrm{e}}^{3+}\xlongequal{}3{\mathrm{F}\mathrm{e}}^{2+}} $
C. 混合溶液中 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 物质的量浓度为 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
D. 第二份溶液中最终溶质为 $ {\rm {\mathrm{F}\mathrm{e}\mathrm{S}\mathrm{O}}_{4}} $
答案:A
解析:由题给图像可知,加入铁粉至过量过程中, $ {\rm OA} $ 段发生反应 $ {\rm \mathrm{F}\mathrm{e}+{\mathrm{N}\mathrm{O}}_{3}^{-}+4{\mathrm{H}}^{+}\xlongequal{}{\mathrm{F}\mathrm{e}}^{3+}+\mathrm{N}\mathrm{O}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm AB} $ 段发生反应 $ {\rm \mathrm{F}\mathrm{e}+2{\mathrm{F}\mathrm{e}}^{3+}\xlongequal{}3{\mathrm{F}\mathrm{e}}^{2+}} $ , $ {\rm BC} $ 段发生反应 $ {\rm \mathrm{F}\mathrm{e}+2{\mathrm{H}}^{+}\xlongequal{}{\mathrm{F}\mathrm{e}}^{2+}+{\mathrm{H}}_{2}↑} $ , $ {\rm \mathrm{B}} $ 正确;由分析知, $ {\rm B} $ 点溶液中溶质为 $ {\rm {\mathrm{F}\mathrm{e}\mathrm{S}\mathrm{O}}_{4}} $ 和 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ , $ {\rm C} $ 点时, $ {\rm 100\mathrm{m}\mathrm{L}} $ 该溶液反应消耗的 $ 22.4\mathrm{g} $ (即 $ 0.4\mathrm{m}\mathrm{o}\mathrm{l} $ )铁都转化为硫酸亚铁,根据硫酸根离子守恒,可得每份溶液中硫酸的物质的量为 $ 0.4\mathrm{m}\mathrm{o}\mathrm{l} $ ,所以硫酸的浓度是 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ {\rm 200\mathrm{m}\mathrm{L}} $ 的原混合溶液中 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 的物质的量为 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}×0.2\mathrm{L}=0.8\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm \mathrm{A}} $ 错误, $ {\rm \mathrm{D}} $ 正确; $ {\rm OA} $ 段发生反应 $ {\rm \mathrm{F}\mathrm{e}+{\mathrm{N}\mathrm{O}}_{3}^{-}+4{\mathrm{H}}^{+}\xlongequal{}{\mathrm{F}\mathrm{e}}^{3+}+\mathrm{N}\mathrm{O}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm A} $ 点时有 $ {\rm {\mathrm{H}}^{+}} $ 剩余,则 $ {\rm A} $ 点时硝酸全部起氧化剂作用,所以混合溶液中 $ {\rm n({\mathrm{N}\mathrm{O}}_{3}^{-})={n}_{A}(\mathrm{F}\mathrm{e})=\dfrac{11.2\mathrm{g}}{56\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}=0.2\mathrm{m}\mathrm{o}\mathrm{l}} $ ,混合溶液中 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 物质的量浓度为 $ {\rm \dfrac{0.2\mathrm{m}\mathrm{o}\mathrm{l}}{0.1\mathrm{L}}=2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ {\rm \mathrm{C}} $ 正确。
二、刷提升
1.如图所示,氮循环是生物圈内的基本循环之一,研究氮的循环和转化对生产和生活有重要的价值。下列说法错误的是( )
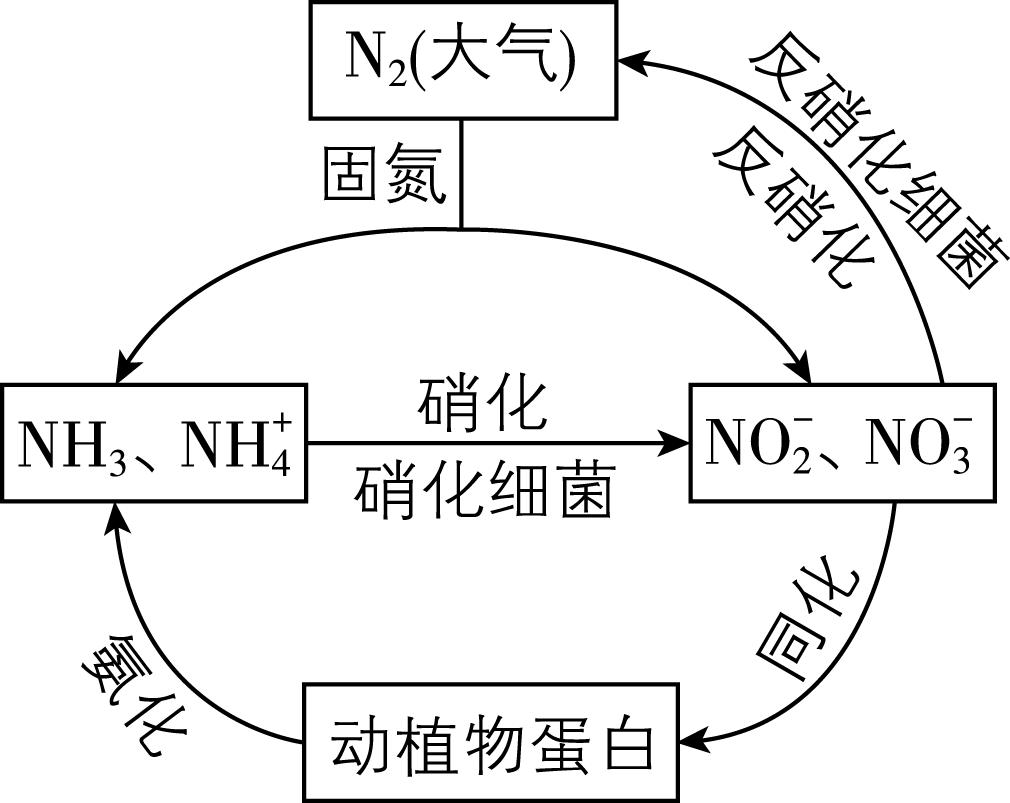
A. 硝化和反硝化过程均为氧化还原反应,反硝化过程中,含氮物质发生还原反应
B. 硝化过程需要有氧化剂参与,反硝化过程有利于氮的良性循环,维持生态平衡
C. 氨态氮与亚硝态氮在氨氧化细菌的作用下转化为氮气的离子方程式: $ {\rm {\mathrm{N}\mathrm{H}}_{4}^{+}+{\mathrm{N}\mathrm{O}}_{2}^{-}\xlongequal{氨氧化细菌}{\mathrm{N}}_{2}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ ,生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ 转移的电子数为3
D. 同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
答案:C
解析:硝化过程为 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 、 $ {\rm {\mathrm{N}\mathrm{H}}_{4}^{+}\to {\mathrm{N}\mathrm{O}}_{2}^{-}} $ 、 $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ ,反硝化过程为 $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ 、 $ {\rm {\mathrm{N}\mathrm{O}}_{2}^{-}\to {\mathrm{N}}_{2}} $ ,均有化合价的变化,故均为氧化还原反应,反硝化过程中 $ {\rm \mathrm{N}} $ 元素的化合价由高价态变为低价态,化合价降低,被还原,故反硝化过程中含氮物质发生还原反应, $ {\rm \mathrm{A}} $ 正确;硝化过程中,氮元素化合价升高,则硝化过程需要有氧化剂参与,反硝化过程中,向大气提供氮气,即反硝化过程利于氮良性循环,维持生态平衡, $ {\rm \mathrm{B}} $ 正确;根据离子反应方程式 $ {\rm {\mathrm{N}\mathrm{H}}_{4}^{+}+{\mathrm{N}\mathrm{O}}_{2}^{-}\xlongequal{氨氧化细菌}{\mathrm{N}}_{2}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ ,生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ 转移 $ 3\mathrm{m}\mathrm{o}\mathrm{l} $ 电子,数目为 $ {\rm 3{N}_{\mathrm{A}}} $ , $ {\rm \mathrm{C}} $ 错误;动植物蛋白为有机物, $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ 、 $ {\rm {\mathrm{N}\mathrm{O}}_{2}^{-}} $ 、 $ {\rm {\mathrm{N}\mathrm{H}}_{4}^{+}} $ 、 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 为无机物,同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化, $ {\rm \mathrm{D}} $ 正确。
2.下列有关实验操作、现象和解释或结论都正确的是( )
序号 | 实验操作 | 现象 | 解释或结论 |
① | 向过量的 $ {\rm \mathrm{F}\mathrm{e}} $ 粉中加入稀硝酸,充分反应后,滴入 $ {\rm \mathrm{K}\mathrm{S}\mathrm{C}\mathrm{N}} $ 溶液 | 溶液呈红色 | 稀硝酸将 $ {\rm \mathrm{F}\mathrm{e}} $ 氧化为 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ |
② | 浓硝酸久置或光照 | 变黄色 | 浓硝酸不稳定,易分解 |
③ | 常温下,将 $ {\rm \mathrm{A}\mathrm{l}} $ 箔插入稀硝酸中 | 无现象 | $ {\rm \mathrm{A}\mathrm{l}} $ 箔表面被 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 氧化,形成致密的薄膜 |
④ | 用玻璃棒蘸取浓硝酸,点到蓝色石蕊试纸上 | 试纸先变红后褪色 | 浓硝酸具有酸性和强氧化性 |
A. ①②
B. ③④
C. ②③④
D. ②④
答案:D
解析:过量的铁粉与稀硝酸反应生成 $ {\rm {\mathrm{F}\mathrm{e}}^{2+}} $ ,再加入 $ {\rm \mathrm{K}\mathrm{S}\mathrm{C}\mathrm{N}} $ 溶液,颜色不变,①错误;浓硝酸久置或光照变黄是 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 分解产生的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 溶于浓硝酸所致,②正确;常温下, $ {\rm \mathrm{A}\mathrm{l}} $ 箔遇浓硝酸钝化,稀硝酸会使 $ {\rm \mathrm{A}\mathrm{l}} $ 箔溶解,③错误;浓硝酸具有酸性和强氧化性,可使蓝色石蕊试纸先变红后褪色,④正确。综上所述,选 $ {\rm \mathrm{D}} $ 。
3.化合价和物质类别是学习元素及其化合物知识的两个要素,可表示为“价—类”二维图。氮元素的“价—类”二维图如图,下列说法正确的是( )
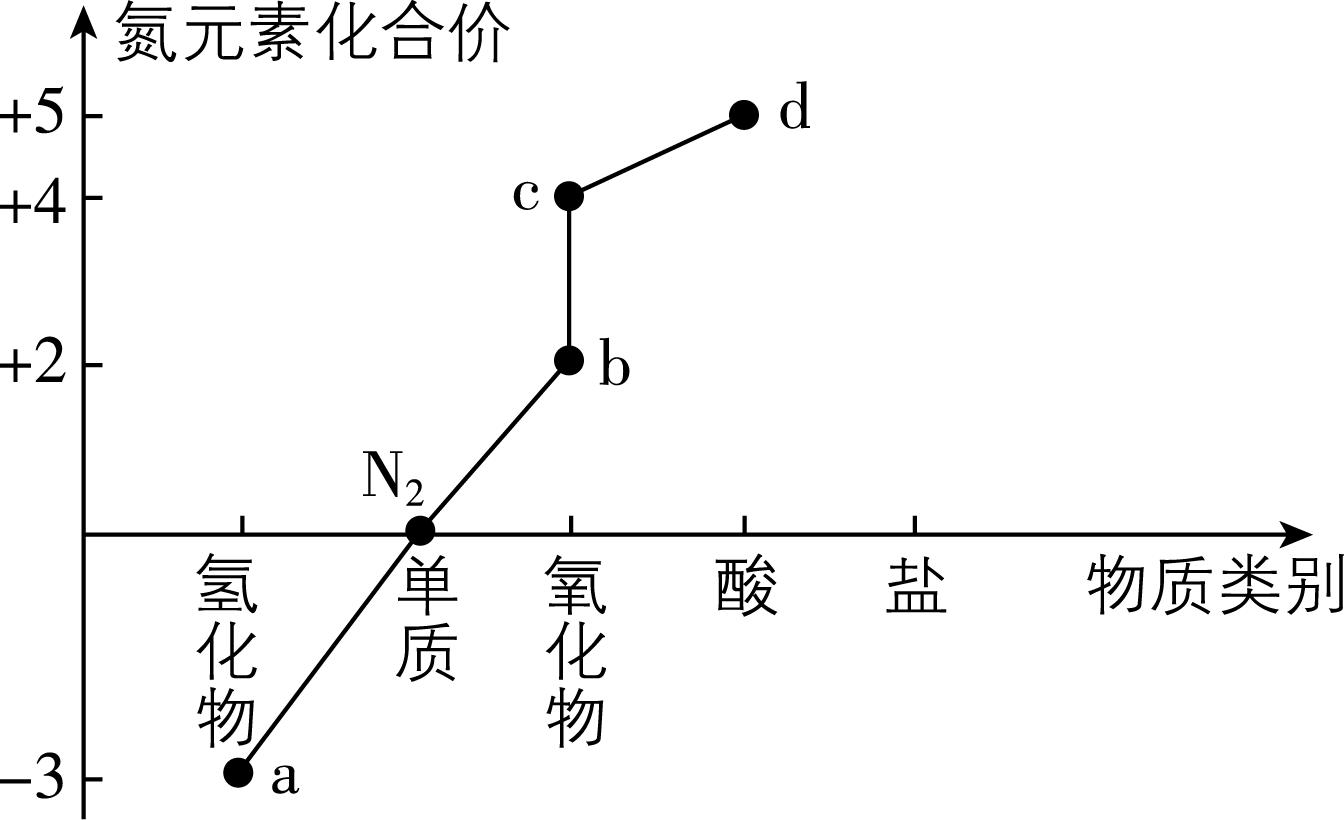
A. $ \mathrm{a} $ 与 $ \mathrm{b} $ 均可用排空气法收集
B. $ \mathrm{a} $ 可以发生催化氧化生成 $ \mathrm{b} $
C. $ \mathrm{c} $ 是酸性氧化物
D. 铜和 $ \mathrm{d} $ 的稀溶液反应, $ \mathrm{d} $ 只表现氧化性
答案:B
解析: $ \mathrm{a} $ 为氨气、 $ \mathrm{b} $ 为一氧化氮、 $ \mathrm{c} $ 为二氧化氮(或四氧化二氮)、 $ \mathrm{d} $ 为硝酸。一氧化氮易与空气中的氧气反应生成二氧化氮,不能用排空气法收集, $ {\rm \mathrm{A}} $ 错误;氨气具有还原性,加热、催化剂作用下氨气与氧气发生催化氧化反应生成一氧化氮和水, $ {\rm \mathrm{B}} $ 正确;二氧化氮与水反应生成硝酸和一氧化氮, $ {\rm \mathrm{N}} $ 由 $ +4 $ 价变为 $ +5 $ 价和 $ +2 $ 价,不能生成 $ +4 $ 价对应的含氧酸,所以二氧化氮不是酸性氧化物, $ {\rm \mathrm{C}} $ 错误;铜与稀硝酸反应生成硝酸铜、一氧化氮和水,反应中氮元素的化合价部分降低被还原、部分不变形成硝酸铜,硝酸表现氧化性和酸性, $ {\rm \mathrm{D}} $ 错误。
4.取 $ 11.2\mathrm{g} $ 铜镁合金,恰好溶解在 $ {\rm 100\mathrm{m}\mathrm{L}} $ 某浓度的硝酸溶液中,生成 $ {\rm \mathrm{N}\mathrm{O}} $ 和 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的混合气体 $ 0.5\mathrm{m}\mathrm{o}\mathrm{l} $ ,向反应后溶液中逐滴滴加 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 溶液,当溶液中金属阳离子全部沉淀,得到 $ 21.4\mathrm{g} $ 沉淀。下列说法不正确的是( )
A. 该合金中 $ {\rm m(\mathrm{C}\mathrm{u}):m(\mathrm{M}\mathrm{g})=4:3} $
B. 原硝酸物质的量浓度为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
C. 硝酸在反应中既体现氧化性又体现酸性
D. 生成的 $ {\rm \mathrm{N}\mathrm{O}} $ 和 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 混合气体能被 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 完全吸收
答案:B
解析:由分析可知,该合金中铜与镁的质量之比为 $ \dfrac{64\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}×0.1\mathrm{m}\mathrm{o}\mathrm{l}}{24\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}×0.2\mathrm{m}\mathrm{o}\mathrm{l}}=\dfrac{4}{3} $ , $ {\rm \mathrm{A}} $ 正确;由题意知, $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 与铜镁合金反应的产物为 $ {\rm \mathrm{N}\mathrm{O}} $ 、 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 、 $ {\rm \mathrm{C}\mathrm{u}({\mathrm{N}\mathrm{O}}_{3})_{2}} $ 、 $ {\rm \mathrm{M}\mathrm{g}({\mathrm{N}\mathrm{O}}_{3})_{2}} $ ,原硝酸的物质的量 $ {\rm n({\mathrm{H}\mathrm{N}\mathrm{O}}_{3})=2n({\mathrm{M}\mathrm{g}}^{2+})+2n({\mathrm{C}\mathrm{u}}^{2+})+n(\mathrm{N}\mathrm{O})+n({\mathrm{N}\mathrm{O}}_{2})=2×0.2\mathrm{m}\mathrm{o}\mathrm{l}+2×0.1\mathrm{m}\mathrm{o}\mathrm{l}+0.5\mathrm{m}\mathrm{o}\mathrm{l}=1.1\mathrm{m}\mathrm{o}\mathrm{l}} $ ,则原硝酸物质的量浓度为 $ {\rm 11\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ {\rm \mathrm{B}} $ 错误;氮元素在反应中有一部分化合价降低得到 $ {\rm \mathrm{N}\mathrm{O}} $ 和 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ,还有一部分化合价未发生变化得到 $ {\rm \mathrm{C}\mathrm{u}({\mathrm{N}\mathrm{O}}_{3})_{2}} $ 、 $ {\rm \mathrm{M}\mathrm{g}({\mathrm{N}\mathrm{O}}_{3})_{2}} $ ,所以硝酸既体现氧化性又体现酸性, $ {\rm \mathrm{C}} $ 正确;设生成的 $ {\rm \mathrm{N}\mathrm{O}} $ 和 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的物质的量分别为 $ a\mathrm{m}\mathrm{o}\mathrm{l} $ 、 $ b\mathrm{m}\mathrm{o}\mathrm{l} $ ,则 $ a+b=0.5 $ ,根据得失电子守恒, $ 3a+b=2×0.1+2×0.2 $ ,两式联立可得: $ a=0.05 $ , $ b=0.45 $ ,由于 $ {\rm \mathrm{N}\mathrm{O}+{\mathrm{N}\mathrm{O}}_{2}+2\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}\xlongequal{}2{\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{2}+{\mathrm{H}}_{2}\mathrm{O}} $ 、 $ {\rm 2{\mathrm{N}\mathrm{O}}_{2}+2\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}\xlongequal{}{\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{2}+{\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}+{\mathrm{H}}_{2}\mathrm{O}} $ ,当 $ {\rm \dfrac{n({\mathrm{N}\mathrm{O}}_{2})}{n(\mathrm{N}\mathrm{O})}⩾ 1} $ 时,氮氧化物能被 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 完全吸收,所以该反应过程中的氮氧化物能被完全吸收, $ {\rm \mathrm{D}} $ 正确。
5.为了探究浓硝酸的性质,进行以下五组实验,均观察到红棕色气体。下列分析错误的是( )
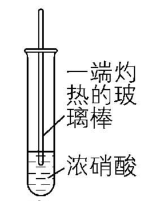
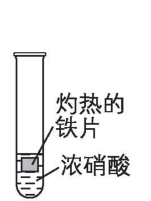
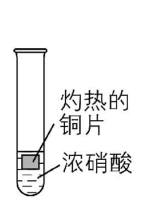
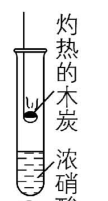
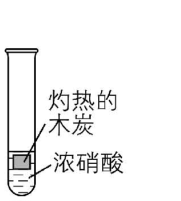
① ② ③ ④ ⑤
A. ①④⑤实验对比,④中的红棕色气体可能是由挥发的浓硝酸受热分解产生的
B. ②中灼热的铁片可与浓硝酸发生反应,生成红棕色的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $
C. 将带火星的木条靠近①的试管口,木条复燃,说明 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 支持燃烧
D. ⑤中的红棕色气体可以证明浓硝酸有不稳定性
答案:D
解析:①中浓硝酸受热分解生成 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ;②中灼热的铁片与浓硝酸发生反应生成 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ;③中灼热的铜片与浓硝酸发生反应生成 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ;④中挥发出的 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 受热发生分解反应生成 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ;⑤中除硝酸分解外,灼热的木炭与浓硝酸还会发生反应: $ {\rm \mathrm{C}+4{\mathrm{H}\mathrm{N}\mathrm{O}}_{3}(浓)\xlongequal{△}4{\mathrm{N}\mathrm{O}}_{2}↑+{\mathrm{C}\mathrm{O}}_{2}↑+2{\mathrm{H}}_{2}\mathrm{O}} $ ,生成 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 。浓硝酸易挥发,挥发出的 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 受热发生分解反应生成红棕色的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ , $ {\rm \mathrm{A}} $ 正确;灼热的铁片与浓硝酸发生反应生成红棕色的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ , $ {\rm \mathrm{B}} $ 正确;灼热的玻璃棒插入浓硝酸中, $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 分解生成 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 、 $ {\rm {\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ ,分解产生的二氧化氮与氧气的物质的量之比为 $ 4:1 $ ,与空气中氮气与氧气的比例相当,空气不能使带火星的木条复燃,而混合气使带火星的木条复燃,说明二氧化氮支持燃烧, $ {\rm \mathrm{C}} $ 正确;⑤中灼热的木炭与浓硝酸发生氧化还原反应也会产生红棕色气体,不能根据生成红棕色气体判断发生了分解反应,即不能证明浓硝酸有不稳定性, $ {\rm \mathrm{D}} $ 错误。
6.铁与不同密度的 $ {\rm {\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ 溶液反应时产生的含氮产物的百分含量分布如图所示,下列有关说法错误的是( )
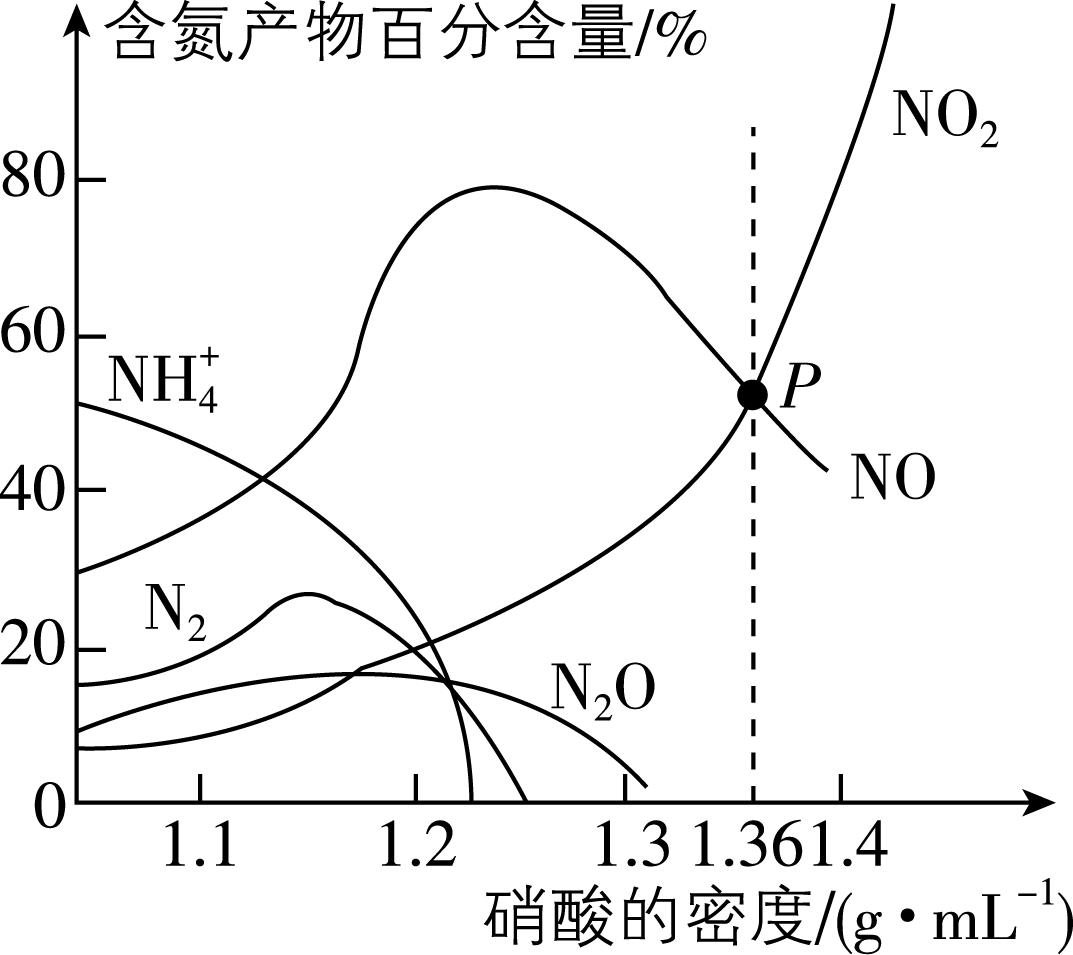
A. 硝酸的密度越大,其还原产物中高价态的成分所占比例越多
B. 一般来说,不同密度的硝酸与铁反应的还原产物不是单一的
C. $ {\rm P} $ 点处氧化剂与还原剂的物质的量之比一定为 $ 2:3 $
D. $ {\rm {\mathrm{N}}_{2}} $ 、 $ {\rm \mathrm{N}\mathrm{O}} $ 、 $ {\rm {\mathrm{N}}_{2}\mathrm{O}} $ 、 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 都既有氧化性又有还原性
答案:C
解析:由题图可知,硝酸的密度越大,其还原产物中高价态的成分所占比例越多, $ {\rm \mathrm{A}} $ 正确;由题图可知,一般来说,不同密度的硝酸与铁反应的还原产物不是单一的, $ {\rm \mathrm{B}} $ 正确; $ {\rm P} $ 点处生成的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 和 $ {\rm \mathrm{N}\mathrm{O}} $ 的百分含量相等,则生成的 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 和 $ {\rm \mathrm{N}\mathrm{O}} $ 物质的量之比为 $ 1:1 $ ,但铁与硝酸反应生成的不一定是 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ ,也可能是 $ {\rm {\mathrm{F}\mathrm{e}}^{2+}} $ , $ {\rm P} $ 点处氧化剂与还原剂的物质的量之比无法确定, $ {\rm \mathrm{C}} $ 错误;氮元素的最低化合价为 $ -3 $ 价,最高价为 $ +5 $ 价, $ {\rm {\mathrm{N}}_{2}} $ 、 $ {\rm \mathrm{N}\mathrm{O}} $ 、 $ {\rm {\mathrm{N}}_{2}\mathrm{O}} $ 、 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 中的 $ {\rm \mathrm{N}} $ 都处于中间价态,都既有氧化性又有还原性, $ {\rm \mathrm{D}} $ 正确。
7.在某 $ {\rm 100\mathrm{m}\mathrm{L}} $ 的混合液中,硝酸和硫酸的物质的量浓度分别是 $ {\rm 0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 、 $ {\rm 0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,向该混合液中加入 $ 1.92\mathrm{g} $ 铜粉,加热,待充分反应后,所得溶液中铜离子的物质的量浓度是(假设反应后溶液体积不变)( )
A. $ {\rm 0.15\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
B. $ {\rm 0.225\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
C. $ {\rm 0.30\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
D. $ {\rm 0.45\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
答案:B
解析:溶液中同时存在 $ {\rm {\mathrm{H}}^{+}} $ 和 $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ 时,能够与 $ {\rm \mathrm{C}\mathrm{u}} $ 发生反应,该溶液中 $ {\rm {\mathrm{H}}^{+}} $ 的物质的量为 $ {\rm 0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}×0.1\mathrm{L}+0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}×2×0.1\mathrm{L}=0.06\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm n(\mathrm{C}\mathrm{u})=\dfrac{m}{M}=\dfrac{1.92\mathrm{g}}{64\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}=0.03\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm n({\mathrm{N}\mathrm{O}}_{3}^{-})=0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}×0.1\mathrm{L}=0.04\mathrm{m}\mathrm{o}\mathrm{l}} $ 。反应的离子方程式为 $ {\rm 3\mathrm{C}\mathrm{u}+8{\mathrm{H}}^{+}+2{\mathrm{N}\mathrm{O}}_{3}^{-}\xlongequal{}3{\mathrm{C}\mathrm{u}}^{2+}+2\mathrm{N}\mathrm{O}↑+4{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm {\mathrm{H}}^{+}} $ 的量不足,应根据 $ {\rm {\mathrm{H}}^{+}} $ 的量进行计算, $ {\rm n({\mathrm{C}\mathrm{u}}^{2+})=\dfrac{3×0.06\mathrm{m}\mathrm{o}\mathrm{l}}{8}=0.0225\mathrm{m}\mathrm{o}\mathrm{l}} $ ,因此 $ {\rm c({\mathrm{C}\mathrm{u}}^{2+})=\dfrac{n({\mathrm{C}\mathrm{u}}^{2+})}{V}=\dfrac{0.0225\mathrm{m}\mathrm{o}\mathrm{l}}{0.1\mathrm{L}}=0.225\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,选 $ {\rm \mathrm{B}} $ 。
8.某研究学习小组对硝酸与二氧化氮的部分性质进行探究。查阅资料:纯硝酸为无色液体;实验室存放的浓硝酸通常显黄色。回答下列问题:
(1) 为探究浓硝酸显黄色的原因,进行如下实验:
实验装置 | 操作 | 实验编号 | $ {\rm \mathrm{M}} $ | 实验现象 |
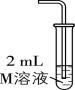
| 向 $ {\rm \mathrm{M}} $ 溶液中按一定速率通入 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 气体 $ 10\mathrm{s} $ | 1 | $ {\rm 6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{H}\mathrm{N}\mathrm{O}}_{3}} $ | 溶液由无色变黄色 |
2 | $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{H}}_{2}\mathrm{S}{\mathrm{O}}_{4}} $ | 溶液由无色变黄色 |
3 | $ {\rm 6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\mathrm{N}\mathrm{a}\mathrm{N}{\mathrm{O}}_{3}} $ | 溶液基本无色 |
4 | | 溶液基本无色 |
① 由实验1和实验3可得出结论:浓硝酸显黄色与 无关。
② 实验4的目的为验证实验2溶液变黄是否与 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 有关,则 $ {\rm \mathrm{M}} $ 为 。
③ 依据上述实验可推知,浓硝酸呈黄色是溶液中 、 共同作用的结果。
(2) 探究 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 的反应。实验装置及步骤如下:
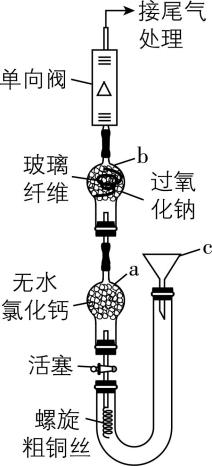
ⅰ.按图连接好装置, ,添加药品。
ⅱ.打开活塞,从仪器 $ \mathrm{c} $ 向 $ {\rm \mathrm{U}} $ 形管中缓慢注入浓硝酸;当浓硝酸快要接触粗铜丝时,关闭活塞,继续注入浓硝酸,使 $ {\rm \mathrm{U}} $ 形管中右侧液面适当高于左侧液面。
ⅲ.慢慢打开活塞,使浓硝酸浸没铜丝;观察到刚进入仪器 $ \mathrm{b} $ 中的红棕色气体迅速褪色,待分散在玻璃纤维上的过氧化钠粉末全部变白后,立即关闭活塞;流出的尾气中未检出 $ {\rm {\mathrm{O}}_{2}} $ 。
① 步骤ⅰ中按图连接好装置后,进行的第一步操作是 。
② 若实验时未使用加有无水氯化钙的仪器 $ \mathrm{a} $ ,则仪器 $ \mathrm{b} $ 中 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 发生某副反应的化学方程式为 。
③ 图中单向阀可实现气体单向流通,其作用是 。
④ 由化合价规律推测, $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 反应生成的物质为 (填化学式)。
答案:(1)① $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $
② $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $
③ $ {\rm {\mathrm{H}}^{+}} $ ; $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $
(2) ① 检查装置气密性
② $ {\rm 2{\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}4\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}+{\mathrm{O}}_{2}↑} $
③ 防止空气中的 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ 、 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 进入仪器 $ \mathrm{b} $ 中
④ $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}} $
解析:(1)① 实验1和实验3中 $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ 浓度相同,阳离子浓度相同,种类不同,说明浓硝酸显黄色与 $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ 无关。
② 根据单一变量原则,实验2和实验4中 $ {\rm {\mathrm{S}\mathrm{O}}_{4}^{2-}} $ 浓度相同,阳离子浓度相同,种类不同,则实验4中的 $ {\rm \mathrm{M}} $ 为 $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 。
③ 实验2和实验4说明浓硝酸显黄色与硫酸根离子无关,实验1和实验3说明浓硝酸显黄色与硝酸根离子无关,结合实验1和实验2的实验现象可知,浓硝酸显黄色是溶液中 $ {\rm {\mathrm{H}}^{+}} $ 与 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 共同作用的结果。
(2) ① 步骤ⅰ中按图连接好装置后,进行的第一步操作是检查装置气密性。
② 仪器 $ \mathrm{a} $ 中无水氯化钙的作用为干燥 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ,若无此装置,将会发生副反应: $ {\rm 2{\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}4\mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}+{\mathrm{O}}_{2}↑} $ 。
③ 因为过氧化钠能与 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ 、 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 反应,因此需防止空气中的 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ 、 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 进入仪器 $ \mathrm{b} $ 中。
④ $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 具有氧化性, $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 中 $ {\rm \mathrm{N}} $ 为 $ +4 $ 价,可升至 $ +5 $ 价,即 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 可将 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 氧化生成 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}} $ ,反应的化学方程式为 $ {\rm 2{\mathrm{N}\mathrm{O}}_{2}+{\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}\xlongequal{}2{\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}} $ 。
9.氨基钠 $ {\rm ({\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{H}}_{2})} $ 是制取靛青染料等工业品的原料,某研究性学习小组设计如图实验装置用氨气和金属钠制取氨基钠(部分夹持装置已省略)。
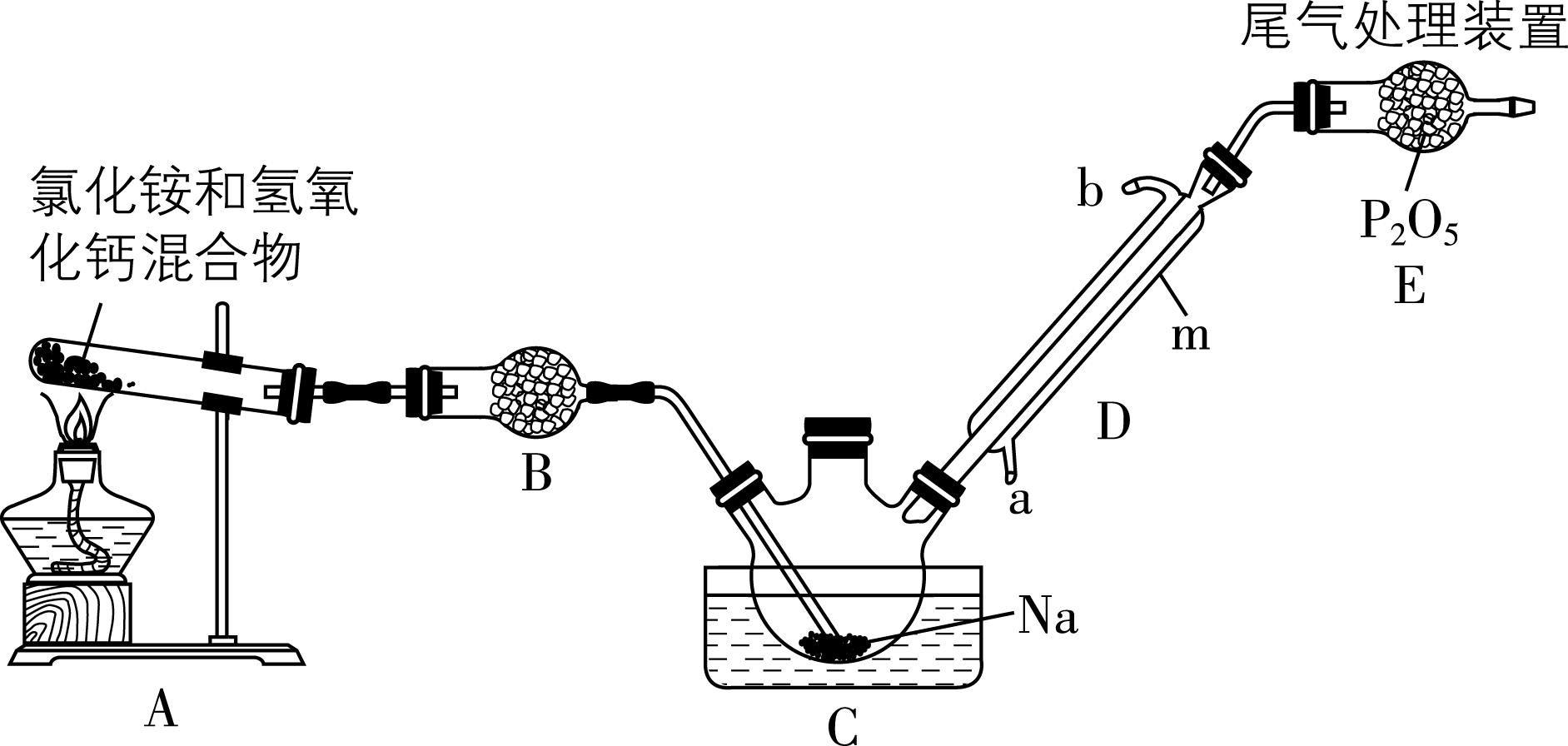
已知:①常温下氨基钠为白色晶体,熔点 $ 210℃ $ ,沸点 $ 400℃ $ ,遇水蒸气剧烈反应生成 $ {\rm \mathrm{N}\mathrm{a}\mathrm{O}\mathrm{H}} $ 和 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 。
②金属钠熔点 $ 97.8℃ $ ,沸点 $ 883℃ $ 。
回答下列问题:
(1) 仪器 $ \mathrm{m} $ 的名称为 ; $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{H}}_{2}} $ 为 (填“离子”或“共价”)化合物。
(2) 装置B中盛装的试剂名称为 。
(3) 装置C中发生反应的化学方程式为 。
(4) 装置 $ {\rm \mathrm{E}} $ 中的 $ {\rm {\mathrm{P}}_{2}{\mathrm{O}}_{5}} $ 可以防止空气中的水分进入装置C中,还可以 。
(5) 上述方法制得的氨基钠中往往混有杂质钠。称取 $ 0.15\mathrm{g} $ 实验制得的样品溶于足量去离子水中,加热,使 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 完全蒸出,并用 $ {\rm {\mathrm{H}}_{3}{\mathrm{B}\mathrm{O}}_{3}} $ 溶液充分吸收 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ ;再向吸收液中逐滴加入 $ {\rm 0.25\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 的硫酸,恰好反应时,消耗硫酸的体积为 $ {\rm 4.7\mathrm{m}\mathrm{L}} $ 。已知 $ {\rm 2{\mathrm{N}\mathrm{H}}_{3}+4{\mathrm{H}}_{3}{\mathrm{B}\mathrm{O}}_{3}\xlongequal{}({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{B}}_{4}{\mathrm{O}}_{7}+5{\mathrm{H}}_{2}\mathrm{O}} $ 、 $ {\rm ({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{B}}_{4}{\mathrm{O}}_{7}+{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}+5{\mathrm{H}}_{2}\mathrm{O}\xlongequal{}({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{S}\mathrm{O}}_{4}+4{\mathrm{H}}_{3}{\mathrm{B}\mathrm{O}}_{3}} $ ,该样品中氨基钠的质量分数为 $ \% $ 。
答案:(1) 直形冷凝管;离子
(2) 碱石灰
(3) $ {\rm 2{\mathrm{N}\mathrm{H}}_{3}+2\mathrm{N}\mathrm{a}\xlongequal{△}2{\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{H}}_{2}+{\mathrm{H}}_{2}} $
(4) 吸收多余的氨气
(5) 61.1
解析:(1) 仪器 $ \mathrm{m} $ 的名称为直形冷凝管。 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{H}}_{2}} $ 是由钠离子和 $ {\rm {\mathrm{N}\mathrm{H}}_{2}^{-}} $ 形成的离子化合物。
(2) 水蒸气不能进入装置 $ {\rm \mathrm{C}} $ ,需要对氨气进行干燥,应选择碱石灰作干燥剂。
(3) 装置 $ {\rm \mathrm{C}} $ 中钠和氨气发生反应生成氨基钠,结合质量守恒,还生成氢气,化学方程式为 $ {\rm 2{\mathrm{N}\mathrm{H}}_{3}+2\mathrm{N}\mathrm{a}\xlongequal{△}2{\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{H}}_{2}+{\mathrm{H}}_{2}} $ 。
(4) 装置 $ {\rm \mathrm{E}} $ 中的 $ {\rm {\mathrm{P}}_{2}{\mathrm{O}}_{5}} $ 可以防止空气中的水分进入装置 $ {\rm \mathrm{C}} $ 中,还可以吸收多余的氨气。
(5) 结合元素守恒及题干反应可知, $ {\rm 2{\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{H}}_{2}\sim 2{\mathrm{N}\mathrm{H}}_{3}\sim ({\mathrm{N}\mathrm{H}}_{4})_{2}{\mathrm{B}}_{4}{\mathrm{O}}_{7}\sim {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ ,则样品中氨基钠的质量分数为 $ {\rm \dfrac{0.25\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}×4.7×{10}^{-3}\mathrm{L}×2×39\mathrm{g}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}}{0.15\mathrm{g}}×100\%=61.1\%} $ 。










