课时1 化学反应与热能
一、刷基础
1.下列变化中,属于放热反应的是( )
①液氮汽化 ②氢氧化钠固体溶于水 ③氢氧化钠溶液与盐酸反应 $ {\rm ④{\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 分解制 $ {\rm {\mathrm{O}}_{2}} $ $ {\rm ⑤\mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}} $ 晶体与 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 晶体混合 ⑥氢气在氧气中燃烧 $ {\rm ⑦{\mathrm{C}\mathrm{O}}_{2}+\mathrm{C}\xlongequal{高温}2\mathrm{C}\mathrm{O}} $ ⑧生石灰和水反应生成熟石灰 ⑨钠块投入水中 ⑩锌与盐酸反应
A. ①②③⑥⑦⑧⑨
B. ①②⑥⑧⑨⑩
C. ③⑥⑧⑨⑩
D. ③④⑤⑧⑨⑩
答案:C
解析:液氮汽化是物理变化不是化学变化,①错误;氢氧化钠固体溶于水是物理变化不是化学变化,②错误;氢氧化钠溶液和盐酸的反应为酸碱中和反应,属于放热反应,③正确;高锰酸钾分解制取氧气,属于吸热反应,④错误; $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}} $ 晶体和氯化铵晶体的反应为吸热反应,⑤错误;氢气在氧气中燃烧放热,⑥正确;二氧化碳与 $ {\rm \mathrm{C}} $ 在高温下反应生成一氧化碳,属于吸热反应,⑦错误;生石灰与水反应生成熟石灰,属于放热反应,⑧正确;钠块投入水中,钠与水反应生成氢氧化钠和氢气,属于放热反应,⑨正确;锌与盐酸的反应为放热反应,⑩正确;故属于放热反应的是③⑥⑧⑨⑩,选 $ {\rm \mathrm{C}} $ 。
2. 下列反应的能量变化规律与图示相符的是( )
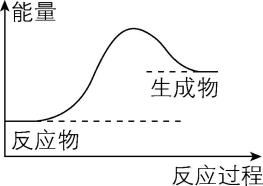
①氯化铵分解 ②过氧化氢分解 ③盐酸与碳酸氢钠固体反应 ④氮气的高温氧化 ⑤氢气在氯气中燃烧 ⑥硫酸和氢氧化钡溶液反应
①②⑤
①③④
③④⑤
②④⑥
答案:B
解析:如图所示,反应物的总能量低于生成物的总能量,则反应为吸热反应。①氯化铵分解为吸热反应,符合题意;②过氧化氢分解为放热反应,不符合题意;③盐酸与碳酸氢钠的反应为吸热反应,符合题意;④氮气的高温氧化为吸热反应,符合题意;⑤氢气在氯气中燃烧,属于放热反应,不符合题意;⑥硫酸和氢氧化钡溶液的反应为放热反应,不符合题意。 $ {\rm \mathrm{B}} $ 正确。
3.用如下两种方法探究 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水反应的热效应,实验时发现Ⅱ烧杯中导管口有气泡冒出。
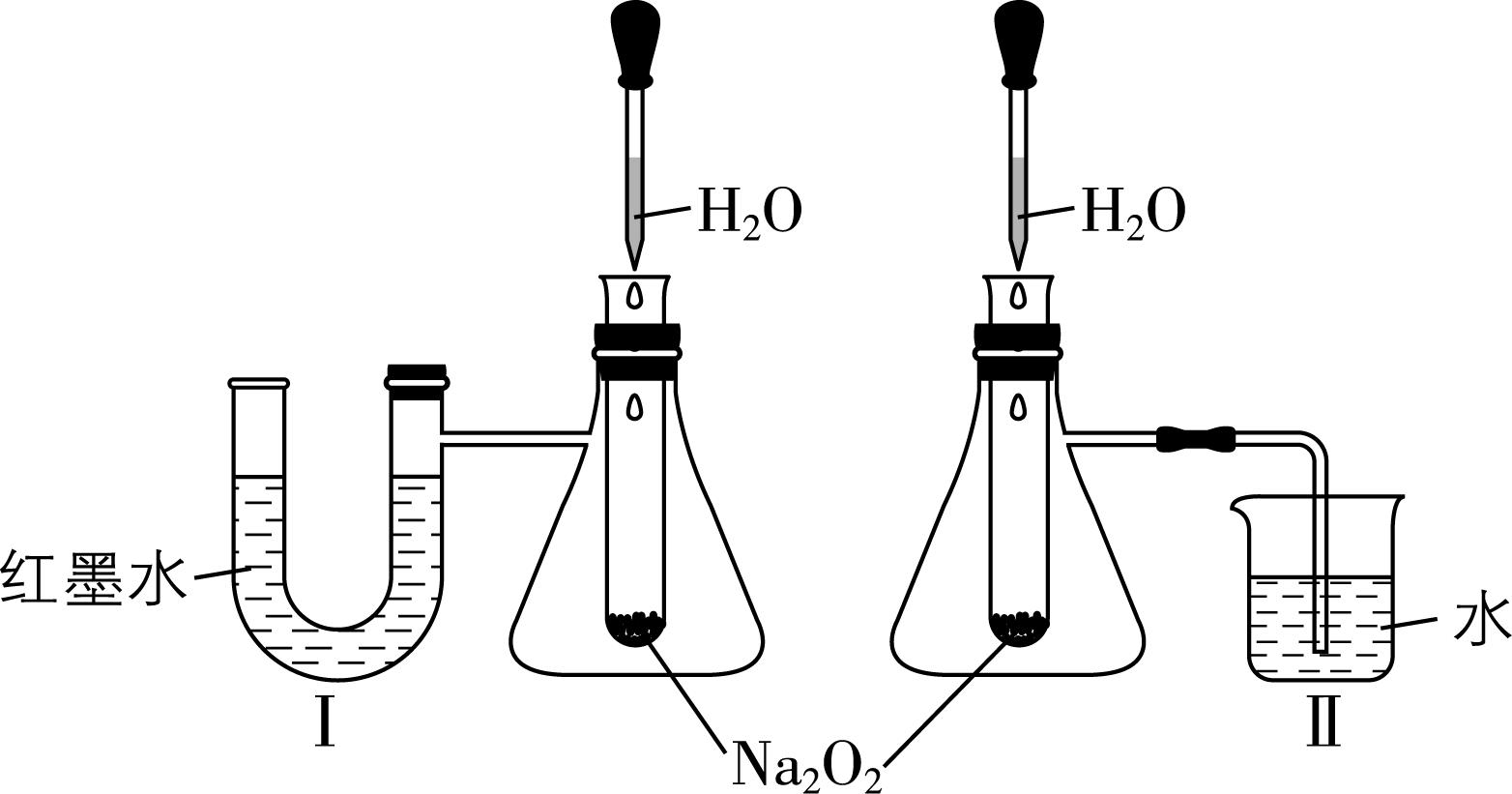
下列说法错误的是( )
A. Ⅱ中气泡是锥形瓶内气压增大造成的
B. Ⅱ中气泡是 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水反应生成氧气造成的
C. 若将温度计伸入试管,会观察到温度示数升高
D. 预测实验时Ⅰ中 $ {\rm \mathrm{U}} $ 形管右侧液面下降
答案:B
解析:装置Ⅰ可通过 $ {\rm \mathrm{U}} $ 形管中红墨水液面的变化判断 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水反应的热效应,装置Ⅱ可通过烧杯中是否产生气泡判断 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水反应的热效应。Ⅱ中产生气泡是因为 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水反应放热,使锥形瓶内气压增大, $ {\rm \mathrm{A}} $ 正确; $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水反应生成的氧气无法进入锥形瓶, $ {\rm \mathrm{B}} $ 错误; $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水的反应为放热反应,若将温度计伸入试管,会观察到温度示数升高, $ {\rm \mathrm{C}} $ 正确; $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{O}}_{2}} $ 与水的反应为放热反应,使锥形瓶内压强增大,挤压 $ {\rm \mathrm{U}} $ 形管中的液体,故实验时Ⅰ中 $ {\rm \mathrm{U}} $ 形管右侧液面下降,左侧升高, $ {\rm \mathrm{D}} $ 正确。
4.下列说法正确的是( )
A. 化学键的断裂和形成是化学反应能量变化的主要原因
B. 伴有能量变化的物质变化过程都是化学变化
C. 在一个确定的化学反应中,反应物的总能量与生成物的总能量一定相同
D. 在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量
答案:A
解析:化学反应过程中,反应物的化学键断裂要吸收能量,而生成物的化学键形成要放出能量,所以化学键的断裂和形成是化学反应能量变化的主要原因, $ {\rm \mathrm{A}} $ 正确;伴有能量变化的物质变化过程不一定是化学变化,如液态水吸热形成水蒸气的过程属于物理变化, $ {\rm \mathrm{B}} $ 错误;在一个确定的化学反应中,必定伴随着能量的变化,即反应物的总能量与生成物的总能量不可能相同, $ {\rm \mathrm{C}} $ 错误;在一个确定的化学反应中,放热反应的反应物总能量高于生成物总能量,吸热反应的反应物总能量低于生成物总能量, $ {\rm \mathrm{D}} $ 错误。
5.氮氧化物是造成光化学烟雾的主要气体,含 $ {\rm \mathrm{N}\mathrm{O}} $ 的烟气需要经过处理后才能排放。科学家研制了使用氢气还原 $ {\rm \mathrm{N}\mathrm{O}} $ 的方法: $ {\rm 2\mathrm{N}\mathrm{O}(\mathrm{g})+2{\mathrm{H}}_{2}(\mathrm{g})⇌{\mathrm{N}}_{2}(\mathrm{g})+2{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})} $ 。已知: $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}} $ 完全反应时放热 $ {\rm 333.0\mathrm{k}\mathrm{J}} $ ,有关化学键键能(断开 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 化学键所吸收的能量或者形成 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 化学键所释放的能量)的数据如表所示。
化学键 | $ {\rm \mathrm{H}—\mathrm{H}} $ | $ {\rm \mathrm{N}\mathrm{O}} $ 中的化学键 | $ {\rm \mathrm{H}—\mathrm{O}} $ | $ {\rm \mathrm{N}\equiv \mathrm{N}} $ |
键能/ $ {\rm (\mathrm{k}\mathrm{J}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1})} $ | 436 | $ x $ | 463 | 946 |
下列说法正确的是( )
A. 将 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}} $ 和 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}} $ 投入容器中发生该反应,可放热 $ {\rm 666.0\mathrm{k}\mathrm{J}} $
B. 相同状态的 $ {\rm \mathrm{N}\mathrm{O}} $ 比 $ {\rm {\mathrm{N}}_{2}} $ 稳定
C. $ x $ 的数值为630
D. 当反应生成的水为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}\mathrm{O}(\mathrm{l})} $ 时放热小于 $ {\rm 333.0\mathrm{k}\mathrm{J}} $
答案:C
解析:该反应为可逆反应,投入的 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}} $ 无法完全消耗,实际放热小于 $ {\rm 666.0\mathrm{k}\mathrm{J}} $ , $ {\rm \mathrm{A}} $ 错误;根据 $ {\rm \mathrm{\Delta }H} $ 计算:断键吸收的总能量 $ {\rm (2x\mathrm{k}\mathrm{J}+2×436\mathrm{k}\mathrm{J})-} $ 成键放出的总能量 $ {\rm (946\mathrm{k}\mathrm{J}+4×463\mathrm{k}\mathrm{J})=-666\mathrm{k}\mathrm{J}} $ ,解得 $ x=630 $ , $ {\rm \mathrm{N}\mathrm{N}} $ 键能 $ {\rm (946\mathrm{k}\mathrm{J}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1})} $ 远高于 $ {\rm \mathrm{N}\mathrm{O}} $ 中化学键的键能 $ {\rm (630\mathrm{k}\mathrm{J}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1})} $ ,键能越大越稳定,所以 $ {\rm {\mathrm{N}}_{2}} $ 更稳定, $ {\rm \mathrm{B}} $ 错误、 $ {\rm \mathrm{C}} $ 正确; $ {\rm {\mathrm{H}}_{2}\mathrm{O}(\mathrm{l})} $ 比 $ {\rm {\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})} $ 能量更低,生成液态水时放热更多,应大于 $ {\rm 333.0\mathrm{k}\mathrm{J}} $ , $ {\rm \mathrm{D}} $ 错误。
6.下列图示与对应的叙述相符的是( )
选项 | A | B |
图示 | 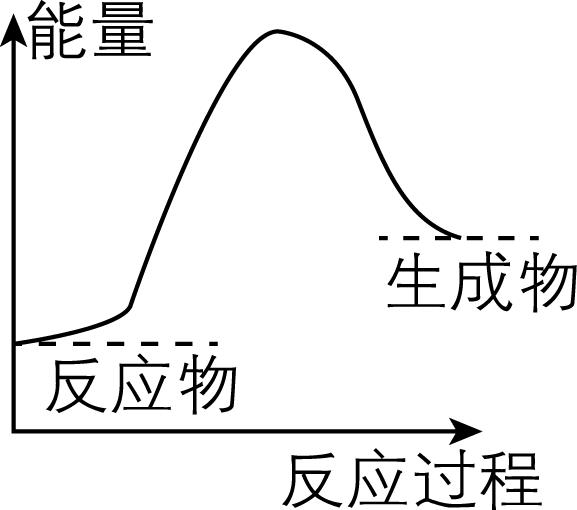
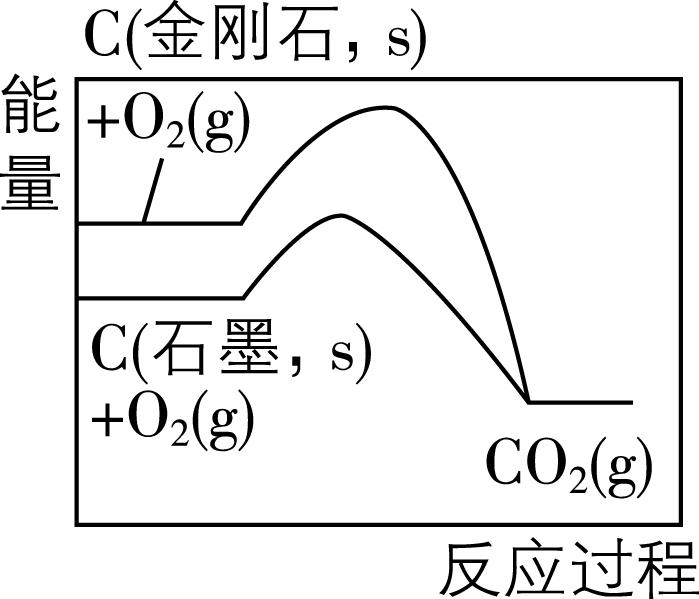
| 
|
叙述 | 该图可表示锌和稀硫酸反应过程中的能量变化 | 由图可知,金刚石比石墨稳定 |
选项 | C | D |
图示 | 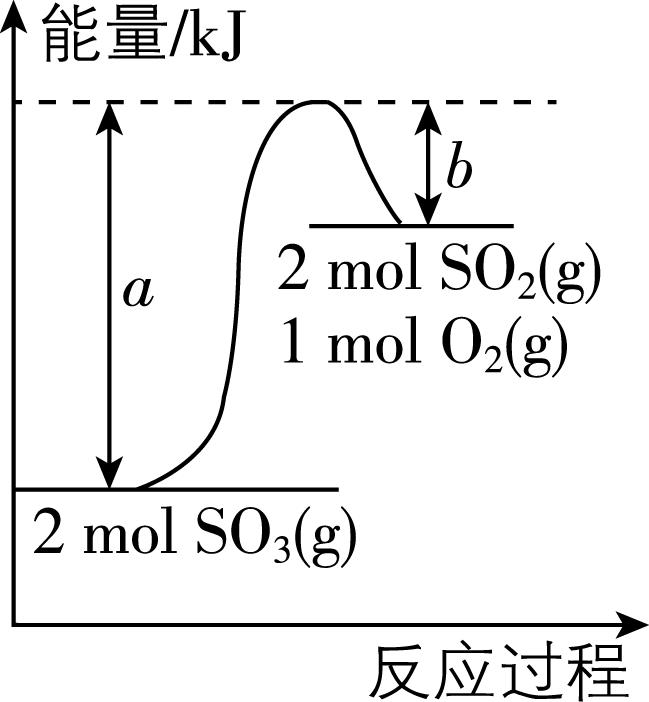
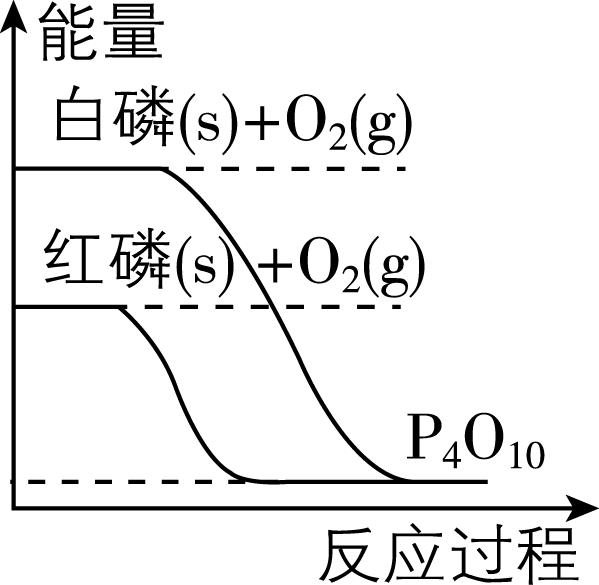
| 
|
叙述 | 由图可知, $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{S}\mathrm{O}}_{3}(\mathrm{g})} $ 转化为 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{S}\mathrm{O}}_{2}(\mathrm{g})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}(\mathrm{g})} $ 吸收 $ {\rm (a-b)\mathrm{k}\mathrm{J}} $ 能量 | 由图可知,白磷转化为红磷是吸热反应 |
解析:题图中反应物的总能量小于生成物的总能量,为吸热反应,而锌和稀硫酸的反应为放热反应,与图示不符, $ {\rm \mathrm{A}} $ 错误;由题图可知,石墨的能量低于金刚石的能量,物质具有的能量越低越稳定,则石墨比金刚石更稳定, $ {\rm \mathrm{B}} $ 错误;由题图可知, $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{S}\mathrm{O}}_{3}(\mathrm{g})} $ 转化为 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{S}\mathrm{O}}_{2}(\mathrm{g})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}(\mathrm{g})} $ 过程中吸收 $ {\rm a\mathrm{k}\mathrm{J}} $ 能量,放出 $ {\rm b\mathrm{k}\mathrm{J}} $ 能量,则总反应吸收 $ {\rm (a-b)\mathrm{k}\mathrm{J}} $ 能量, $ {\rm \mathrm{C}} $ 正确;由题图可知,白磷的能量高于红磷的能量,因此白磷转化为红磷是放热反应, $ {\rm \mathrm{D}} $ 错误。
7.某反应由两步反应构成,其能量变化如图所示,下列叙述正确的是( )
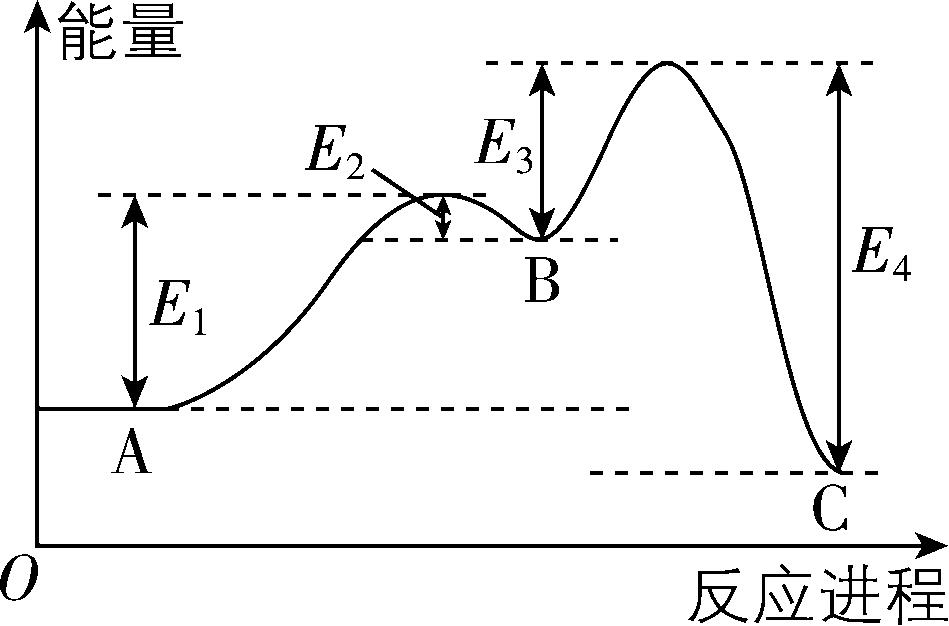
A. 两步反应中反应物的总能量均大于生成物的总能量
B. A、B、C中C最稳定
C. $ {\rm \mathrm{A}\to \mathrm{B}} $ 一定需要加热
D. $ {\rm \mathrm{A}\to \mathrm{C}} $ 为吸热反应
答案:B
解析:第一步,反应物的总能量小于生成物的总能量;第二步,反应物的总能量大于生成物的总能量, $ {\rm \mathrm{A}} $ 错误。能量越低的物质越稳定, $ {\rm \mathrm{A}} $ 、 $ {\rm \mathrm{B}} $ 、 $ {\rm \mathrm{C}} $ 中 $ {\rm \mathrm{C}} $ 的能量最低,故最稳定, $ {\rm \mathrm{B}} $ 正确。 $ {\rm \mathrm{A}\to \mathrm{B}} $ 为吸热反应,但不一定需要加热, $ {\rm \mathrm{C}} $ 错误。 $ {\rm \mathrm{A}\to \mathrm{C}} $ 为放热反应, $ {\rm \mathrm{D}} $ 错误。
8.计算机模拟催化剂表面水煤气产氢反应 $ {\rm [\mathrm{C}\mathrm{O}(\mathrm{g})+{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})\xlongequal{}{\mathrm{C}\mathrm{O}}_{2}(\mathrm{g})+{\mathrm{H}}_{2}(\mathrm{g})]} $ 过程中能量的变化如图所示。下列说法错误的是( )
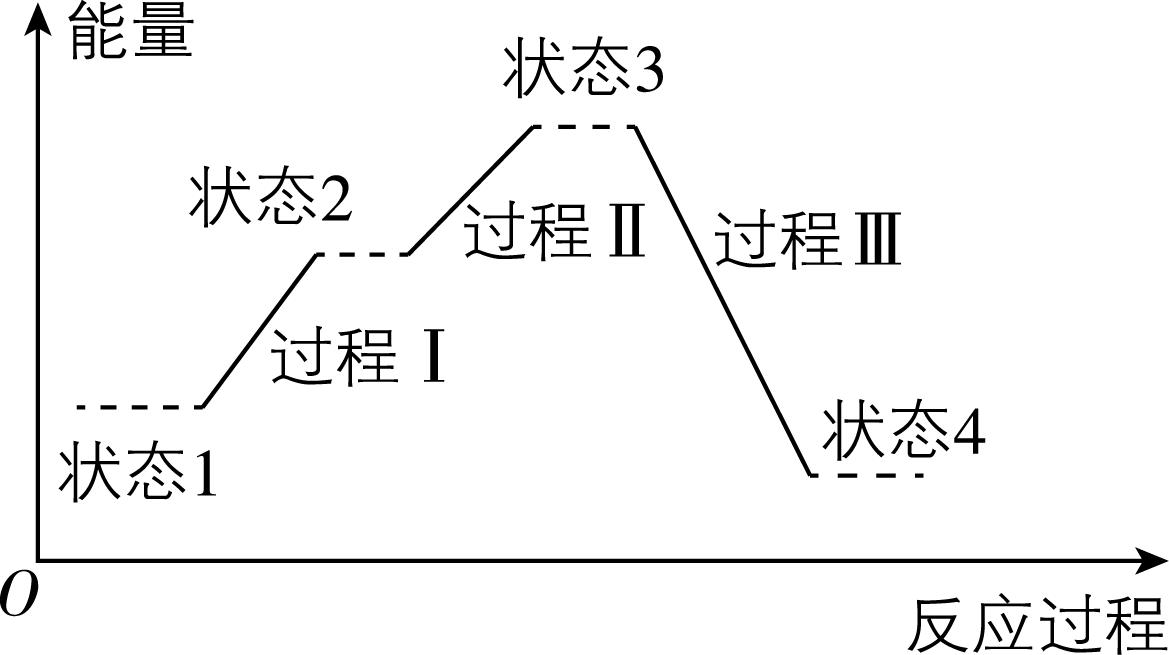
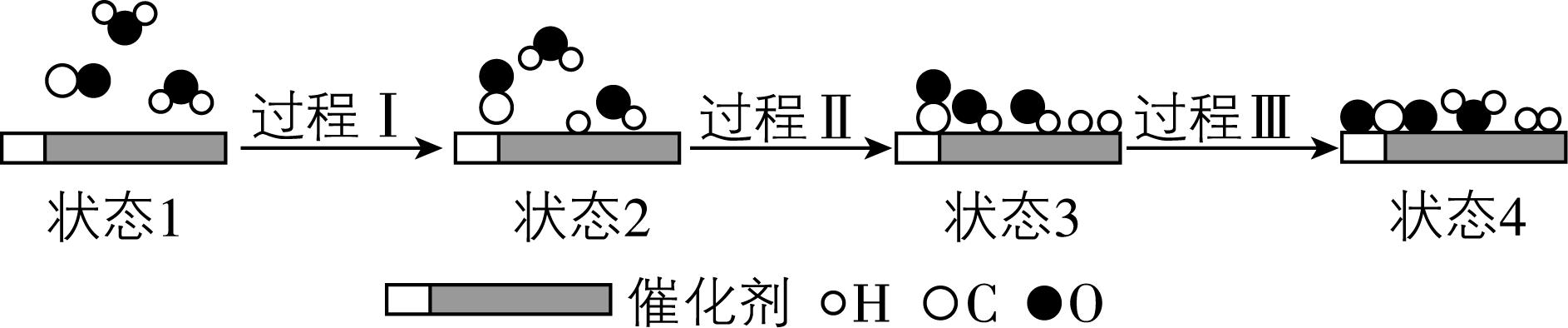
A. 该反应为放热反应
B. 过程Ⅰ、Ⅱ均表示 $ {\rm {\mathrm{H}}_{2}\mathrm{O}} $ 断键的吸收能量过程
C. 过程Ⅲ既有极性共价键断裂,又有极性共价键形成
D. 由图可知 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 比 $ {\rm \mathrm{C}\mathrm{O}} $ 稳定
答案:D
解析:生成物总能量低于反应物总能量,则总反应为放热反应, $ {\rm \mathrm{A}} $ 正确;根据图示,过程Ⅰ、Ⅱ均为 $ {\rm \mathrm{O}—\mathrm{H}} $ 断裂,故均需要吸收能量, $ {\rm \mathrm{B}} $ 正确;过程Ⅲ既有 $ {\rm \mathrm{O}—\mathrm{H}} $ 断裂,又有 $ {\rm \mathrm{C}\xlongequal{}\mathrm{O}} $ 、 $ {\rm \mathrm{O}—\mathrm{H}} $ 形成, $ {\rm \mathrm{C}} $ 正确;根据题图可知 $ {\rm \mathrm{C}\mathrm{O}(\mathrm{g})+{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})} $ 总能量大于 $ {\rm {\mathrm{C}\mathrm{O}}_{2}(\mathrm{g})+{\mathrm{H}}_{2}(\mathrm{g})} $ 总能量,不能判断 $ {\rm {\mathrm{C}\mathrm{O}}_{2}(\mathrm{g})} $ 和 $ {\rm \mathrm{C}\mathrm{O}(\mathrm{g})} $ 的能量大小,进而无法判断二者稳定性强弱, $ {\rm \mathrm{D}} $ 错误。
9.现代社会的一切活动都离不开能量,化学反应在发生物质变化的同时伴随能量的变化。回答下列问题:
(1) 由图甲的能量转化关系可知生成 $ {\rm 16\mathrm{g}{\mathrm{C}\mathrm{H}}_{3}\mathrm{O}\mathrm{H}(\mathrm{l})} $ 需要 (填“吸收”或“放出”) $ {\rm \mathrm{k}\mathrm{J}} $ 能量。
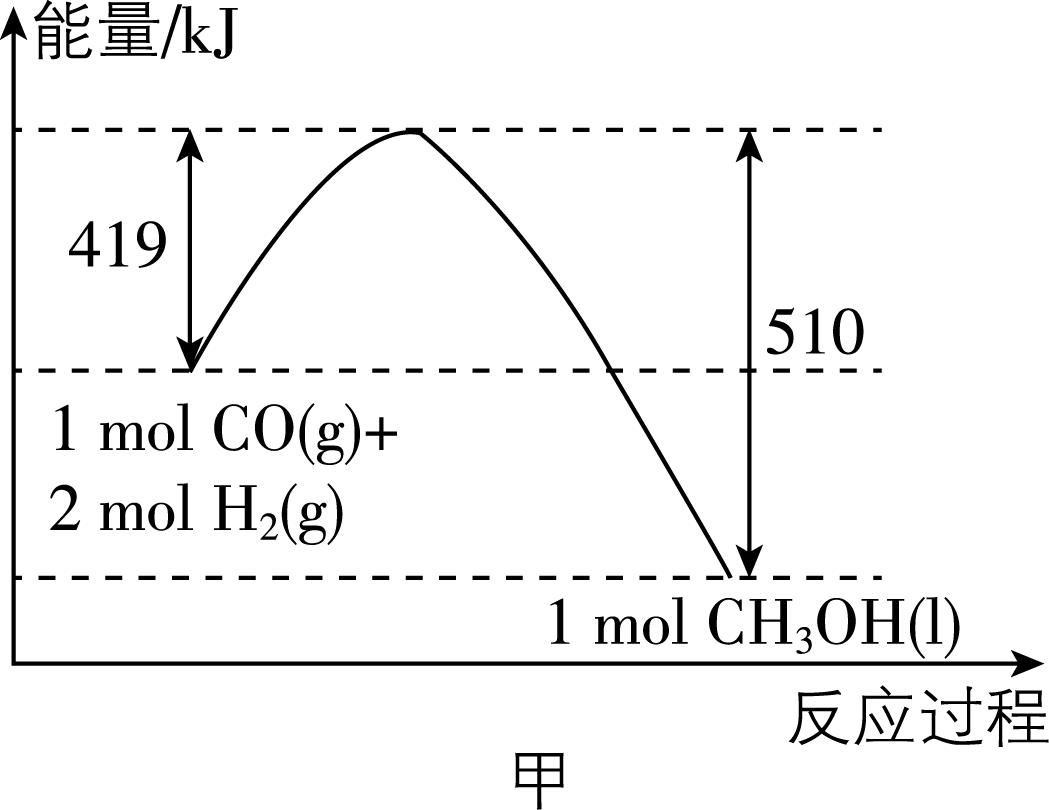
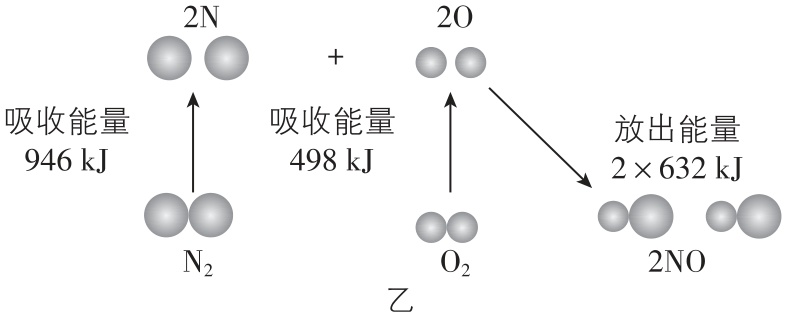
(2) 图乙为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}(\mathrm{g})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}(\mathrm{g})} $ 充分反应生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}(\mathrm{g})} $ 的能量变化图。若生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}(\mathrm{g})} $ ,需要吸收 $ {\rm \mathrm{k}\mathrm{J}} $ 能量。
(3) 某实验小组为了探究化学能与热能的转化,设计了如图丙所示的三套实验装置:
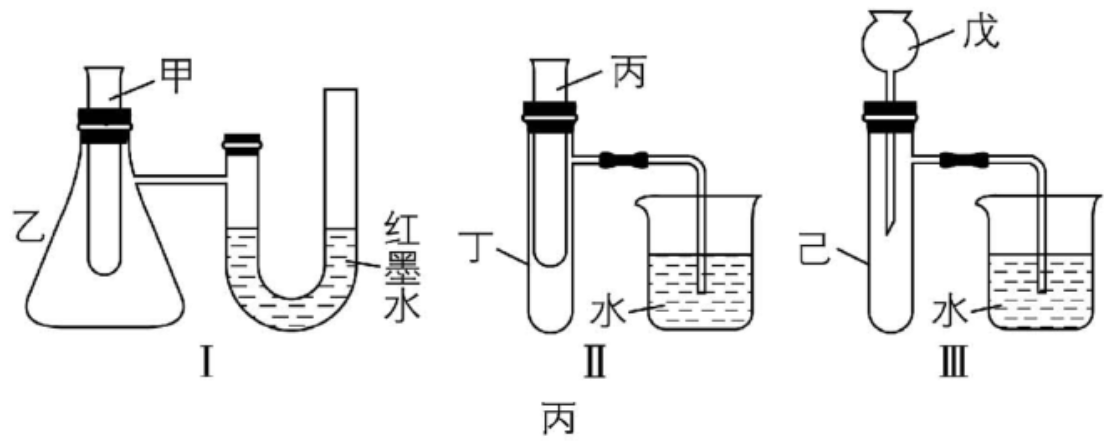
① 某同学选用装置Ⅰ进行实验(实验前 $ {\rm \mathrm{U}} $ 形管里液面左右相平),在甲试管中加入了适量 $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}} $ 溶液与盐酸, $ {\rm \mathrm{U}} $ 形管中可观察到的现象是 。
② 上述3个装置中,能探究“锌与稀硫酸的反应是吸热反应还是放热反应”的装置是 (填序号)。
答案:(1) 放出;45.5
(2) 180
(3) ① 左端液面降低,右端液面升高(或右端液面高于左端液面)
② Ⅰ、Ⅱ
解析:(1) 由图甲知,生成物的总能量低于反应物的总能量,因此该反应是放热反应;生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{C}\mathrm{H}}_{3}\mathrm{O}\mathrm{H}(\mathrm{l})} $ 放出 $ {\rm (510-419)\mathrm{k}\mathrm{J}=91\mathrm{k}\mathrm{J}} $ 能量,则生成 $ 16\mathrm{g} $ 即 $ {\rm 0.5\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{C}\mathrm{H}}_{3}\mathrm{O}\mathrm{H}(\mathrm{l})} $ 放出 $ {\rm 45.5\mathrm{k}\mathrm{J}} $ 能量。
(2) 断裂 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 氮气中化学键需要吸收 $ {\rm 946\mathrm{k}\mathrm{J}} $ 能量,断裂 $ 1\mathrm{m}\mathrm{o}\mathrm{l} $ 氧气中化学键需要吸收 $ {\rm 498\mathrm{k}\mathrm{J}} $ 能量,形成 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 一氧化氮中化学键需放出 $ {\rm 2×632\mathrm{k}\mathrm{J}=1264\mathrm{k}\mathrm{J}} $ 能量,故生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}(\mathrm{g})} $ 时吸收的能量为 $ {\rm 946\mathrm{k}\mathrm{J}+498\mathrm{k}\mathrm{J}-1264\mathrm{k}\mathrm{J}=180\mathrm{k}\mathrm{J}} $ 。
(3) ① 甲试管中加入适量 $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}} $ 溶液与盐酸,二者发生中和反应,中和反应属于放热反应,则乙中气体受热膨胀, $ {\rm \mathrm{U}} $ 形管中可观察到左端液面降低,右端液面升高。
② 题述3个装置中,装置Ⅰ可通过 $ {\rm \mathrm{U}} $ 形管中红墨水液面的变化,判断锌与稀硫酸的反应是吸热反应还是放热反应,装置Ⅱ可通过烧杯中导管口是否产生气泡判断锌与稀硫酸的反应是吸热反应还是放热反应,装置Ⅲ是将锌与稀硫酸反应产生的气体 $ {\rm ({\mathrm{H}}_{2})} $ 通入水中,则右侧烧杯中导管口一定有气泡冒出,不能证明该反应是放热反应还是吸热反应,则满足题意的装置是Ⅰ、Ⅱ。
二、刷提升
1.可以用图示法分析化学反应中的能量变化,下列说法不正确的是( )
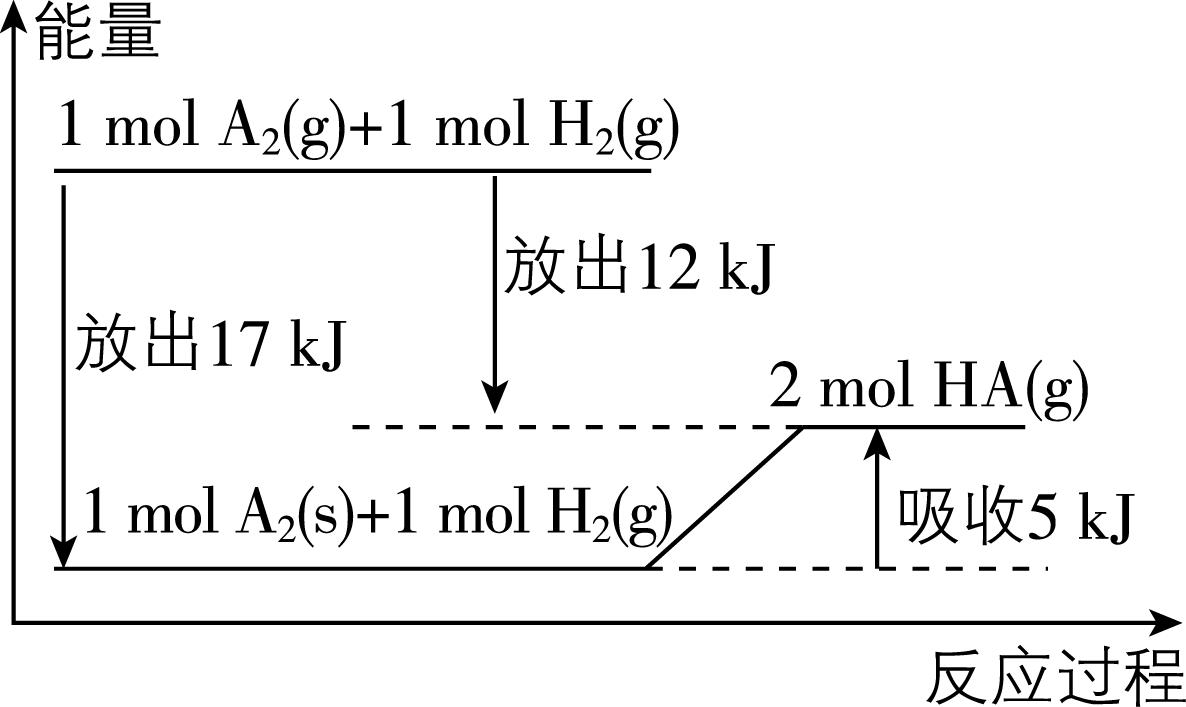
A. $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 与过量 $ {\rm {\mathrm{H}}_{2}(\mathrm{g})} $ 化合生成 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{g})} $ 时,需要吸收 $ {\rm 10\mathrm{k}\mathrm{J}} $ 的能量
B. $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 变为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{g})} $ 时,需要吸收 $ {\rm 17\mathrm{k}\mathrm{J}} $ 的能量
C. $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{g})} $ 分解生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{g})} $ 与 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ 时,需要吸收 $ {\rm 12\mathrm{k}\mathrm{J}} $ 的能量
D. $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{l})} $ 分解生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 与 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ 时,需要放出 $ {\rm 5\mathrm{k}\mathrm{J}} $ 的能量
答案:D
解析:由题图可知, $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 与 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ 反应生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{g})} $ ,吸收 $ {\rm 5\mathrm{k}\mathrm{J}} $ 的能量,则 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 与过量 $ {\rm {\mathrm{H}}_{2}(\mathrm{g})} $ 反应生成 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{g})} $ ,吸收 $ {\rm 10\mathrm{k}\mathrm{J}} $ 的能量, $ {\rm \mathrm{A}} $ 正确;由题图可知, $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{g})} $ 转化为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 放出 $ {\rm 17\mathrm{k}\mathrm{J}} $ 能量,则 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 转化为 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{g})} $ 需要吸收 $ {\rm 17\mathrm{k}\mathrm{J}} $ 的能量, $ {\rm \mathrm{B}} $ 正确;由题图可知, $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{g})} $ 与 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ 反应生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{g})} $ ,放出 $ {\rm 12\mathrm{k}\mathrm{J}} $ 能量,则 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{g})} $ 分解生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{g})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ 时,吸收 $ {\rm 12\mathrm{k}\mathrm{J}} $ 的能量, $ {\rm \mathrm{C}} $ 正确;由题图可知, $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{g})} $ 分解生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ ,放出 $ {\rm 5\mathrm{k}\mathrm{J}} $ 能量, $ {\rm \mathrm{H}\mathrm{A}(\mathrm{l})} $ 转化为 $ {\rm \mathrm{H}\mathrm{A}(\mathrm{g})} $ 需要吸热,则 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{A}(\mathrm{l})} $ 分解生成 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{A}}_{2}(\mathrm{s})} $ 和 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}(\mathrm{g})} $ ,放出的能量小于 $ {\rm 5\mathrm{k}\mathrm{J}} $ , $ {\rm \mathrm{D}} $ 错误。
2.如图是金属镁和卤素单质 $ {\rm ({\mathrm{X}}_{2})} $ 反应的能量变化示意图,下列说法正确的是( )
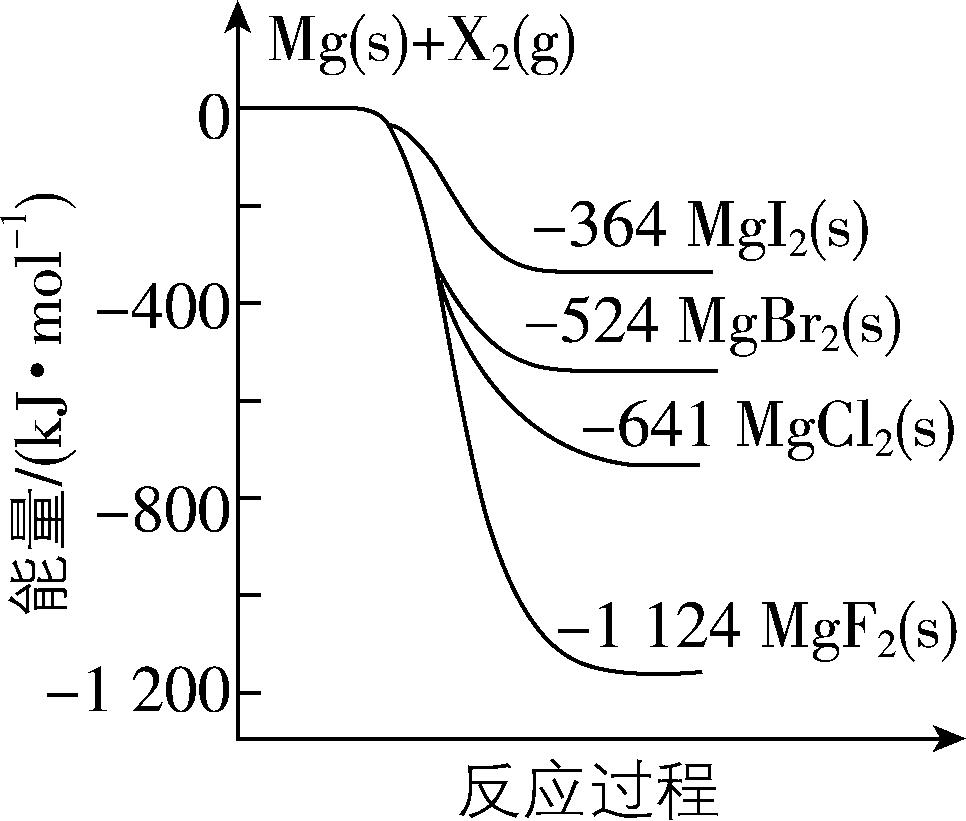
A. 由 $ {\rm {\mathrm{M}\mathrm{g}\mathrm{C}\mathrm{l}}_{2}} $ 制取 $ {\rm \mathrm{M}\mathrm{g}} $ 是放热过程
B. $ {\rm 22.4\mathrm{L}{\mathrm{F}}_{2}(\mathrm{g})} $ 与足量的 $ {\rm \mathrm{M}\mathrm{g}} $ 充分反应,放热 $ {\rm 1124\mathrm{k}\mathrm{J}} $
C. $ {\rm \mathrm{M}\mathrm{g}(\mathrm{s})} $ 和卤素单质 $ {\rm {\mathrm{X}}_{2}(\mathrm{g})} $ 的反应都是放热反应
D. 此温度下四种卤化镁中 $ {\rm {\mathrm{M}\mathrm{g}\mathrm{I}}_{2}(\mathrm{s})} $ 所含化学键的键能最大
答案:C
解析:由题图可知,氯化镁的能量低于镁和氯气的能量之和,则由氯化镁制取镁的过程是吸热过程, $ {\rm \mathrm{A}} $ 错误;未指明是否为标准状况,反应放出的热量不能确定, $ {\rm \mathrm{B}} $ 错误;由题图可知,金属镁和卤素单质的能量之和大于生成物的能量,故镁与卤素单质 $ {\rm {\mathrm{X}}_{2}(\mathrm{g})} $ 的反应都是放热反应, $ {\rm \mathrm{C}} $ 正确;物质的键能越大,能量越低,四种卤化镁中 $ {\rm {\mathrm{M}\mathrm{g}\mathrm{F}}_{2}(\mathrm{s})} $ 的能量最低,则 $ {\rm {\mathrm{M}\mathrm{g}\mathrm{F}}_{2}(\mathrm{s})} $ 所含化学键的键能最大, $ {\rm \mathrm{D}} $ 错误。
3.化学反应 $ {\rm {\mathrm{A}}_{2}(\mathrm{g})+{\mathrm{B}}_{2}(\mathrm{g})\xlongequal{}2\mathrm{A}\mathrm{B}(\mathrm{g})} $ 的能量变化如图所示。下列叙述错误的是( )
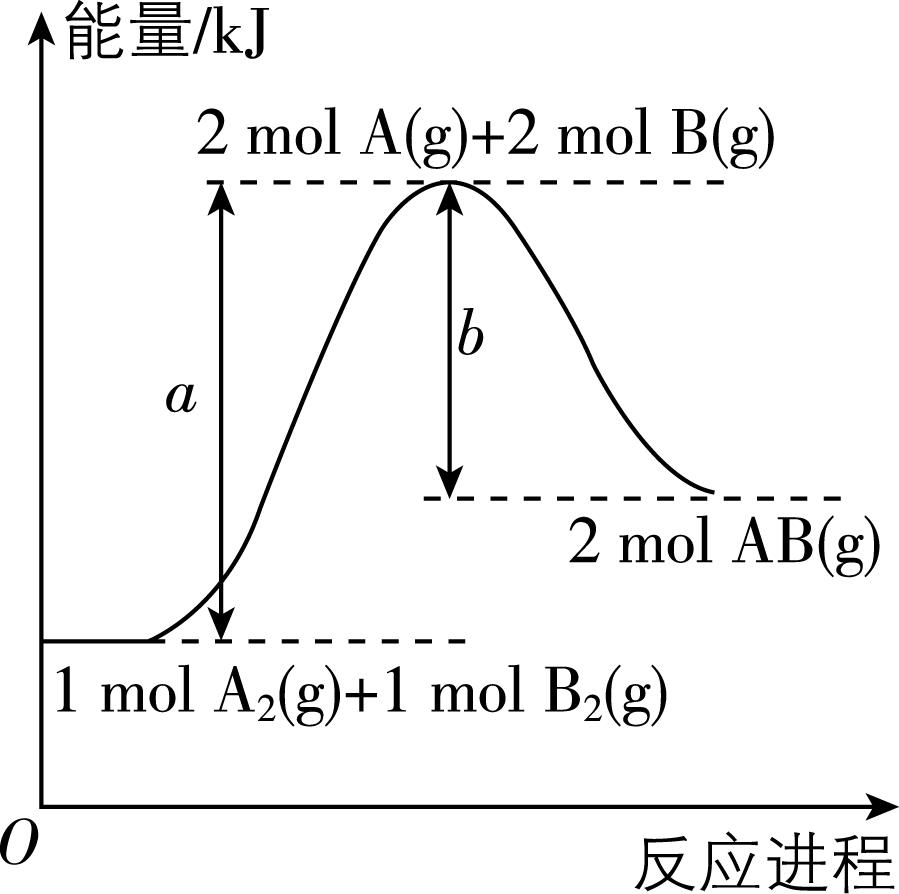
A. 该反应一定需要在加热条件下才能进行
B. 反应物的总能量比生成物的总能量低
C. 该反应每生成 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{A}\mathrm{B}} $ 气体分子吸收 $ {\rm 2(a-b)\mathrm{k}\mathrm{J}} $ 能量
D. 破坏反应物中化学键所需的能量高于形成生成物中化学键释放的能量
答案:A
解析:反应吸、放热与反应条件无关,该反应不一定需要在加热条件下才能进行, $ {\rm \mathrm{A}} $ 错误;根据图示,反应物的总能量比生成物的总能量低, $ {\rm \mathrm{B}} $ 正确;根据图示,生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{A}\mathrm{B}} $ 气体分子吸收 $ {\rm (a-b)\mathrm{k}\mathrm{J}} $ 能量,则该反应每生成 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{A}\mathrm{B}} $ 气体分子吸收 $ {\rm 2(a-b)\mathrm{k}\mathrm{J}} $ 能量, $ {\rm \mathrm{C}} $ 正确;根据图示,生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{A}\mathrm{B}(\mathrm{g})} $ ,破坏反应物中化学键所需的能量为 $ {\rm a\mathrm{k}\mathrm{J}} $ ,形成生成物中化学键,释放 $ {\rm b\mathrm{k}\mathrm{J}} $ 能量,破坏反应物中化学键所需的能量高于形成生成物中化学键释放的能量, $ {\rm \mathrm{D}} $ 正确。
4. $ {\rm {\mathrm{N}}_{4}} $ 分子结构如图所示,已知断裂 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}—\mathrm{N}} $ 吸收 $ {\rm 167\mathrm{k}\mathrm{J}} $ 能量,断裂 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\equiv \mathrm{N}} $ 吸收 $ {\rm 942\mathrm{k}\mathrm{J}} $ 能量。下列说法正确的是( )
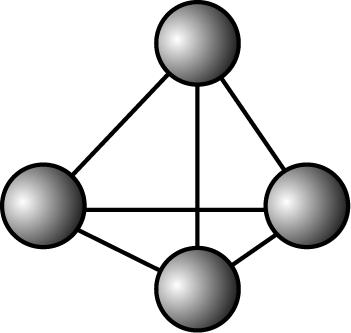
A. $ {\rm {\mathrm{N}}_{4}} $ 比 $ {\rm {\mathrm{N}}_{2}} $ 更稳定
B. $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{4}} $ 转化为 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ ,吸收 $ {\rm 882\mathrm{k}\mathrm{J}} $ 能量
C. $ {\rm {\mathrm{N}}_{4}} $ 中的 $ {\rm \mathrm{N}} $ 原子未满足最外层 $ 8{\mathrm{e}}^{-} $ 结构
D. $ {\rm {\mathrm{N}}_{4}} $ 与 $ {\rm {\mathrm{N}}_{2}} $ 中均含有非极性共价键
答案:D
解析:由题图可知, $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{4}} $ 中含有 $ {\rm 6\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}—\mathrm{N}} $ ,可生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ ,形成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\equiv \mathrm{N}} $ ,则 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{4}} $ 转化为 $ {\rm {\mathrm{N}}_{2}} $ 时化学键断裂吸收的热量为 $ {\rm 6×167\mathrm{k}\mathrm{J}=1002\mathrm{k}\mathrm{J}} $ ,化学键形成放出的热量为 $ {\rm 2×942\mathrm{k}\mathrm{J}=1884\mathrm{k}\mathrm{J}} $ ,所以反应放出的热量为 $ {\rm 1884\mathrm{k}\mathrm{J}-1002\mathrm{k}\mathrm{J}=882\mathrm{k}\mathrm{J}} $ ,则 $ {\rm {\mathrm{N}}_{4}} $ 的能量高于 $ {\rm {\mathrm{N}}_{2}} $ , $ {\rm {\mathrm{N}}_{2}} $ 比 $ {\rm {\mathrm{N}}_{4}} $ 更稳定, $ {\rm \mathrm{A}} $ 、 $ {\rm \mathrm{B}} $ 错误;由分子结构可知, $ {\rm {\mathrm{N}}_{4}} $ 中的每个 $ {\rm \mathrm{N}} $ 原子形成三个共价键,有一个孤电子对,满足最外层 $ 8{\mathrm{e}}^{-} $ 稳定结构, $ {\rm \mathrm{C}} $ 错误; $ {\rm {\mathrm{N}}_{4}} $ 与 $ {\rm {\mathrm{N}}_{2}} $ 中 $ {\rm \mathrm{N}} $ 与 $ {\rm \mathrm{N}} $ 间均形成非极性共价键, $ {\rm \mathrm{D}} $ 正确。
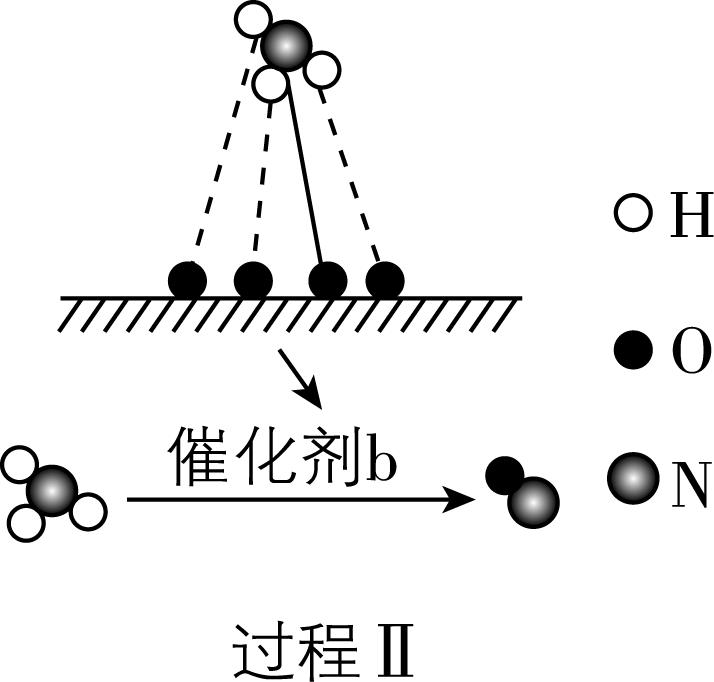
5.氮的转化通过驱动生态系统物质循环支持生命活动,其失衡会引发水体富营养化、酸雨及温室效应等环境问题。氮及其化合物在催化剂作用下的转化过程中的能量变化及机理如图所示。下列分析正确的是( )
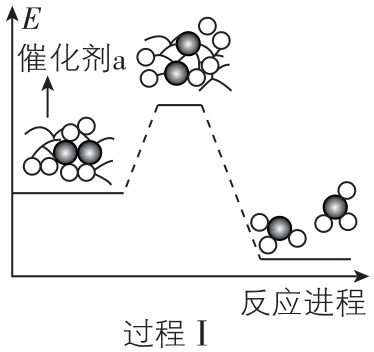
A. 过程Ⅰ、Ⅱ均属于氮的固定
B. 由图可知,过程Ⅰ发生的总反应为放热反应
C. 过程Ⅱ中,在催化剂 $ \mathrm{b} $ 表面被氧化的过程中没有能量变化
D. 过程Ⅱ中,发生反应的化学方程式为 $ {\rm 4{\mathrm{N}\mathrm{H}}_{3}+7{\mathrm{O}}_{2}\xlongequal{}4{\mathrm{N}\mathrm{O}}_{2}+6{\mathrm{H}}_{2}\mathrm{O}} $
答案:B
解析:将游离态 $ {\rm \mathrm{N}} $ 变为化合态 $ {\rm \mathrm{N}} $ 的过程称为氮的固定,过程Ⅰ属于氮的固定,而过程Ⅱ不属于氮的固定, $ {\rm \mathrm{A}} $ 错误;由图示可知,过程Ⅰ中的生成物总能量小于反应物总能量,反应放出热量,因此总反应为放热反应, $ {\rm \mathrm{B}} $ 正确;过程Ⅱ中,在催化剂 $ \mathrm{b} $ 表面 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 被氧化的过程中有化学键的断裂与形成,断键吸热,成键放热,故该变化过程中一定伴随能量变化, $ {\rm \mathrm{C}} $ 错误;在过程Ⅱ中,氨气和氧气反应生成一氧化氮和水,根据得失电子守恒及原子守恒,可知发生反应的化学方程式为 $ {\rm\hspace{-0.5em} \begin{array} {l} \rm 4{\mathrm{N}\mathrm{H}}_{3}+5{\mathrm{O}}_{2}\hspace{-0.5em} \begin{array}{c}{催化剂}\\ \overline{\overline{△}}\end{array} \hspace{-0.5em}4\mathrm{N}\mathrm{O}+6{\mathrm{H}}_{2}\mathrm{O}\end{array} \hspace{-0.5em} } $ , $ {\rm \mathrm{D}} $ 错误。
6.反应 $ {\rm \mathrm{A}+\mathrm{B}\to \mathrm{C}} $ (吸热反应)分两步进行: $ {\rm ①\mathrm{A}+\mathrm{B}\to \mathrm{X}} $ (放热反应); $ {\rm ②\mathrm{X}\to \mathrm{C}} $ (吸热反应)。下列示意图中,能正确表示反应过程中能量变化的是( )
A. 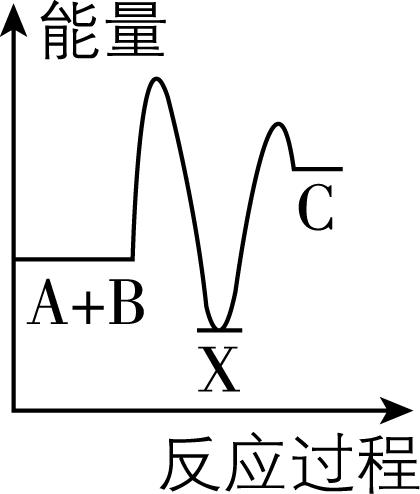
B. 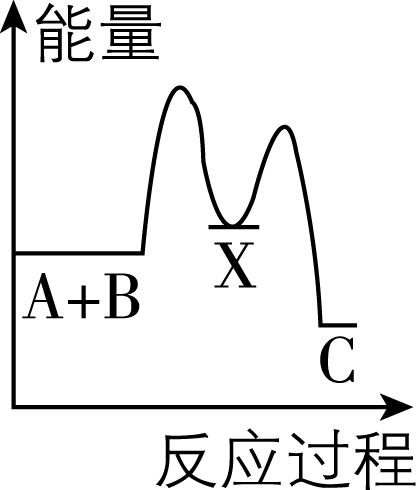
C. 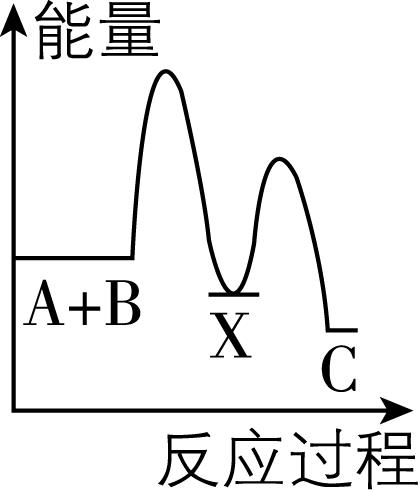
D. 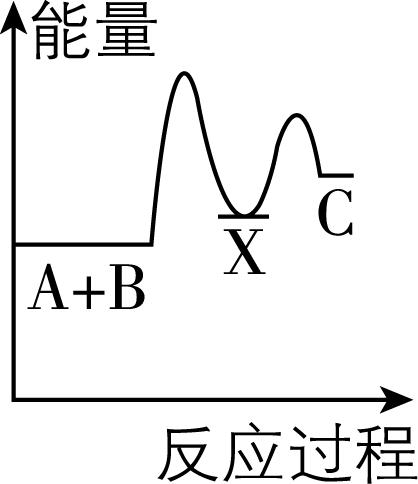
答案:A
解析:放热反应的特点是反应物总能量大于生成物总能量;吸热反应的特点是反应物总能量小于生成物总能量。 $ {\rm \mathrm{A}+\mathrm{B}\to \mathrm{C}} $ 是吸热反应, $ {\rm \mathrm{A}+\mathrm{B}\to \mathrm{X}} $ 是放热反应, $ {\rm \mathrm{X}\to \mathrm{C}} $ 是吸热反应, $ {\rm \mathrm{A}} $ 符合题意; $ {\rm \mathrm{A}+\mathrm{B}\to \mathrm{C}} $ 是放热反应, $ {\rm \mathrm{A}+\mathrm{B}\to \mathrm{X}} $ 是吸热反应, $ {\rm \mathrm{X}\to \mathrm{C}} $ 是放热反应, $ {\rm \mathrm{B}} $ 不符合题意; $ {\rm \mathrm{A}+\mathrm{B}\to \mathrm{C}} $ 是放热反应, $ {\rm \mathrm{X}\to \mathrm{C}} $ 是放热反应, $ {\rm \mathrm{C}} $ 不符合题意; $ {\rm \mathrm{A}+\mathrm{B}\to \mathrm{X}} $ 是吸热反应, $ {\rm \mathrm{D}} $ 不符合题意。
7.化学变化过程中存在物质变化与能量变化,某化学兴趣小组按如图所示装置实验,以验证此结论。
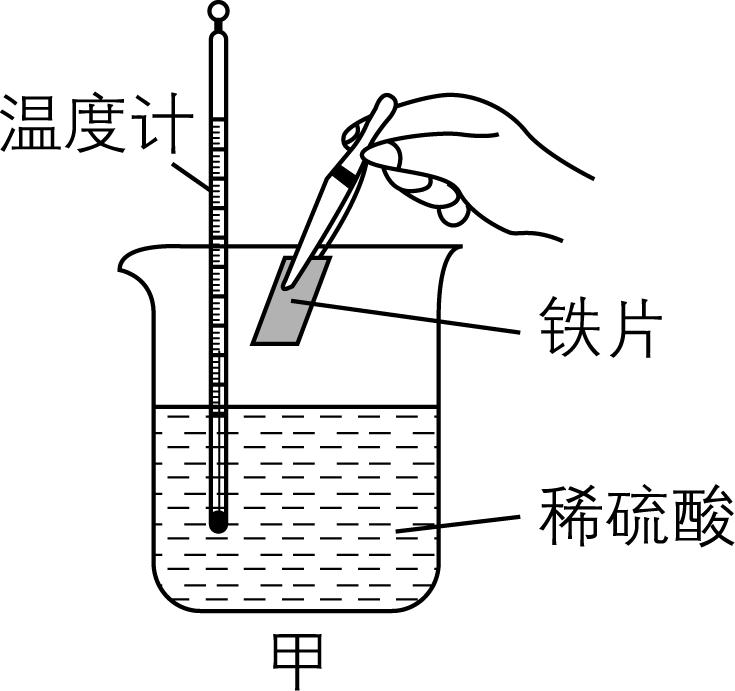
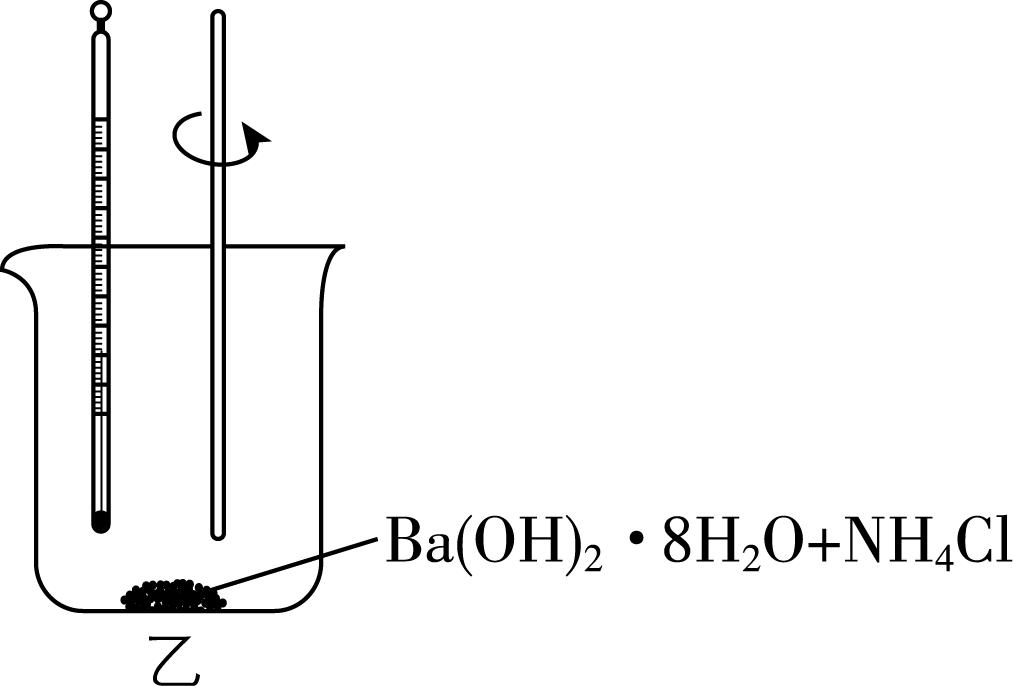
请回答下列问题:
(1) 进行实验时,装置甲中温度计水银的液面 (填“升高”或“降低”),装置乙中反应的化学方程式为 。
(2) 为探究 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 与盐酸的反应是吸热反应还是放热反应,某同学进行了下列实验(盐酸浓度相同,每项实验各做3次,取平均值)。
实验序号 | 试剂 | 固体 | 混合前温度/ $ ℃ $ | 混合后温度/ $ ℃ $ |
$ \mathrm{a} $ | $ {\rm 35\mathrm{m}\mathrm{L}} $ 水 | $ {\rm 2.5\mathrm{g}{\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ | 20.0 | 18.5 |
$ \mathrm{b} $ | $ {\rm 35\mathrm{m}\mathrm{L}} $ 水 | $ {\rm 3.2\mathrm{g}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ | 20.0 | 24.3 |
$ \mathrm{c} $ | $ {\rm 35\mathrm{m}\mathrm{L}} $ 盐酸 | $ {\rm 2.5\mathrm{g}{\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ | 20.0 | 16.2 |
$ \mathrm{d} $ | $ {\rm 35\mathrm{m}\mathrm{L}} $ 盐酸 | $ {\rm 3.2\mathrm{g}{\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ | 20.0 | 25.1 |
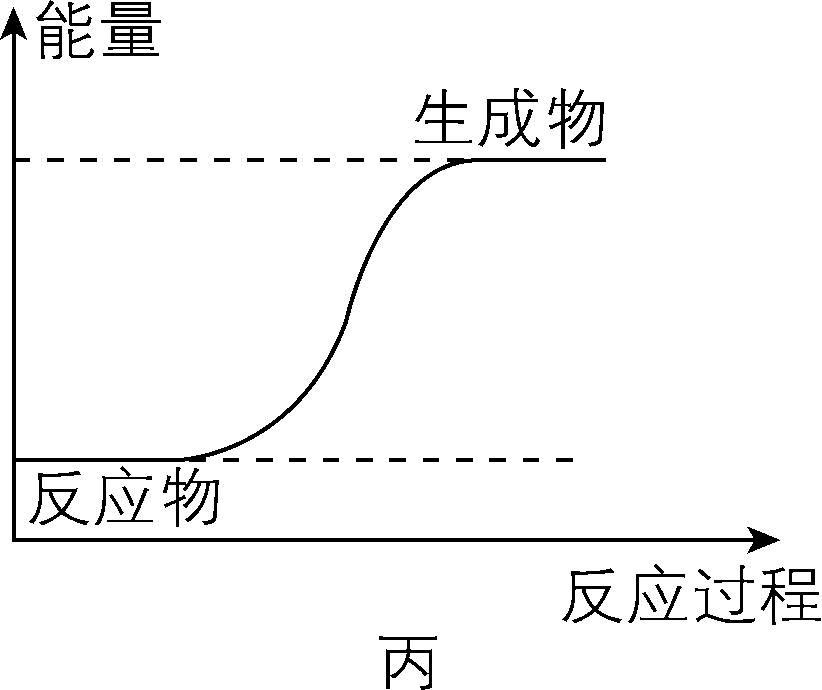
设计 $ \mathrm{a} $ 、 $ \mathrm{b} $ 组实验的目的是 , 和盐酸反应的能量变化情况符合图丙。
答案:(1) 升高; $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}+2{\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}\xlongequal{}{\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}+2{\mathrm{N}\mathrm{H}}_{3}↑+10{\mathrm{H}}_{2}\mathrm{O}} $
(2) 作为对照实验,排除物质溶解对实验的影响; $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $
解析:(1) 装置甲中铁与稀硫酸的反应为放热反应,故温度计中水银的液面升高; $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}} $ 与 $ {\rm {\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}} $ 反应的化学方程式为 $ {\rm \mathrm{B}\mathrm{a}(\mathrm{O}\mathrm{H})_{2}\cdot 8{\mathrm{H}}_{2}\mathrm{O}+2{\mathrm{N}\mathrm{H}}_{4}\mathrm{C}\mathrm{l}\xlongequal{}{\mathrm{B}\mathrm{a}\mathrm{C}\mathrm{l}}_{2}+2{\mathrm{N}\mathrm{H}}_{3}↑+10{\mathrm{H}}_{2}\mathrm{O}} $ 。
(2) $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶于水的过程中也伴随着热量变化,为探究 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ 、 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 与盐酸反应的热效应,需要做对照实验排除溶解过程热效应的影响;分析实验 $ \mathrm{a} $ 、 $ \mathrm{c} $ 可知, $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 与盐酸反应后,混合溶液的温度比 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 在相同量水中溶解后的温度低,说明 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 与盐酸的反应为吸热反应;同理,分析实验 $ \mathrm{b} $ 、 $ \mathrm{d} $ 可知, $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{C}\mathrm{O}}_{3}} $ 与盐酸的反应为放热反应,故 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 与盐酸反应时,符合图丙所示的能量变化。
8.现代社会中,人类的一切活动都离不开能量,研究化学能与热能的转化具有重要价值。回答下列问题:
(1) 某实验小组为了探究化学能与热能的转化,设计了如图所示的三套实验装置(装置中夹持仪器已略去)。
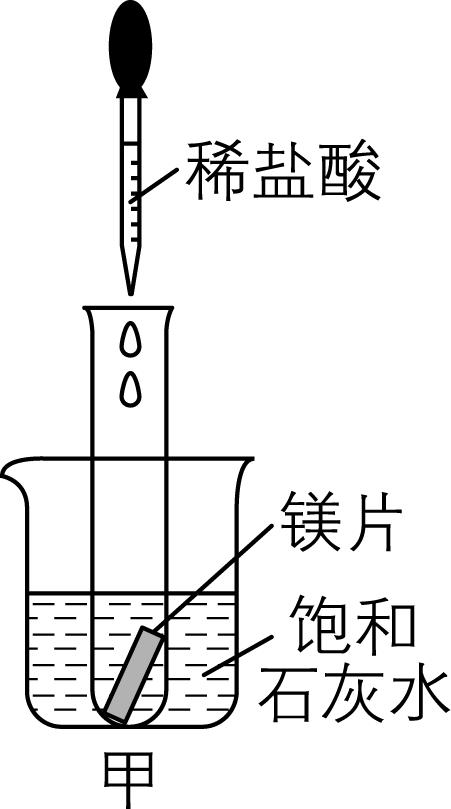
① 观察到甲装置烧杯中的实验现象是 。
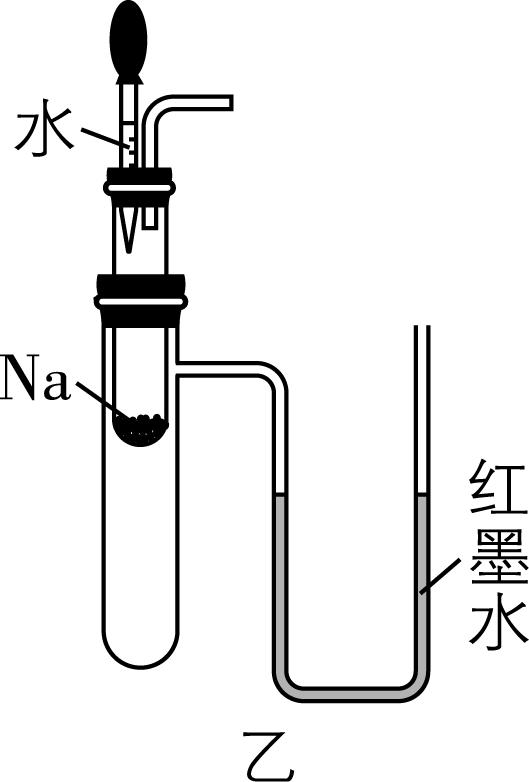
② 用乙装置进行实验(实验前 $ {\rm \mathrm{U}} $ 形管里液面左右相平), $ {\rm \mathrm{U}} $ 形管中可观察到的现象是 ,说明该反应属于 (填“吸热”或“放热”)反应。
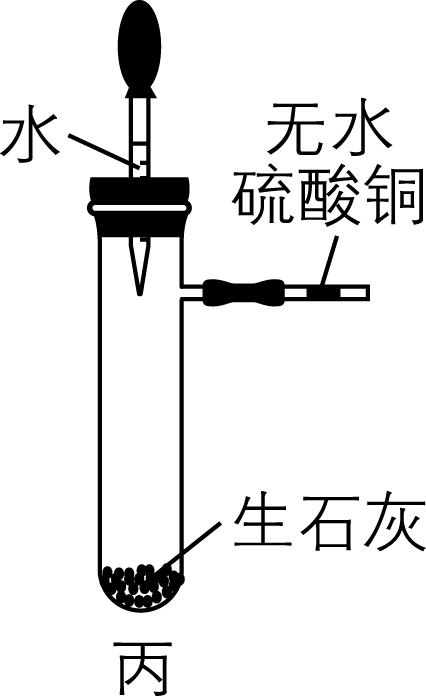
③ 将装置丙中胶头滴管内的水滴到生石灰上,支管处的白色粉末(无水硫酸铜)变为蓝色,其原因是 。
④ 上述三个实验方案验证了以上三个反应的反应物总能量 (填“高于”或“低于”)生成物总能量。
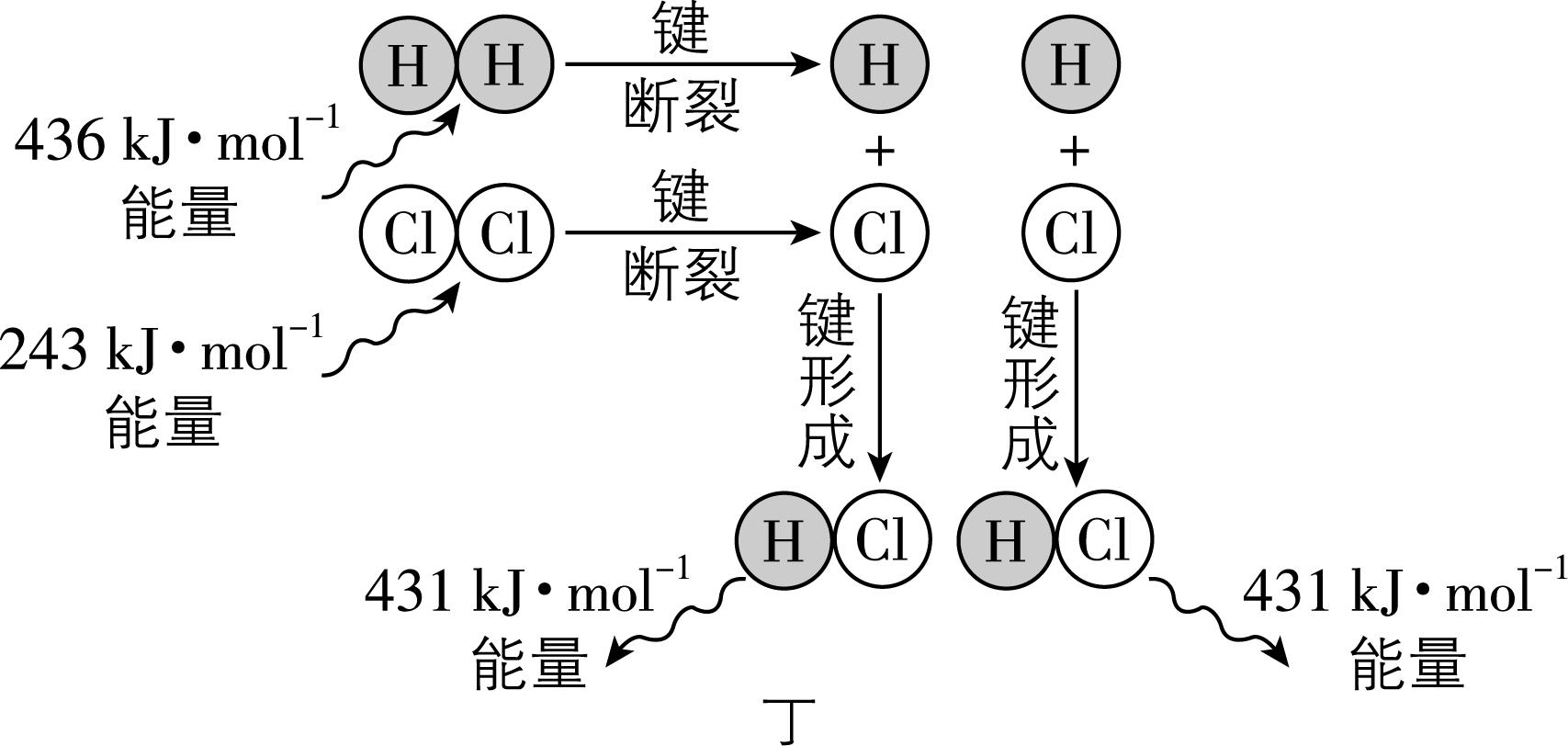
(2) 已知反应 $ {\rm {\mathrm{H}}_{2}(\mathrm{g})+{\mathrm{C}\mathrm{l}}_{2}(\mathrm{g})\xlongequal{}2\mathrm{H}\mathrm{C}\mathrm{l}(\mathrm{g})} $ 的能量变化如图丁所示,该反应生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{C}\mathrm{l}(\mathrm{g})} $ 时, (填“吸收”或“释放”) $ {\rm \mathrm{k}\mathrm{J}} $ 能量。
答案:① 镁片逐渐溶解且表面有大量气泡产生,烧杯中有白色固体析出
② 红墨水的液面左低右高;放热
③ 生石灰与水反应放热,温度升高,水蒸发,无水硫酸铜白色粉末遇水变蓝
④ 高于
(2) 释放;183
解析:① 镁与稀盐酸的反应方程式为 $ {\rm \mathrm{M}\mathrm{g}+2\mathrm{H}\mathrm{C}\mathrm{l}\xlongequal{}{\mathrm{M}\mathrm{g}\mathrm{C}\mathrm{l}}_{2}+{\mathrm{H}}_{2}↑} $ ,镁片逐渐溶解,因生成气体,所以观察到有气泡产生,且该反应放出热量,使烧杯内的饱和石灰水温度升高,由于氢氧化钙的溶解度随温度的升高而降低,所以饱和石灰水中氢氧化钙固体析出。
② 钠与水的反应是放热反应,具支试管中的空气受热膨胀,使红墨水向右管移动,液面左低右高。
③ 生石灰与水反应放出的热量使水蒸发,无水硫酸铜白色粉末遇水变蓝,生成 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}\cdot 5{\mathrm{H}}_{2}\mathrm{O}} $ (蓝色)。
④ 题述实验方案验证了三个反应是放热反应,即反应物总能量高于生成物总能量。
(2) 根据图丁可知,反应 $ {\rm {\mathrm{H}}_{2}(\mathrm{g})+{\mathrm{C}\mathrm{l}}_{2}(\mathrm{g})\xlongequal{}2\mathrm{H}\mathrm{C}\mathrm{l}(\mathrm{g})} $ 的 $ {\rm \mathrm{\Delta }H=} $ 反应物键能之和-生成物键能之和 $ {\rm =(436+243-431×2)\mathrm{k}\mathrm{J}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}=-183\mathrm{k}\mathrm{J}\cdot {\mathrm{m}\mathrm{o}\mathrm{l}}^{-1}} $ ,则该反应生成 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{H}\mathrm{C}\mathrm{l}(\mathrm{g})} $ 时,释放 $ {\rm 183\mathrm{k}\mathrm{J}} $ 能量。
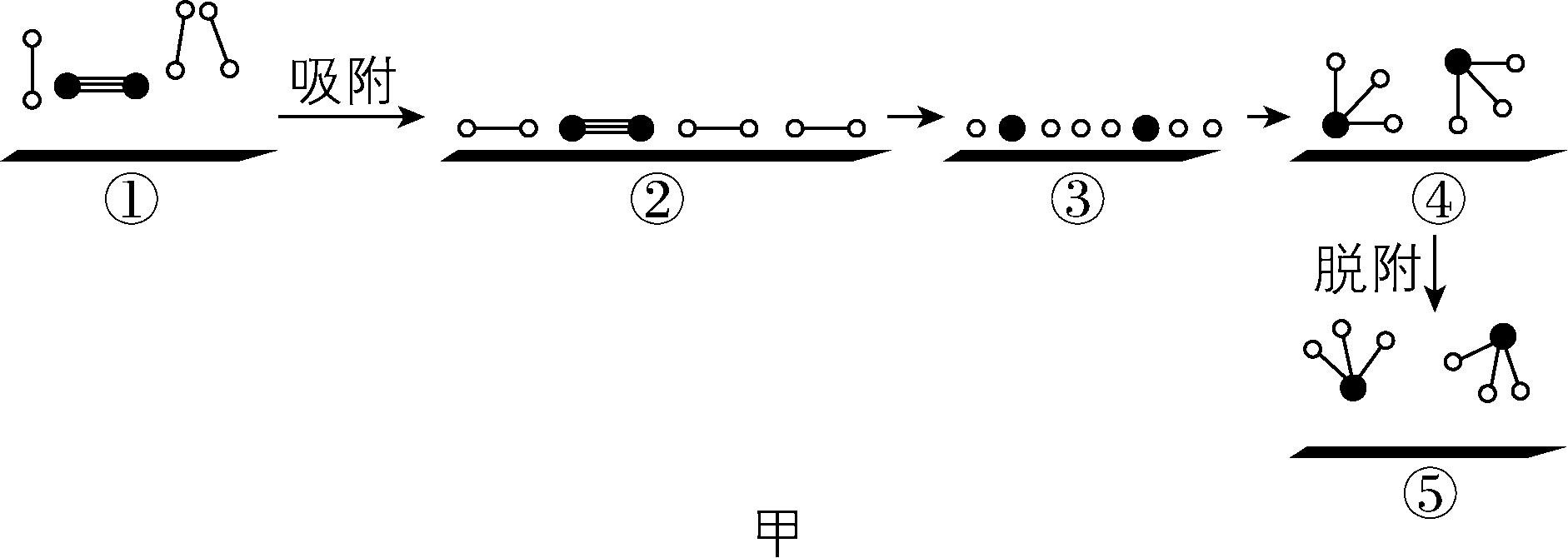
9. 9.某反应的微观历程及反应过程中的能量变化如图甲、乙所示。其中 、
、 、
、 、分别表示 $ {\rm {\mathrm{N}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 、 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 、催化剂。
、分别表示 $ {\rm {\mathrm{N}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 、 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 、催化剂。
下列说法不正确的是( )
A. 该反应为 $ {\rm {\mathrm{N}}_{2}+3{\mathrm{H}}_{2}⇌2{\mathrm{N}\mathrm{H}}_{3}} $
B. $ ①\to ② $ 过程中催化剂与气体之间形成离子键
C. $ ②\to ③ $ 过程中,需要吸收能量
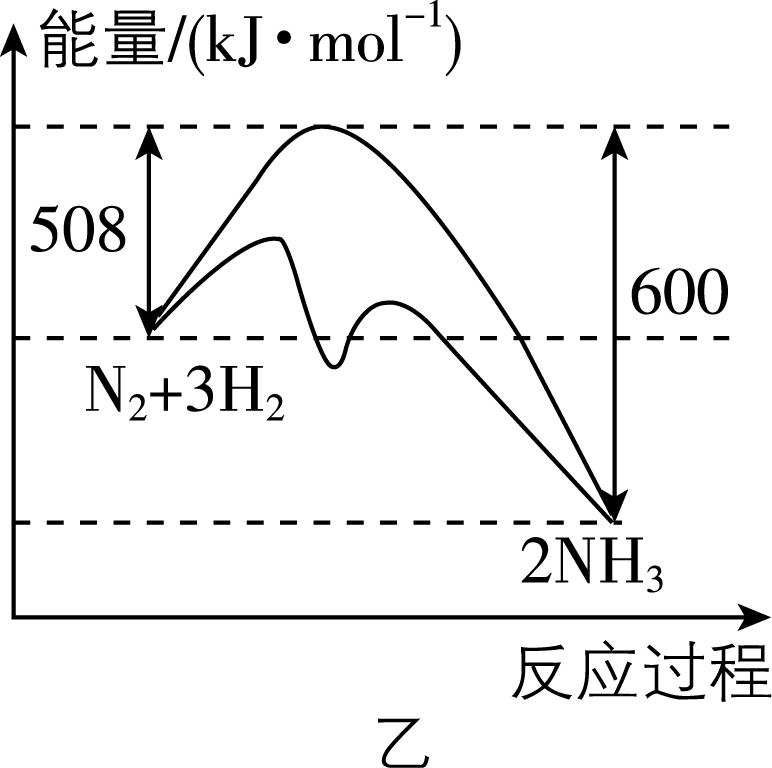
D. 图乙说明该反应中,反应物化学键断裂所吸收的能量小于生成物化学键形成所放出的能量
答案:B
解析:分析题图甲反应历程可知,该反应为 $ {\rm {\mathrm{N}}_{2}+3{\mathrm{H}}_{2}⇌2{\mathrm{N}\mathrm{H}}_{3}} $ , $ {\rm \mathrm{A}} $ 正确; $ ①\to ② $ 过程中氮气、氢气被吸附到了催化剂表面,并未形成离子键, $ {\rm \mathrm{B}} $ 错误; $ ②\to ③ $ 过程是化学键断裂的过程,需要吸收能量, $ {\rm \mathrm{C}} $ 正确;由反应过程中的能量变化图可知,该反应为放热反应,说明反应物化学键断裂所吸收的能量小于生成物化学键形成所放出的能量, $ {\rm \mathrm{D}} $ 正确。






























