课时1 化学反应的速率
一、刷基础
1.下列说法正确的是( )
A. 化学反应速率通常用单位时间内反应物或生成物的质量变化来表示
B. 用不同物质的浓度变化表示同一段时间内、同一反应的速率时,其数值之比等于化学方程式中对应物质的化学计量数之比
C. 化学反应速率指的是某时刻的瞬时速率
D. 化学反应速率的单位由时间单位和物质的量单位决定
答案:B
解析:化学反应速率通常用单位时间内反应物浓度的减小或生成物浓度的增大来表示(取正值), $ {\rm \mathrm{A}} $ 错误;用不同物质的浓度变化表示同一段时间内、同一反应的速率时,其数值之比等于化学方程式中对应物质的化学计量数之比, $ {\rm \mathrm{B}} $ 正确;化学反应速率指的是某时间段内的平均速率, $ {\rm \mathrm{C}} $ 错误;化学反应速率的单位由时间单位和物质的量浓度单位决定, $ {\rm \mathrm{D}} $ 错误。
2.某温度下,在 $ {\rm 3\mathrm{L}} $ 恒容密闭容器中投入一定量的A、B,发生反应: $ {\rm 3\mathrm{A}(\mathrm{g})+b\mathrm{B}(\mathrm{g})⇌c\mathrm{C}(\mathrm{g})+2\mathrm{D}(\mathrm{s})} $ , $ 12\mathrm{s} $ 时生成C的物质的量为 $ 1.2\mathrm{m}\mathrm{o}\mathrm{l} $ (反应进程如图所示)。下列说法中正确的是( )
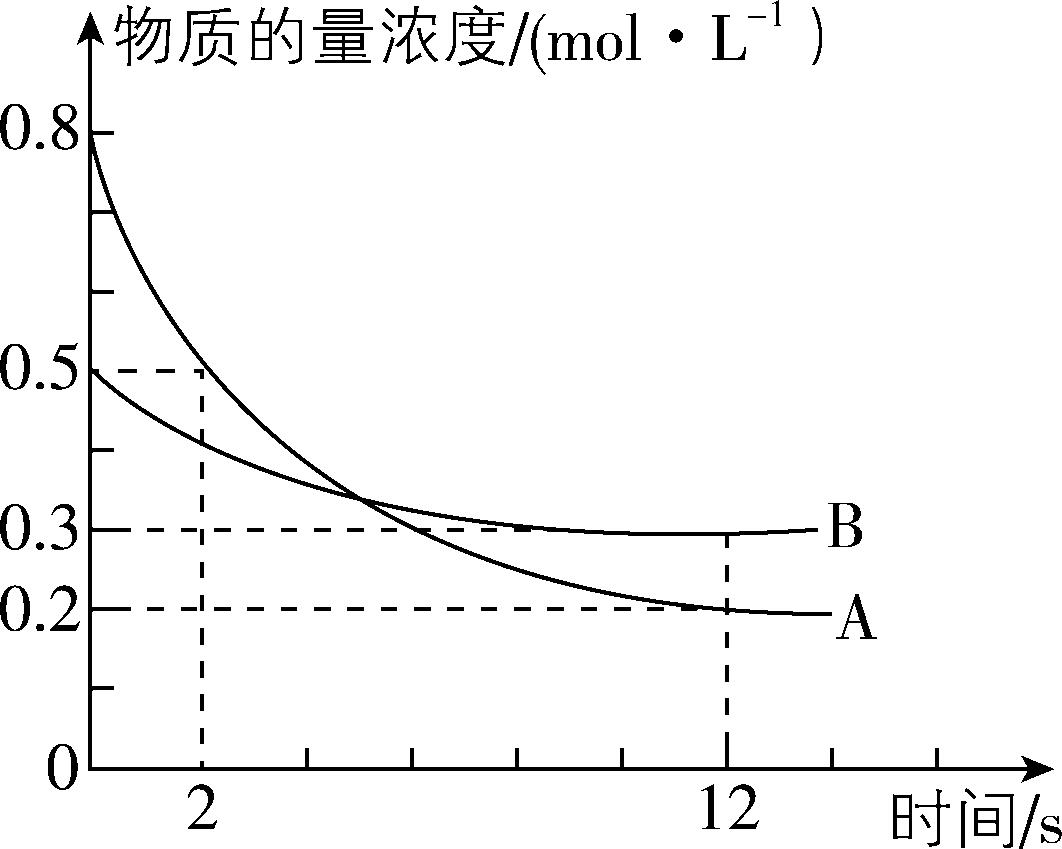
A. 图中两曲线相交时,A的消耗速率等于A的生成速率
B. 化学计量数之比 $ b:c=2:1 $
C. $ 12\mathrm{s} $ 时,B的转化率为 $ 40\% $
D. $ 0\sim 2\mathrm{s} {\rm ,D} $ 的平均反应速率为 $ {\rm 0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $
答案:C
解析:由图可知,两曲线相交后, $ {\rm \mathrm{A}} $ 的浓度还在降低, $ {\rm \mathrm{A}} $ 的消耗速率大于 $ {\rm \mathrm{A}} $ 的生成速率, $ {\rm \mathrm{A}} $ 错误;浓度变化量之比等于化学计量数之比, $ 12\mathrm{s} $ 内 $ {\rm \mathrm{A}} $ 、 $ {\rm \mathrm{B}} $ 、 $ {\rm \mathrm{C}} $ 的浓度变化分别为 $ {\rm 0.6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 、 $ {\rm 0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 、 $ {\rm \dfrac{1.2\mathrm{m}\mathrm{o}\mathrm{l}}{3\mathrm{L}}=0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,化学计量数之比 $ b:c=1:2 $ , $ {\rm \mathrm{B}} $ 错误; $ 12\mathrm{s} $ 内, $ {\rm \mathrm{B}} $ 的浓度由 $ {\rm 0.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 变为 $ {\rm 0.3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ 12\mathrm{s} $ 时 $ {\rm \mathrm{B}} $ 的转化率为 $ {\rm \dfrac{(0.5-0.3)\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}}{0.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}}×100\%=40\%} $ , $ {\rm \mathrm{C}} $ 正确; $ {\rm \mathrm{D}} $ 是固体,不能用 $ {\rm \mathrm{D}} $ 的浓度变化表示反应速率, $ {\rm \mathrm{D}} $ 错误。
3.将 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{A}} $ 和 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{B}} $ 在 $ {\rm 2\mathrm{L}} $ 的恒容密闭容器中混合,一定条件下发生反应: $ {\rm \mathrm{A}(\mathrm{g})+n\mathrm{B}(\mathrm{g})⇌3\mathrm{C}(\mathrm{g})} $ , $ 5 \min $ 后测得A剩余 $ 0.8\mathrm{m}\mathrm{o}\mathrm{l} {\rm ,B} $ 的平均反应速率为 $ {\rm 0.24\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,则 $ n $ 为( )
A. 1
B. 2
C. 3
D. 4
答案:B
解析:根据题意可计算出 $ 5 \min $ 内 $ {\rm \mathrm{A}} $ 的平均反应速率 $ {\rm v(\mathrm{A})=\dfrac{(2-0.8)\mathrm{m}\mathrm{o}\mathrm{l}}{2\mathrm{L}×5 \min }=0.12\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,已知 $ 5 \min $ 内 $ {\rm \mathrm{B}} $ 的平均反应速率 $ {\rm v(\mathrm{B})=0.24\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,又因为同一反应、同一时间段内用不同物质表示的化学反应速率之比等于相应物质的化学计量数之比,即 $ {\rm \dfrac{v(\mathrm{A})}{v(\mathrm{B})}=\dfrac{1}{n}} $ ,所以 $ n=2 $ ,选 $ {\rm \mathrm{B}} $ 。
4.反应 $ {\rm 4\mathrm{A}(\mathrm{s})+5\mathrm{B}(\mathrm{g})⇌4\mathrm{C}(\mathrm{g})+6\mathrm{D}(\mathrm{g})} $ 在 $ {\rm 10\mathrm{L}} $ 密闭容器中进行,半分钟后,D的物质的量增加了 $ 0.45\mathrm{m}\mathrm{o}\mathrm{l} $ ,则下列说法正确的是( )
A. 半分钟时 $ {\rm v(\mathrm{B})=0.0015\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $
B. 半分钟内 $ {\rm v(\mathrm{A})=0.0010\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $
C. 半分钟内 $ {\rm v(\mathrm{C})=0.0010\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $
D. 半分钟内 $ {\rm v(\mathrm{D})=0.045\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $
答案:C
解析:化学反应速率是一段时间内的平均速率,不是瞬时速率,半分钟时的 $ {\rm v(\mathrm{B})} $ 是指瞬时速率,根据题给信息无法计算, $ {\rm \mathrm{A}} $ 错误; $ {\rm \mathrm{A}} $ 物质是固体,浓度视为常数,不能用其浓度变化表示反应速率, $ {\rm \mathrm{B}} $ 错误;半分钟后, $ {\rm \mathrm{D}} $ 的物质的量增加了 $ 0.45\mathrm{m}\mathrm{o}\mathrm{l} $ ,则半分钟内 $ {\rm v(\mathrm{D})=\dfrac{\mathrm{\Delta }n(\mathrm{D})}{V\mathrm{\Delta }t}=\dfrac{0.45\mathrm{m}\mathrm{o}\mathrm{l}}{10\mathrm{L}×30\mathrm{s}}=0.0015\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $ , $ {\rm v(\mathrm{C})=\dfrac{4}{6}v(\mathrm{D})=0.0010\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $ , $ {\rm \mathrm{C}} $ 正确、 $ {\rm \mathrm{D}} $ 错误。
5.关于 $ {\rm 2\mathrm{A}(\mathrm{g})+\mathrm{B}(\mathrm{g})⇌3\mathrm{C}(\mathrm{g})} $ 的化学反应,下列表示的反应速率最快的是( )
A. $ {\rm v(\mathrm{A})=0.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
B. $ {\rm v(\mathrm{B})=0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
C. $ {\rm v(\mathrm{C})=0.01\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $
D. $ {\rm v(\mathrm{C})=1.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
答案:B
解析:统一单位并换算成用物质 $ {\rm \mathrm{B}} $ 表示的反应速率,再比较数值大小。 $ {\rm \mathrm{A}} $ 项, $ {\rm v(\mathrm{B})=\dfrac{v(\mathrm{A})}{2}=\dfrac{0.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}}{2}=0.25\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ; $ {\rm \mathrm{B}} $ 项, $ {\rm v(\mathrm{B})=0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ; $ {\rm \mathrm{C}} $ 项, $ {\rm v(\mathrm{B})=\dfrac{v(\mathrm{C})}{3}=\dfrac{0.01\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}}{3}=\dfrac{0.01\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}}{3}×60\mathrm{s}\cdot { \min }^{-1}=0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ; $ {\rm \mathrm{D}} $ 项, $ {\rm v(\mathrm{B})=\dfrac{v(\mathrm{C})}{3}=\dfrac{1.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}}{3}\approx 0.367\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,选 $ {\rm \mathrm{B}} $ 。
6.化学反应: $ {\rm \mathrm{A}(\mathrm{g})+3\mathrm{B}(\mathrm{g})\xlongequal{}\mathrm{C}(\mathrm{g})+2\mathrm{D}(\mathrm{g})} $ ,在4种不同情况下的化学反应速率分别为 $ {\rm ①v(\mathrm{A})=0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $ ; $ {\rm ②v(\mathrm{B})=0.45\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $ ; $ {\rm ③v(\mathrm{C})=0.3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $ ; $ {\rm ④v(\mathrm{D})=0.45\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $ 。下列有关化学反应速率的比较中正确的是( )
A. $ ① > ② > ③ > ④ $
B. $ ① < ③ < ②=④ $
C. $ ① > ②=③ > ④ $
D. $ ② < ① < ④ < ③ $
答案:D
解析:化学反应中,某物质表示的化学反应速率与该物质的化学计量数的比值越大,化学反应速率越大,由题中数据可知, $ {\rm \dfrac{v(\mathrm{C})}{1}(0.3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}) > \dfrac{v(\mathrm{D})}{2}(0.225\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}) > \dfrac{v(\mathrm{A})}{1}(0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}) > \dfrac{v(\mathrm{B})}{3}(0.15\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1})} $ ,故化学反应速率: $ ② < ① < ④ < ③ $ ,选 $ {\rm \mathrm{D}} $ 。
7.下列措施对改变反应速率的影响正确的是( )
A. $ {\rm {\mathrm{C}\mathrm{a}\mathrm{C}\mathrm{O}}_{3}} $ 与稀盐酸反应,加入 $ {\rm \mathrm{N}\mathrm{a}\mathrm{C}\mathrm{l}} $ 溶液后不会改变反应速率
B. 在合成氨反应 $ {\rm {\mathrm{N}}_{2}(\mathrm{g})+3{\mathrm{H}}_{2}(\mathrm{g})⇌2{\mathrm{N}\mathrm{H}}_{3}(\mathrm{g})} $ 中,保持温度和容器容积不变,增加氮气的量能增大反应速率
C. 加入催化剂一定加快反应的速率
D. $ {\rm \mathrm{Z}\mathrm{n}} $ 与稀硫酸反应制取 $ {\rm {\mathrm{H}}_{2}} $ ,改用 $ 98\% $ 的浓硫酸将加快 $ {\rm {\mathrm{H}}_{2}} $ 的生成速率
答案:B
解析: $ {\rm {\mathrm{C}\mathrm{a}\mathrm{C}\mathrm{O}}_{3}} $ 与稀盐酸反应的实质是碳酸钙与氢离子反应,加入 $ {\rm \mathrm{N}\mathrm{a}\mathrm{C}\mathrm{l}} $ 溶液后,氢离子浓度减小,反应速率减慢, $ {\rm \mathrm{A}} $ 错误;保持温度和容器容积不变,增加氮气的量,则氮气的浓度增加,因此能增大反应速率, $ {\rm \mathrm{B}} $ 正确;存在可使反应速率减缓的催化剂, $ {\rm \mathrm{C}} $ 错误; $ 98\% $ 的浓硫酸具有强氧化性,与 $ {\rm \mathrm{Z}\mathrm{n}} $ 反应生成的是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 而不是 $ {\rm {\mathrm{H}}_{2}} $ , $ {\rm \mathrm{D}} $ 错误。
8.反应 $ {\rm \mathrm{C}(\mathrm{s})+{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})⇌\mathrm{C}\mathrm{O}(\mathrm{g})+{\mathrm{H}}_{2}(\mathrm{g})} $ 在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A. 降低温度
B. 将容器的容积缩小一半
C. 保持容积不变,充入 $ {\rm {\mathrm{N}}_{2}} $ 使体系压强增大
D. 保持压强不变,充入 $ {\rm {\mathrm{N}}_{2}} $ 使容器容积变大
答案:C
解析:降低温度,反应速率减小, $ {\rm \mathrm{A}} $ 错误;将容器的容积缩小一半,反应物浓度变大,反应速率增大, $ {\rm \mathrm{B}} $ 错误;保持容积不变,充入 $ {\rm {\mathrm{N}}_{2}} $ 使体系压强增大,反应物的浓度不变,对反应速率几乎没有影响, $ {\rm \mathrm{C}} $ 正确;保持压强不变,充入 $ {\rm {\mathrm{N}}_{2}} $ 使容器容积变大,反应物浓度变小,反应速率减小, $ {\rm \mathrm{D}} $ 错误。
9.反应 $ {\rm a\mathrm{A}(\mathrm{g})+b\mathrm{B}(\mathrm{g})\xlongequal{}c\mathrm{C}(\mathrm{g})} $ 在容积和温度恒定的容器中进行,在某一分钟内测得:A减少 $ {\rm 0.15\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1} ,B} $ 减少 $ {\rm 0.05\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1} ,C} $ 增加 $ {\rm 0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,则下列叙述正确的是( )
A. 随着反应的进行,体系的压强逐渐增大
B. 化学计量数之比 $ a:b:c=3:1:2 $
C. 单位时间内反应物浓度的减少量等于生成物浓度的增加量
D. 若在前 $ 10\mathrm{s} $ 内A减少了 $ x\mathrm{m}\mathrm{o}\mathrm{l} $ ,则在前 $ 20\mathrm{s} $ 内A减少了 $ 2x\mathrm{m}\mathrm{o}\mathrm{l} $
答案:B
解析:随着反应的进行,气体的总物质的量浓度逐渐减小,在容器容积和温度不变的条件下,气体物质的量减小,体系的压强逐渐减小, $ {\rm \mathrm{A}} $ 错误;各物质浓度变化量之比等于化学计量数之比,则 $ a:b:c=0.15:0.05:0.1=3:1:2 $ , $ {\rm \mathrm{B}} $ 正确;由题干信息可知,单位时间内反应物浓度的减少量与生成物浓度的增加量不相等, $ {\rm \mathrm{C}} $ 错误;第2个 $ 10\mathrm{s} $ 内的反应速率比前 $ 10\mathrm{s} $ 内小,故第2个 $ 10\mathrm{s} $ 内减少的 $ {\rm \mathrm{A}} $ 的物质的量小于 $ x\mathrm{m}\mathrm{o}\mathrm{l} $ ,前 $ 20\mathrm{s} $ 内减少的 $ {\rm \mathrm{A}} $ 的物质的量小于 $ 2x\mathrm{m}\mathrm{o}\mathrm{l} $ , $ {\rm \mathrm{D}} $ 错误。
10.在某温度和容积不变的密闭容器中,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变化的曲线如图所示,则下列叙述正确的是( )
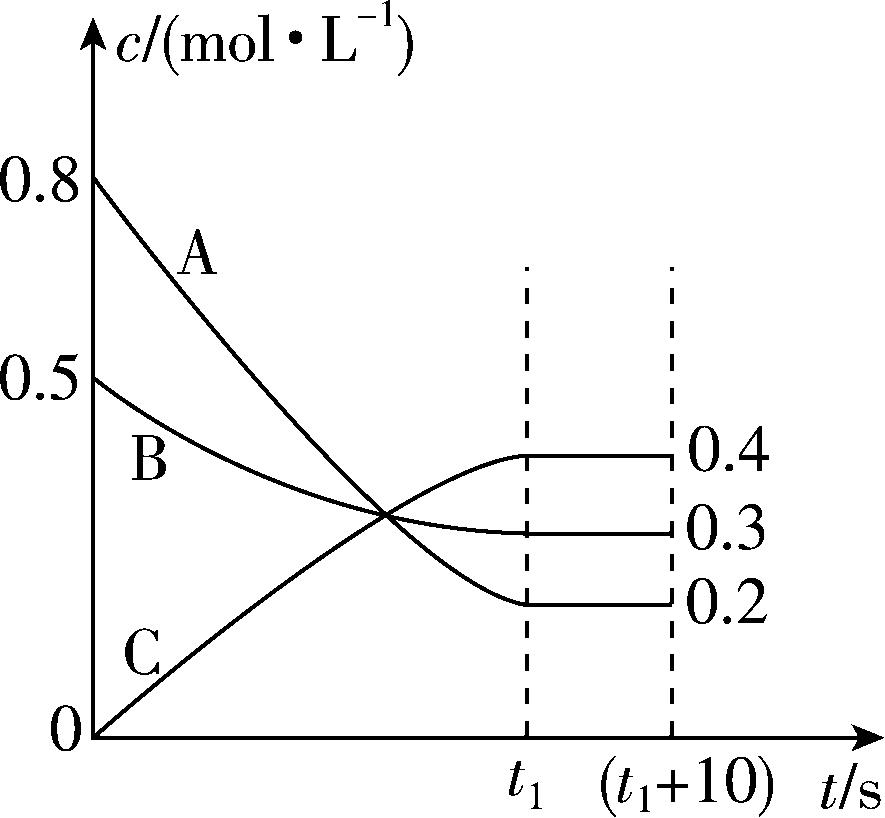
A. 该反应的化学方程式为 $ {\rm \mathrm{A}(\mathrm{g})+3\mathrm{B}(\mathrm{g})⇌2\mathrm{C}(\mathrm{g})} $
B. $ {t}_{1}\mathrm{s} $ 时该反应已停止
C. 恒温恒容条件下充入氩气,使容器压强增大,则反应速率不变
D. $ {t}_{1}\mathrm{s} $ 时,反应物A的转化率为 $ 25\% $
答案:C
解析: $ 0\sim {t}_{1}\mathrm{s} $ , $ {\rm \mathrm{A}} $ 的浓度减小了 $ {\rm 0.8\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}-0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}=0.6\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ {\rm \mathrm{B}} $ 的浓度减小了 $ {\rm 0.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}-0.3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}=0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ {\rm \mathrm{C}} $ 的浓度增大了 $ {\rm 0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,根据各物质浓度变化量之比等于化学计量数之比,可得该反应的化学方程式为 $ {\rm 3\mathrm{A}(\mathrm{g})+\mathrm{B}(\mathrm{g})⇌2\mathrm{C}(\mathrm{g})} $ , $ {\rm \mathrm{A}} $ 错误; $ {t}_{1}\mathrm{s} $ 时,反应达到平衡状态,正、逆反应速率相等且不为0,反应并没有停止,是动态平衡, $ {\rm \mathrm{B}} $ 错误;恒温恒容条件下充入氩气,使容器压强增大,但是反应物和产物浓度不变,则反应速率不变, $ {\rm \mathrm{C}} $ 正确;设反应容器容积为 $ {\rm V\mathrm{L}} $ ,由图可知, $ {t}_{1}\mathrm{s} $ 时,反应物 $ {\rm \mathrm{A}} $ 的转化率 $ {\rm =\dfrac{(0.8-0.2)V\mathrm{m}\mathrm{o}\mathrm{l}}{0.8V\mathrm{m}\mathrm{o}\mathrm{l}}×100\%=75\%} $ , $ {\rm \mathrm{D}} $ 错误。
11.为了探究外界条件对 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 分解反应速率的影响,某同学分别在三支试管中加入了相同体积的 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液,并测量收集 $ {\rm V\mathrm{m}\mathrm{L}} $ 气体所需的时间,实验记录如下:
实验序号 | $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 溶液浓度 | 催化剂 | 所用时间 |
① | $ 5\% $ | 2滴 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{F}\mathrm{e}\mathrm{C}\mathrm{l}}_{3}} $ 溶液 | $ {t}_{1} $ |
② | $ 10\% $ | 2滴 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{F}\mathrm{e}\mathrm{C}\mathrm{l}}_{3}} $ 溶液 | $ {t}_{2} $ |
③ | $ 10\% $ | 2滴 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ 溶液 | $ {t}_{3} $ |
下列结论错误的是( )
A. 实验①②研究的是浓度对反应速率的影响
B. 实验②③研究的是不同催化剂对反应速率的影响
C. 若 $ {t}_{3} > {t}_{2} $ ,则说明 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 比 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ 对 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 分解催化效果好
D. 若探究温度对反应速率的影响,该实验不宜过度加热
答案:C
解析:实验①②中过氧化氢的浓度不同,其他因素相同,则其研究的是浓度对反应速率的影响, $ {\rm \mathrm{A}} $ 正确;实验②③中过氧化氢浓度相同,②中加入的催化剂是氯化铁,③中加入的催化剂是硫酸铜,研究的是不同催化剂对反应速率的影响, $ {\rm \mathrm{B}} $ 正确;实验②③中,两种催化剂的阳离子和阴离子均不同,若 $ {t}_{3} > {t}_{2} $ ,不能说明 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 比 $ {\rm {\mathrm{C}\mathrm{u}}^{2+}} $ 对 $ {\rm {\mathrm{H}}_{2}{\mathrm{O}}_{2}} $ 分解催化效果好, $ {\rm \mathrm{C}} $ 错误;过度加热会导致较多的水蒸气混入气体中,影响气体体积的测定, $ {\rm \mathrm{D}} $ 正确。
12.硫代硫酸钠 $ {\rm ({\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3})} $ 是重要的还原剂,能被酸性 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液氧化,反应原理如下: $ {\rm 5{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}+8{\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}+7{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}\xlongequal{}8{\mathrm{M}\mathrm{n}\mathrm{S}\mathrm{O}}_{4}+5{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}+4{\mathrm{K}}_{2}{\mathrm{S}\mathrm{O}}_{4}+7{\mathrm{H}}_{2}\mathrm{O}} $ 。某学习小组为探究影响该化学反应速率的因素,设计了如表所示系列实验。
实验序号 | 温度/ $ ℃ $ | $ {\rm V/\mathrm{m}\mathrm{L}} $ | 紫色恰好褪去的时间/ $ \mathrm{s} $ |
稀硫酸 $ {\rm (1.5000\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1})} $ | 蒸馏水 | $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 溶液 $ {\rm (0.1250\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1})} $ | $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液 $ {\rm (0.2500\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1})} $ |
① | 25 | 5.00 | 0 | 25.00 | 10.00 | $ {t}_{1} $ |
② | 25 | 5.00 | 10.00 | 15.00 | $ {\rm {V}_{1}} $ | $ {t}_{2} $ |
③ | 40 | $ {\rm {V}_{2}} $ | $ {\rm {V}_{3}} $ | 15.00 | $ {\rm {V}_{4}} $ | $ {t}_{3} $ |
下列说法错误的是( )
A. 实验②和③探究温度对反应速率的影响,则需 $ {\rm {V}_{3}={V}_{4}=10.00} $
B. $ {t}_{1} < {t}_{2} $ , $ {t}_{3} < {t}_{2} $
C. 实验中除能观察到溶液紫色褪去外还能观察到溶液变浑浊
D. 若实验①中, $ {t}_{1}=5\mathrm{s} $ ,则前 $ 5\mathrm{s} $ 内平均反应速率 $ {\rm v({\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4})=0.0500\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $
答案:D
解析:实验①和②的 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 溶液体积不同,探究 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 溶液浓度对该反应速率的影响,则其他条件应保持相同,溶液总体积为 $ {\rm 40.00\mathrm{m}\mathrm{L}} $ ,实验②中蒸馏水为 $ {\rm 10.00\mathrm{m}\mathrm{L}} $ ,则 $ {\rm {V}_{1}=10.00} $ ;实验②和③温度不同,则保持其他条件相同,即实验③中 $ {\rm {V}_{2}=5.00} $ 、 $ {\rm {V}_{3}=10.00} $ , $ {\rm {V}_{4}=10.00} $ , $ {\rm \mathrm{A}} $ 正确。实验①和②温度相同,但实验②混合溶液中 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 浓度较低,反应速率更慢,故 $ {t}_{1} < {t}_{2} $ ;实验②和③中仅温度不同,其他条件相同,实验③温度更高,反应速率更快,故 $ {t}_{3} < {t}_{2} $ , $ {\rm \mathrm{B}} $ 正确。 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 物质的量为 $ 0.25×10×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l}=2.5×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l} $ ,实验②和③中硫酸物质的量为 $ 1.5×5×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l}=7.5×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l} $ ,硫代硫酸钠物质的量为 $ 0.125×15×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l}=1.875×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l} $ ,根据化学方程式 $ {\rm 5{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}+8{\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}+7{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}\xlongequal{}8{\mathrm{M}\mathrm{n}\mathrm{S}\mathrm{O}}_{4}+5{\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}\mathrm{O}}_{4}+4{\mathrm{K}}_{2}{\mathrm{S}\mathrm{O}}_{4}+7{\mathrm{H}}_{2}\mathrm{O}} $ , $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 完全反应, $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{S}}_{2}{\mathrm{O}}_{3}} $ 与 $ {\rm {\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ 过量,酸性条件下, $ {\rm {\mathrm{S}}_{2}{\mathrm{O}}_{3}^{2-}} $ 发生歧化反应生成 $ {\rm \mathrm{S}} $ 和 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ ,因此实验中除能观察到溶液紫色褪去外还能观察到溶液变浑浊, $ {\rm \mathrm{C}} $ 正确。实验①中 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 的初始浓度为 $ {\rm \dfrac{0.25×10}{40}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}=0.0625\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ (稀释后),初始至完全反应时平均速率 $ {\rm v({\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4})=\dfrac{0.0625}{5}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}=0.0125\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot {\mathrm{s}}^{-1}} $ , $ {\rm \mathrm{D}} $ 错误。
二、刷提升
1.下列措施可减慢化学反应速率的是( )
A. 葡萄糖转化为乙醇时,加入酒化酶
B. 在糕点、月饼等食品的包装袋内放置除氧剂
C. 煤燃烧时,向炉膛里鼓风,并用煤粉代替煤块
D. 向铁屑与稀硫酸反应的溶液中加几滴 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ 溶液
答案:B
解析:葡萄糖转化为乙醇时,酒化酶是催化剂,能够加快化学反应速率, $ {\rm \mathrm{A}} $ 不符合题意;在糕点、月饼等食品的包装袋内放置除氧剂,可减小食品包装袋内 $ {\rm {\mathrm{O}}_{2}} $ 的浓度,从而减慢化学反应速率, $ {\rm \mathrm{B}} $ 符合题意;煤燃烧时,向炉膛里鼓风可以增大氧气浓度,用煤粉代替煤块可以增大固体与气体的接触面积,均能加快化学反应速率, $ {\rm \mathrm{C}} $ 不符合题意;向铁屑与稀硫酸反应的溶液中加几滴 $ {\rm {\mathrm{C}\mathrm{u}\mathrm{S}\mathrm{O}}_{4}} $ 溶液,铁置换出的铜附着在铁上,形成原电池,从而加快化学反应速率, $ {\rm \mathrm{D}} $ 不符合题意。
2.下列措施对增大反应速率明显有效的是( )
A. 恒温、恒容条件下,向 $ {\rm \mathrm{C}(\mathrm{s})+{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})⇌\mathrm{C}\mathrm{O}(\mathrm{g})+{\mathrm{H}}_{2}(\mathrm{g})} $ 反应体系中增加C的量
B. $ {\rm \mathrm{F}\mathrm{e}} $ 与稀硫酸反应制取 $ {\rm {\mathrm{H}}_{2}} $ 时,改用浓硫酸
C. 过氧化氢分解时,加入适量的 $ {\rm {\mathrm{M}\mathrm{n}\mathrm{O}}_{2}} $
D. 合成氨反应中,在恒温、恒容条件下充入氩气使体系压强增大
答案:C
解析:碳为固体,增加反应体系中碳的量不影响反应速率, $ {\rm \mathrm{A}} $ 错误;铁与浓硫酸反应不生成氢气,且常温下铁遇浓硫酸发生钝化,阻碍了反应的进行, $ {\rm \mathrm{B}} $ 错误;二氧化锰可以催化过氧化氢分解,加快反应速率, $ {\rm \mathrm{C}} $ 正确;恒温、恒容条件下充入氩气使体系压强增大,但是不改变反应物的浓度,反应速率不受影响, $ {\rm \mathrm{D}} $ 错误。
3.少量铁粉与 $ {\rm 100\mathrm{m}\mathrm{L}0.01\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 的稀盐酸反应,为了加快反应速率而不改变产生 $ {\rm {\mathrm{H}}_{2}} $ 的量,可以使用如下方法中的( )
①将铁粉换成铁块 ②加入 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}} $ 固体
③将 $ {\rm 0.01\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 的稀盐酸换成 $ 98\% $ 的浓硫酸
④加入 $ {\rm \mathrm{N}\mathrm{a}\mathrm{C}\mathrm{l}} $ 溶液 ⑤适当升高温度(不考虑盐酸挥发) ⑥改用 $ {\rm 100\mathrm{m}\mathrm{L}0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 稀盐酸
A. ②④
B. ①③
C. ⑤⑥
D. ④⑤
答案:C
解析:①将铁粉换为铁块会导致反应物接触面积减小,反应速率会减慢,不符合题意;②加入 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{N}\mathrm{O}}_{3}} $ 固体引入了 $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ , $ {\rm {\mathrm{N}\mathrm{O}}_{3}^{-}} $ 在酸性条件下会被 $ {\rm \mathrm{F}\mathrm{e}} $ 还原生成氮氧化物,得不到 $ {\rm {\mathrm{H}}_{2}} $ ,不符合题意;③铁与浓硫酸反应不生成 $ {\rm {\mathrm{H}}_{2}} $ ,且常温下铁遇浓硫酸发生钝化,不符合题意;④加入 $ {\rm \mathrm{N}\mathrm{a}\mathrm{C}\mathrm{l}} $ 溶液, $ {\rm {\mathrm{H}}^{+}} $ 浓度变小,反应速率减慢,不符合题意;⑤适当升高温度会加快反应速率,不改变生成氢气的量,符合题意;⑥改用 $ {\rm 100\mathrm{m}\mathrm{L}0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 稀盐酸,氢离子的浓度增大,反应速率增大,铁少量且质量不变,生成氢气的量不变,符合题意。故选 $ {\rm \mathrm{C}} $ 。
4.等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间 $ (t) $ 内产生气体体积 $ {\rm (V)} $ 的变化情况如图,根据图示分析实验条件,下列说法中一定不正确的是( )
组别 | 对应曲线 | $ {\rm c(\mathrm{H}\mathrm{C}\mathrm{l})/(\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1})} $ | 反应温度/ $ ℃ $ | 铁的状态 |
1 | $ \mathrm{a} $ | | 30 | 粉末状 |
2 | $ \mathrm{b} $ | | 30 | 粉末状 |
3 | $ \mathrm{c} $ | 2.5 | | 块状 |
4 | $ \mathrm{d} $ | 2.5 | 30 | 块状 |
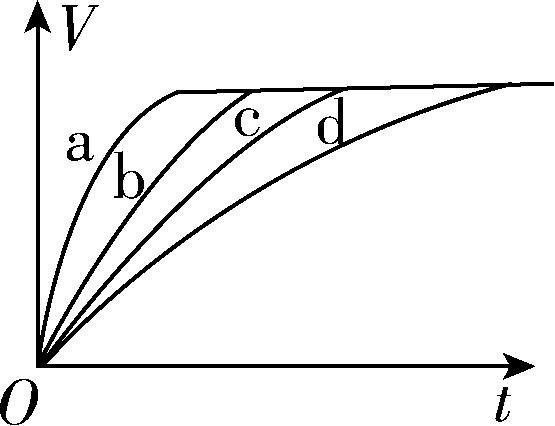
A. 第4组实验的反应速率最慢
B. 第1组实验中盐酸的浓度可能大于 $ {\rm 2.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
C. 第2组实验中盐酸的浓度可能等于 $ {\rm 2.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
D. 第3组实验的反应温度低于 $ 30℃ $
答案:D
解析:根据图像可知,产生相同体积气体,第4组实验所需时间最长,则第4组实验的反应速率最慢, $ {\rm \mathrm{A}} $ 正确;第1、2组与第4组相比较,由于铁的状态不同(使用粉末状铁反应速率大),不能判断其盐酸的浓度是否比第4组大,因此盐酸的浓度有可能大于、等于或小于 $ {\rm 2.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ {\rm \mathrm{B}} $ 、 $ {\rm \mathrm{C}} $ 正确;采用变量控制法分析反应条件,第3、4组比较,第3组生成氢气的速率较大,所以反应温度高于 $ 30℃ $ , $ {\rm \mathrm{D}} $ 错误。
5.A与B在容积为 $ {\rm 1\mathrm{L}} $ 的密闭容器中发生反应: $ {\rm a\mathrm{A}(\mathrm{g})+b\mathrm{B}(\mathrm{g})⇌c\mathrm{C}(\mathrm{g})+d\mathrm{D}(\mathrm{g})} $ , $ {t}_{1} $ 、 $ {t}_{2} \min $ 时分别测得部分数据如表:
反应时间/ $ \min $ | $ {\rm n(\mathrm{B})/\mathrm{m}\mathrm{o}\mathrm{l}} $ | $ {\rm n(\mathrm{C})/\mathrm{m}\mathrm{o}\mathrm{l}} $ | $ {\rm n(\mathrm{D})/\mathrm{m}\mathrm{o}\mathrm{l}} $ |
$ {t}_{1} $ | 0.12 | 0.06 | 0.10 |
$ {t}_{2} $ | 0.06 | 0.12 | 0.20 |
下列说法正确的是( )
A. $ 0\sim {t}_{1} \min $ ,平均反应速率 $ {\rm v(\mathrm{B})=\dfrac{0.04}{{t}_{1}}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
B. $ {t}_{2} \min $ 时, $ {\rm v(\mathrm{D})=\dfrac{0.20}{{t}_{2}}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
C. 升高温度时, $ {\rm v(\mathrm{B})} $ 、 $ {\rm v(\mathrm{C})} $ 、 $ {\rm v(\mathrm{D})} $ 均增大
D. $ b:d=5:3 $
答案:C
解析:从题表中数据可以得出, $ {t}_{1}\sim {t}_{2} \min $ , $ {\rm \mathrm{\Delta }n(\mathrm{B})=0.06\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm \mathrm{\Delta }n(\mathrm{C})=0.06\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm \mathrm{\Delta }n(\mathrm{D})=0.10\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm b:c:d=\mathrm{\Delta }n(\mathrm{B}):\mathrm{\Delta }n(\mathrm{C}):\mathrm{\Delta }n(\mathrm{D})=3:3:5} $ ,则 $ 0\sim {t}_{1} \min $ , $ {\rm \mathrm{\Delta }n(\mathrm{B})=\mathrm{\Delta }n(\mathrm{C})=0.06\mathrm{m}\mathrm{o}\mathrm{l}} $ ,所以 $ {\rm \mathrm{B}} $ 的起始量为 $ 0.12\mathrm{m}\mathrm{o}\mathrm{l}+0.06\mathrm{m}\mathrm{o}\mathrm{l}=0.18\mathrm{m}\mathrm{o}\mathrm{l} $ 。 $ 0\sim {t}_{1} \min $ ,平均反应速率 $ {\rm v(\mathrm{B})=\dfrac{\dfrac{0.06\mathrm{m}\mathrm{o}\mathrm{l}}{1\mathrm{L}}}{{t}_{1} \min }=\dfrac{0.06}{{t}_{1}}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ , $ {\rm \mathrm{A}} $ 错误; $ 0\sim {t}_{2} \min $ , $ {\rm v(\mathrm{D})=\dfrac{\dfrac{0.20\mathrm{m}\mathrm{o}\mathrm{l}}{1\mathrm{L}}}{{t}_{2} \min }=\dfrac{0.20}{{t}_{2}}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,但此速率为 $ 0\sim {t}_{2} \min $ 用物质 $ {\rm \mathrm{D}} $ 表示的平均反应速率,而不是 $ {t}_{2} \min $ 时用物质 $ {\rm \mathrm{D}} $ 表示的瞬时速率, $ {\rm \mathrm{B}} $ 错误;升高温度,反应速率加快,则 $ {\rm v(\mathrm{B})} $ 、 $ {\rm v(\mathrm{C})} $ 、 $ {\rm v(\mathrm{D})} $ 均增大, $ {\rm \mathrm{C}} $ 正确;由分析可知, $ b:d=3:5 $ , $ {\rm \mathrm{D}} $ 错误。
6.用 $ {\rm {\mathrm{N}\mathrm{a}}_{2}{\mathrm{F}\mathrm{e}\mathrm{O}}_{4}} $ 溶液氧化废水中的还原性污染物 $ {\rm \mathrm{M}} $ ,为研究降解效果设计如下对比实验探究温度、浓度、 $ {\rm \mathrm{p}\mathrm{H}} $ 对降解速率和效果的影响,实验测得 $ {\rm \mathrm{M}} $ 的浓度与时间的关系如图所示。
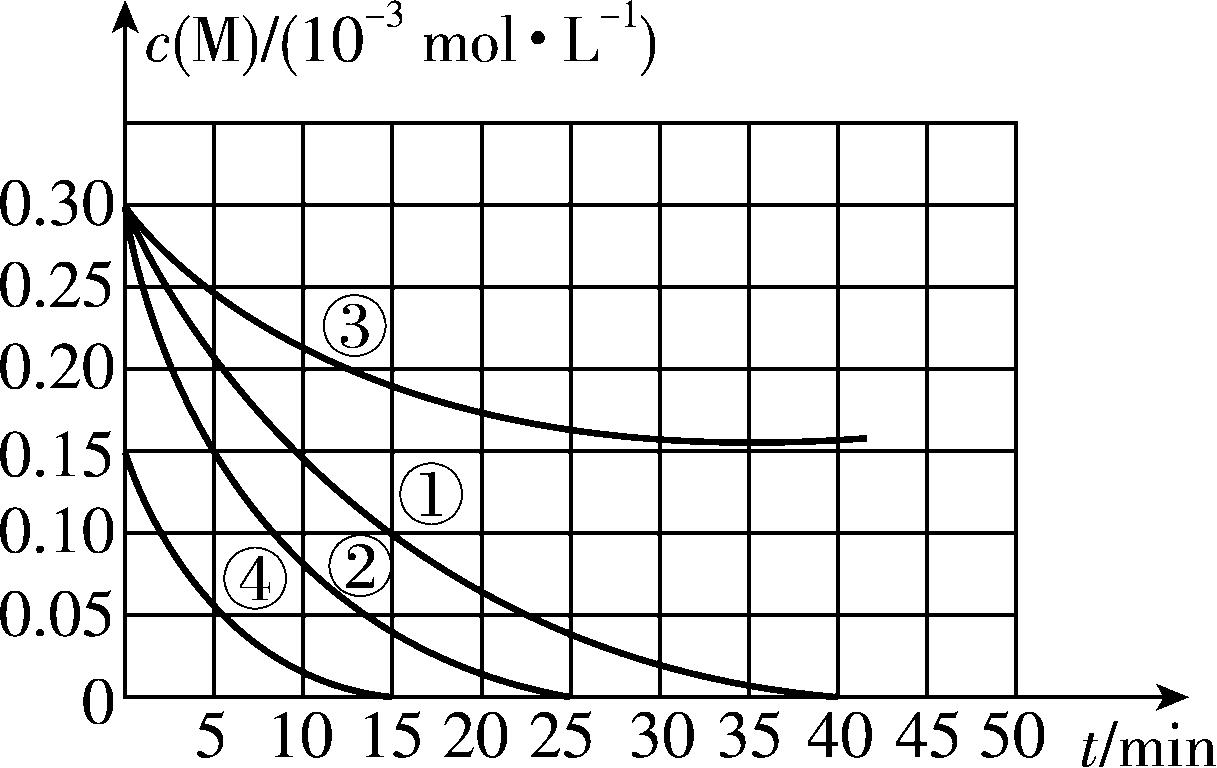
实验编号 | 温度/ $ ℃ $ | $ {\rm \mathrm{p}\mathrm{H}} $ |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |
下列说法错误的是( )
A. 实验①, $ 0\sim 15 \min $ , $ {\rm \mathrm{M}} $ 的降解速率约为 $ {\rm 1.33×{10}^{-2}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
B. 对比实验①④说明 $ {\rm \mathrm{M}} $ 的浓度越小, $ {\rm \mathrm{M}} $ 降解的速率越慢
C. 实验①③证明 $ {\rm \mathrm{p}\mathrm{H}} $ 越高,越不利于 $ {\rm \mathrm{M}} $ 的降解
D. 对比实验①②说明温度升高, $ {\rm \mathrm{M}} $ 降解速率加快
答案:A
解析:由图中数据,可知实验①中 $ 15 \min $ 内, $ {\rm \mathrm{\Delta }c(\mathrm{M})=(0.3-0.1)×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}=2×{10}^{-4}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 则 $ {\rm v(\mathrm{M})=\dfrac{\mathrm{\Delta }c(\mathrm{M})}{\mathrm{\Delta }t}=\dfrac{2×{10}^{-4}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}}{15 \min }\approx 1.33×{10}^{-5}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ , $ {\rm \mathrm{A}} $ 错误;实验①和实验④的反应温度相同、 $ {\rm \mathrm{p}\mathrm{H}} $ 相同,起始浓度不同, $ 0~15 \min $ 内,实验④中 $ {\rm \mathrm{M}} $ 的浓度变化量小于实验①中 $ {\rm \mathrm{M}} $ 的浓度变化量,说明 $ {\rm \mathrm{M}} $ 的浓度越小,降解的速率越慢, $ {\rm \mathrm{B}} $ 正确;由图表可看出,实验①③温度相同, $ {\rm \mathrm{M}} $ 的起始浓度相同,实验③的 $ {\rm \mathrm{p}\mathrm{H}} $ 高,相同时间内,实验③中 $ {\rm \mathrm{M}} $ 的浓度大,且充分反应后, $ {\rm \mathrm{M}} $ 的浓度仍大于 $ {\rm 1.5×{10}^{-4}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,说明 $ {\rm \mathrm{p}\mathrm{H}} $ 越高,越不利于 $ {\rm \mathrm{M}} $ 的降解, $ {\rm \mathrm{C}} $ 正确;根据图表信息可知,实验①②的单一变量是温度,实验②的温度 $ > $ 实验①,从曲线看,在相同时间内,曲线②的下降幅度大于曲线①的,故温度升高, $ {\rm \mathrm{M}} $ 的降解速率加快, $ {\rm \mathrm{D}} $ 正确。
7.某学习小组为测定化学反应速率,并探究外界条件对化学反应速率的影响,进行如下实验。
Ⅰ.甲同学利用图甲所示装置测定化学反应速率。
已知: $ {\rm 2{\mathrm{M}\mathrm{n}\mathrm{O}}_{4}^{-}+5{\mathrm{H}}_{2}{\mathrm{C}}_{2}{\mathrm{O}}_{4}+6{\mathrm{H}}^{+}\xlongequal{}2{\mathrm{M}\mathrm{n}}^{2+}+10{\mathrm{C}\mathrm{O}}_{2}↑+8{\mathrm{H}}_{2}\mathrm{O}} $
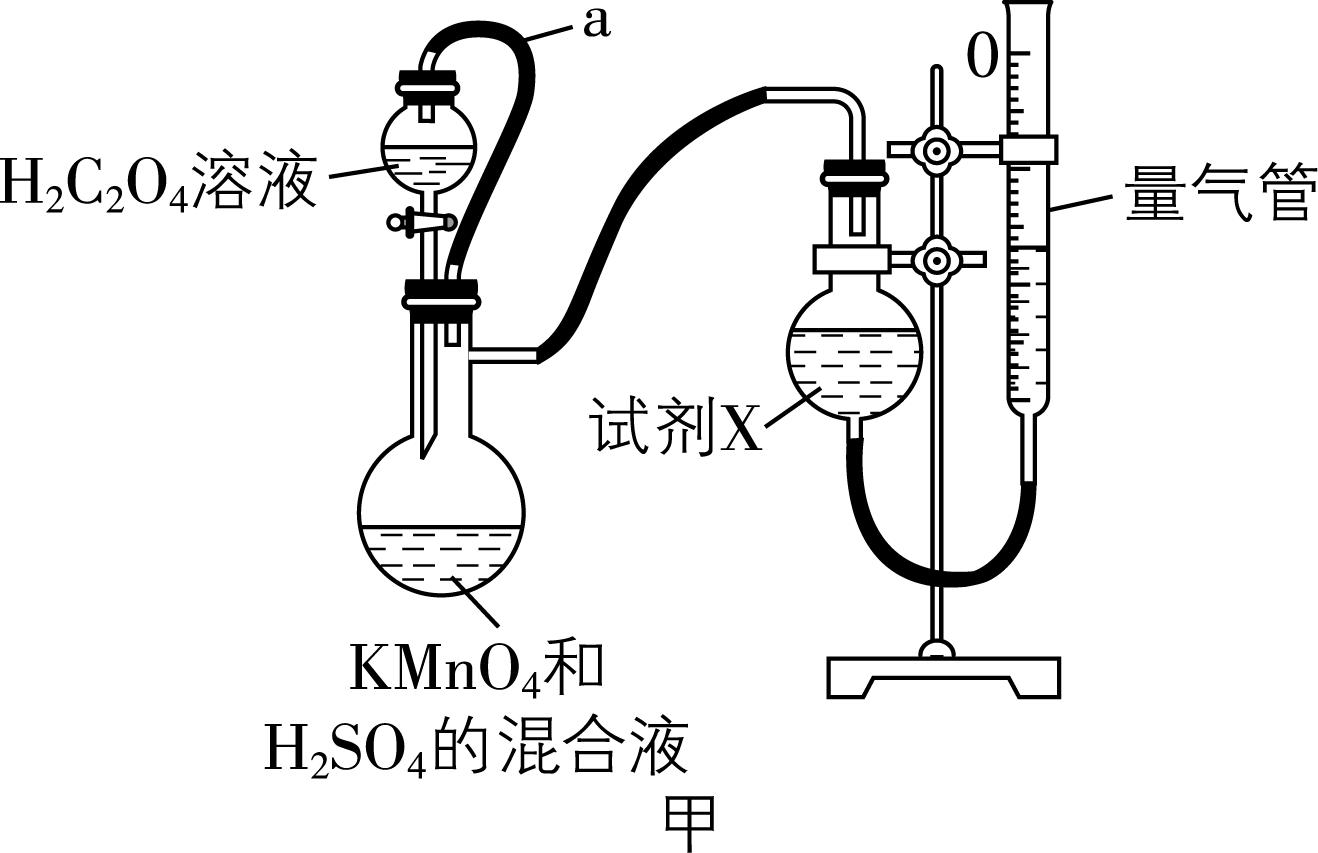
回答下列问题:
(1) 橡皮管 $ \mathrm{a} $ 除可以避免液体滴加引起气体体积测量误差外,另一个作用是 。
(2) 试剂 $ {\rm \mathrm{X}} $ 为 (填化学式)溶液;实验结束后的操作:ⅰ.恢复至室温;ⅱ.…… ,视线与量气管凹液面最低处相平,读取数据。“……”处的操作为 。
Ⅱ.乙同学设计如下实验探究外界条件对化学反应速率的影响。
编号 | $ {\rm 0.01\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 酸性 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液体积/ $ {\rm \mathrm{m}\mathrm{L}} $ | $ {\rm 0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{H}}_{2}{\mathrm{C}}_{2}{\mathrm{O}}_{4}} $ 溶液体积/ $ {\rm \mathrm{m}\mathrm{L}} $ | 水的体积/ $ {\rm \mathrm{m}\mathrm{L}} $ | 反应温度/ $ ℃ $ | 褪至无色所需时间/ $ \mathrm{s} $ |
1 | 5.0 | 5.0 | 0 | 20 | 125 |
2 | 5.0 | 4.0 | $ {\rm {V}_{1}} $ | 20 | 320 |
3 | $ {\rm {V}_{2}} $ | 5.0 | 0 | 50 | 30 |
(3) $ {\rm {V}_{1}=} $ ,实验1、3探究的是 对反应速率的影响。
(4) $ 0\sim 30\mathrm{s} $ 内,实验3用 $ {\rm {\mathrm{H}}_{2}{\mathrm{C}}_{2}{\mathrm{O}}_{4}} $ 表示的反应速率为 $ {\rm \mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ 。
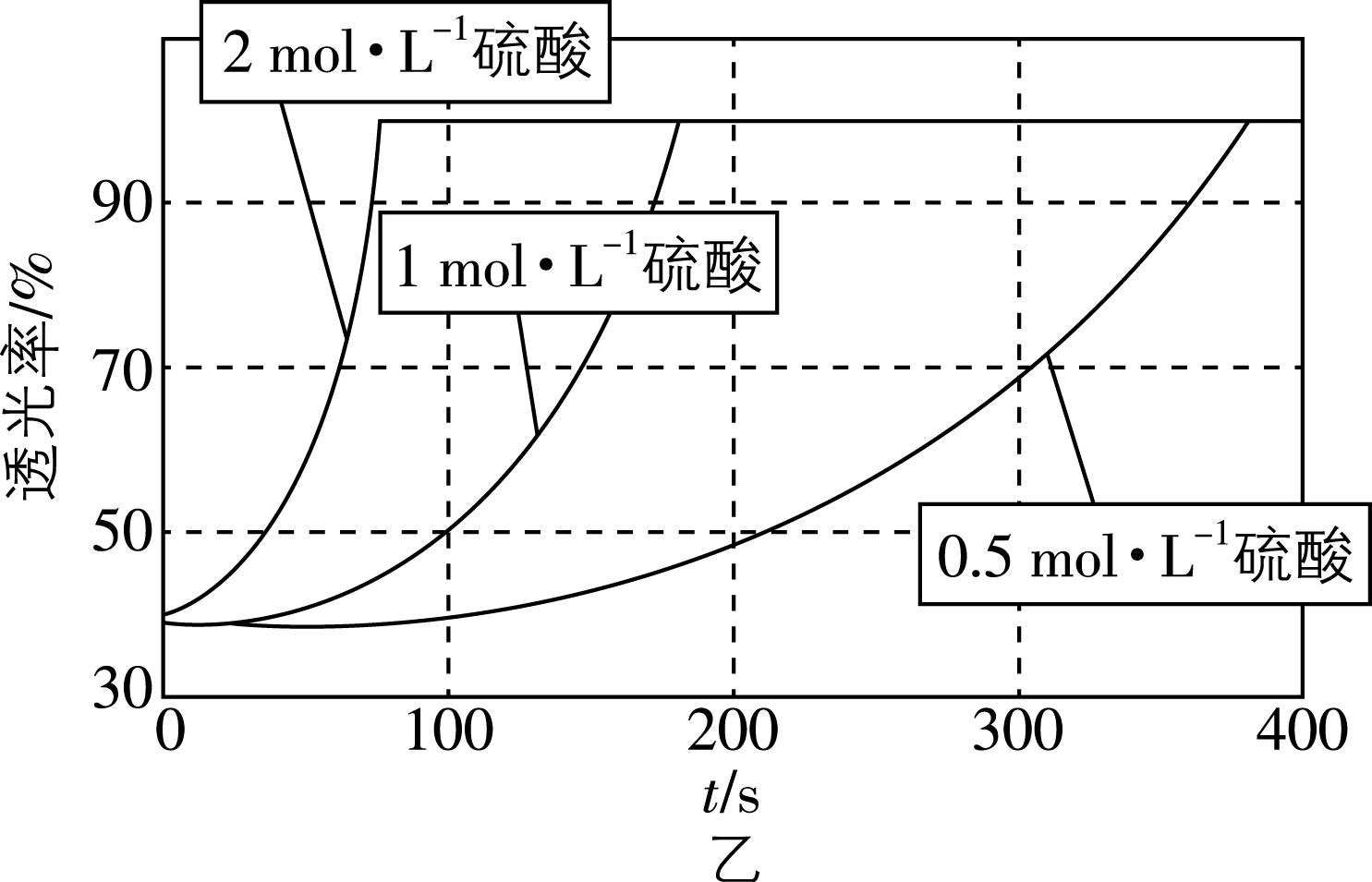
(5) 研究发现 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液的酸化程度对反应的速率也有较大影响,其他条件相同,用不同浓度的硫酸进行酸化,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图乙所示,由此得出的结论是 。
答案:(1) 平衡气压使液体顺利滴下
(2) $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ ;上下移动量气管,使左右两边液面相平
(3) 1.0;反应温度
(4) 0.025
(5) 在一定范围内,硫酸的浓度越大,化学反应速率越快
解析:(1) 橡皮管 $ \mathrm{a} $ 连通分液漏斗和蒸馏烧瓶,由分液漏斗向蒸馏烧瓶滴加液体时,会有等体积气体通过橡皮管 $ \mathrm{a} $ 进入分液漏斗,从而可以避免液体滴加引起气体体积测量误差,同时平衡气压使液体顺利滴下。
(2) 二氧化碳不溶于饱和 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶液,可通过排饱和 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶液的方法收集 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ ,则试剂 $ {\rm \mathrm{X}} $ 为饱和 $ {\rm {\mathrm{N}\mathrm{a}\mathrm{H}\mathrm{C}\mathrm{O}}_{3}} $ 溶液;反应前后,装置内的气体应处于同温同压下,则实验结束后,先恢复到室温,再上下移动量气管、使左右两边液面相平,然后视线与凹液面的最低处相平,读取数据。
(3) 实验1、2探究草酸溶液的浓度对化学反应速率的影响,根据实验1可知溶液的总体积 $ {\rm V=5.0\mathrm{m}\mathrm{L}+5.0\mathrm{m}\mathrm{L}=10.0\mathrm{m}\mathrm{L}} $ ,则 $ {\rm {V}_{1}=10.0-5.0-4.0=1.0} $ , $ {\rm {V}_{2}=10.0-5.0=5.0} $ ;实验1、3中除了反应温度不同,其余条件均相同,则探究的是反应温度对反应速率的影响。
(4) 溶液褪至无色时, $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 已完全反应,用时 $ 30\mathrm{s} $ , $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液的初始浓度为 $ {\rm c({\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4})=\dfrac{0.01\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}×5.0\mathrm{m}\mathrm{L}}{10.0\mathrm{m}\mathrm{L}}=0.005\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ ,则用 $ {\rm {\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4}} $ 溶液的浓度变化表示的化学反应速率 $ {\rm v({\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4})=\dfrac{0.005\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}}{0.5 \min }=0.010\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,用 $ {\rm {\mathrm{H}}_{2}{\mathrm{C}}_{2}{\mathrm{O}}_{4}} $ 表示的化学反应速率 $ {\rm v({\mathrm{H}}_{2}{\mathrm{C}}_{2}{\mathrm{O}}_{4})=\dfrac{5}{2}v({\mathrm{K}\mathrm{M}\mathrm{n}\mathrm{O}}_{4})=0.025\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ 。
(5) 由图乙可知,在一定范围内,硫酸的浓度越大,达到相同透光率所需的时间越短,表明反应速率越快。
8. $ {\rm {\mathrm{I}}^{-}} $ 可以作为水溶液中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 歧化反应的催化剂,可能的催化过程如下:
$ {\rm ⅰ.{\mathrm{S}\mathrm{O}}_{2}+4{\mathrm{I}}^{-}+4{\mathrm{H}}^{+}\xlongequal{}\mathrm{S}↓+2{\mathrm{I}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}} $ ;
$ {\rm ⅱ.{\mathrm{I}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}+{\mathrm{S}\mathrm{O}}_{2}\xlongequal{}{\mathrm{S}\mathrm{O}}_{4}^{2-}+4{\mathrm{H}}^{+}+2{\mathrm{I}}^{-}} $ 。
为探究ⅰ、ⅱ反应速率与 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 歧化反应速率的关系,进行如下实验:分别将 $ {\rm 18\mathrm{m}\mathrm{L}{\mathrm{S}\mathrm{O}}_{2}} $ 饱和溶液加入 $ {\rm 2\mathrm{m}\mathrm{L}} $ 下列试剂中,密闭放置,观察现象(已知: $ {\rm {\mathrm{I}}_{2}} $ 易溶解在 $ {\rm \mathrm{K}\mathrm{I}} $ 溶液中)。
序号 | 试剂组成 | 实验现象 |
Ⅰ | $ {\rm 0.4\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\mathrm{K}\mathrm{I}} $ | 溶液变黄,一段时间后出现浑浊 |
Ⅱ | $ {\rm a\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\mathrm{K}\mathrm{I}} $ 、 $ {\rm 0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ | 溶液变黄,出现浑浊较Ⅰ快 |
Ⅲ | $ {\rm 0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ | 无明显现象 |
Ⅳ | $ {\rm 0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\mathrm{K}\mathrm{I}} $ 、 $ {\rm 0.0002\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{I}}_{2}} $ | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较Ⅰ快 |
下列说法不正确的是( )
A. 水溶液中 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 歧化反应的化学方程式为 $ {\rm 3{\mathrm{S}\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{{\mathrm{I}}^{-}}\mathrm{S}↓+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $
B. Ⅱ是Ⅰ的对比实验,则 $ a=0.4 $
C. 比较Ⅰ、Ⅱ、Ⅲ可得出结论: $ {\rm {\mathrm{I}}^{-}} $ 是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 歧化反应的催化剂, $ {\rm {\mathrm{H}}^{+}} $ 单独存在时不具有催化作用,但有 $ {\rm {\mathrm{I}}^{-}} $ 存在时 $ {\rm {\mathrm{H}}^{+}} $ 可以加快 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 歧化反应的速率
D. 实验表明, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的歧化反应速率:Ⅳ $ > Ⅰ $ ,原因是反应ⅰ比ⅱ快,Ⅳ中由反应ⅱ产生的 $ {\rm {\mathrm{H}}^{+}} $ 使反应ⅰ加快
答案:D
解析: $ {\rm {\mathrm{I}}^{-}} $ 为催化剂,将 $ ⅰ+ⅱ×2 $ 消去 $ {\rm {\mathrm{I}}^{-}} $ 、 $ {\rm {\mathrm{I}}_{2}} $ ,可得反应的化学方程式: $ {\rm 3{\mathrm{S}\mathrm{O}}_{2}+2{\mathrm{H}}_{2}\mathrm{O}\xlongequal{{\mathrm{I}}^{-}}\mathrm{S}↓+2{\mathrm{H}}_{2}{\mathrm{S}\mathrm{O}}_{4}} $ , $ {\rm \mathrm{A}} $ 正确;Ⅱ是Ⅰ的对比实验,所用 $ {\rm c(\mathrm{K}\mathrm{I})} $ 应该相等,否则无法得出正确结论,故 $ a=0.4 $ , $ {\rm \mathrm{B}} $ 正确;比较Ⅰ、Ⅱ、Ⅲ可得出结论: $ {\rm {\mathrm{I}}^{-}} $ 是 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 歧化反应的催化剂, $ {\rm {\mathrm{H}}^{+}} $ 单独存在时不具有催化作用,但有 $ {\rm {\mathrm{I}}^{-}} $ 存在时 $ {\rm {\mathrm{H}}^{+}} $ 可以加快 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 歧化反应的速率, $ {\rm \mathrm{C}} $ 正确;实验表明, $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 的歧化反应速率:Ⅳ $ > Ⅰ $ ,结合Ⅰ、Ⅱ反应速率不同的原因(氢离子使反应速率加快),可知Ⅳ中由反应ⅱ产生的氢离子使反应速率加快,反应ⅱ比ⅰ快, $ {\rm \mathrm{D}} $ 错误。





