课时2 化学反应的限度
一、刷基础
1.观察图:对合成氨反应,下列叙述错误的是( )
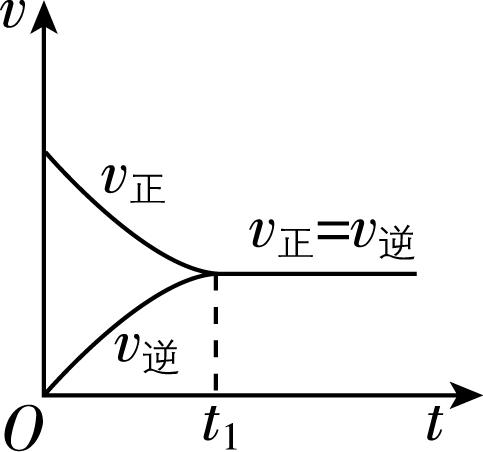
A. 开始反应时,正反应速率最大,逆反应速率为零
B. 随着反应的进行,正反应速率逐渐减小,逆反应速率逐渐增大
C. 反应到达 $ {t}_{1} $ 时,正反应速率与逆反应速率相等,反应停止
D. 反应在 $ {t}_{1} $ 之后,正反应速率与逆反应速率相等,反应达到化学平衡状态
答案:C
解析:反应开始时,反应物的浓度最大,正反应速率最大,生成物的浓度为零,逆反应速率为零, $ {\rm \mathrm{A}} $ 正确;随着反应的进行,反应物的浓度降低,则正反应速率逐渐减小,生成物的浓度增大,则逆反应速率逐渐增大, $ {\rm \mathrm{B}} $ 正确;反应到达 $ {t}_{1} $ 时,正反应速率与逆反应速率相等,但都不为零,反应没有停止, $ {\rm \mathrm{C}} $ 错误;反应在 $ {t}_{1} $ 之后,正反应速率与逆反应速率相等,反应达到化学平衡状态, $ {\rm \mathrm{D}} $ 正确。
2.下列过程与可逆反应无关的是( )
A. 高炉炼铁排放的尾气,随高炉的高度增加, $ {\rm \mathrm{C}\mathrm{O}} $ 的比例不变
B. 氯气溶于水,溶液中既存在 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 也存在 $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $
C. 铜和浓硫酸在加热条件下能反应,不加热不能反应
D. $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{O}}_{2}} $ 在接触室中反应生成 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $
答案:C
解析:高炉炼铁的尾气中 $ {\rm \mathrm{C}\mathrm{O}} $ 比例不变说明反应 $ {\rm \mathrm{C}+{\mathrm{C}\mathrm{O}}_{2}⇌2\mathrm{C}\mathrm{O}} $ 是可逆反应, $ {\rm \mathrm{A}} $ 不符合题意; $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $ 溶于水存在可逆反应: $ {\rm {\mathrm{C}\mathrm{l}}_{2}+{\mathrm{H}}_{2}\mathrm{O}⇌\mathrm{H}\mathrm{C}\mathrm{l}\mathrm{O}+{\mathrm{H}}^{+}+{\mathrm{C}\mathrm{l}}^{-}} $ ,溶液中既存在 $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 也存在 $ {\rm {\mathrm{C}\mathrm{l}}_{2}} $ , $ {\rm \mathrm{B}} $ 不符合题意;铜与浓硫酸在加热时反应生成 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 等产物,常温下不反应,与可逆反应无关, $ {\rm \mathrm{C}} $ 符合题意; $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 与 $ {\rm {\mathrm{O}}_{2}} $ 反应生成 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ 是典型的可逆反应: $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{△}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{D}} $ 不符合题意。
3.下列关于平衡状态和反应限度的说法正确的是( )
A. 一个可逆反应达到平衡状态后,这个反应在该条件下不再反应
B. 当一个可逆反应达到平衡状态时,正、逆反应速率相等
C. 平衡状态是一种静止的状态,反应物和生成物的浓度相等
D. 化学反应的限度不可以通过改变条件而改变
答案:B
解析:化学平衡是一个动态平衡,可逆反应在平衡状态时仍然继续进行反应,只不过正、逆反应速率相等, $ {\rm \mathrm{A}} $ 错误, $ {\rm \mathrm{B}} $ 正确;平衡状态是一种表面静止的状态,正、逆反应速率相等,各组分的浓度保持不变,但反应物和生成物的浓度不一定相等, $ {\rm \mathrm{C}} $ 错误;化学反应的限度可以通过改变条件而改变, $ {\rm \mathrm{D}} $ 错误。
4.在一定温度下,恒容的密闭容器中,可逆反应 $ {\rm \mathrm{X}(\mathrm{g})+3\mathrm{Y}(\mathrm{g})⇌2\mathrm{Z}(\mathrm{g})} $ 达到平衡的标志是( )
A. 气体总质量保持不变
B. $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Y}} $ 、 $ {\rm \mathrm{Z}} $ 的浓度都相等
C. 容器内压强不再发生变化
D. $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Y}} $ 、 $ {\rm \mathrm{Z}} $ 的分子数之比为 $ 1:3:2 $
答案:C
解析:反应前后全是气体,气体总质量是恒量,气体总质量保持不变,反应不一定平衡, $ {\rm \mathrm{A}} $ 不符合题意; $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Y}} $ 、 $ {\rm \mathrm{Z}} $ 的浓度都相等,不能判断浓度是否还发生改变,反应不一定平衡, $ {\rm \mathrm{B}} $ 不符合题意;该反应为反应前后气体分子数发生变化的反应,气体总物质的量是变量,压强是变量,容器内压强不再发生变化,反应一定达到平衡状态, $ {\rm \mathrm{C}} $ 符合题意; $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Y}} $ 、 $ {\rm \mathrm{Z}} $ 的分子数之比为 $ 1:3:2 $ ,不能判断各物质浓度是否还发生改变,反应不一定平衡, $ {\rm \mathrm{D}} $ 不符合题意。
5.可逆反应 $ {\rm 2{\mathrm{N}\mathrm{O}}_{2}(\mathrm{g})} $ (红棕色) $ {\rm ⇌2\mathrm{N}\mathrm{O}(\mathrm{g})} $ (无色) $ {\rm +{\mathrm{O}}_{2}(\mathrm{g})} $ ,在容积固定的密闭容器中达到平衡状态的标志是( )
①单位时间内生成 $ {\rm n\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}} $ 的同时生成 $ {\rm 2n\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}\mathrm{O}}_{2}} $ ②单位时间内生成 $ {\rm n\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}} $ 的同时生成 $ {\rm 2n\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}} $ ③用 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 、 $ {\rm \mathrm{N}\mathrm{O}} $ 、 $ {\rm {\mathrm{O}}_{2}} $ 表示的反应速率之比为 $ 2:2:1 $ 的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的压强不再改变的状态 ⑦混合气体的平均相对分子质量不再改变的状态
A. ①④⑥⑦
B. ②③⑤⑦
C. ①③④⑤
D. ①②③④⑤⑥⑦
答案:A
解析:①单位时间内生成 $ {\rm n\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}} $ 的同时生成 $ {\rm 2n\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}\mathrm{O}}_{2}} $ ,正、逆反应速率相等,说明反应已达到平衡状态。②生成 $ {\rm {\mathrm{O}}_{2}} $ 和生成 $ {\rm \mathrm{N}\mathrm{O}} $ 都是正反应方向,单位时间内生成 $ {\rm n\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{O}}_{2}} $ 必生成 $ {\rm 2n\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{N}\mathrm{O}} $ ,不能判断正、逆反应速率是否相等,不能说明反应达到平衡状态。③中无论达到平衡与否,用各物质表示的化学反应速率之比都等于化学计量数之比,所以 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 、 $ {\rm \mathrm{N}\mathrm{O}} $ 、 $ {\rm {\mathrm{O}}_{2}} $ 表示的反应速率之比为 $ 2:2:1 $ 的状态不一定是平衡状态。 $ {\rm ④{\mathrm{N}\mathrm{O}}_{2}} $ 为红棕色气体,其余为无色气体,混合气体的颜色不变,则表示 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的浓度不再变化,说明反应已达到平衡状态。⑤容器容积固定、反应前后气体质量守恒,气体密度始终不变,混合气体的密度不再改变不一定是平衡状态。⑥反应后气体的物质的量增大,压强是变量,压强不变,意味着各物质的含量不再变化,说明已达到平衡状态。⑦由于气体的质量不变,反应后气体分子数增多,平均相对分子质量减小,气体的平均相对分子质量不变,说明气体中各物质的物质的量不变,反应已达到平衡状态。①④⑥⑦达到平衡状态,选 $ {\rm \mathrm{A}} $ 。
6.硫酸是一种重要的化工产品,目前硫酸的主要生产方法是“接触法”,其主要反应之一为 $ {\rm 2{\mathrm{S}\mathrm{O}}_{2}+{\mathrm{O}}_{2}\stackrel{催化剂}{\underset{△}{⇌}}2{\mathrm{S}\mathrm{O}}_{3}} $ 。下列有关该反应的说法不正确的是( )
A. $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{O}}_{2}} $ 不可能全部转化为 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $
B. 反应达到平衡后,正、逆反应速率相等且均为0
C. 该反应从开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D. 工业上生产 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ 时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
答案:B
解析:该反应为可逆反应,反应物的转化率 $ < 100\% $ ,故 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{O}}_{2}} $ 不可能全部转化为 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ , $ {\rm \mathrm{A}} $ 正确;反应达到平衡后,正、逆反应速率相等,化学平衡是一种动态平衡,反应速率不可能为 $ {\rm 0, \mathrm{B}} $ 错误;该反应从开始到平衡的过程中,反应物浓度不断减小,生成物浓度不断增大,故正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等,达到平衡状态, $ {\rm \mathrm{C}} $ 正确;工业上生产 $ {\rm {\mathrm{S}\mathrm{O}}_{3}} $ 时,要考虑转化率及反应时间,即同时考虑反应所能达到的限度和化学反应速率两方面的问题, $ {\rm \mathrm{D}} $ 正确。
7.对于可逆反应 $ {\rm 4{\mathrm{N}\mathrm{H}}_{3}+5{\mathrm{O}}_{2}⇌4\mathrm{N}\mathrm{O}+6{\mathrm{H}}_{2}\mathrm{O}} $ ,下列叙述正确的是( )
A. 加入催化剂,可以加快反应速率并增大反应限度
B. 保持容器内气体压强不变,向其中加入 $ {\rm \mathrm{H}\mathrm{e}} $ ,化学反应速率不变
C. 保持容器容积不变,向其中加入 $ {\rm \mathrm{H}\mathrm{e}} $ ,化学反应速率增大
D. 达到化学平衡时, $ {\rm 4{v}_{正}({\mathrm{O}}_{2})=5{v}_{逆}(\mathrm{N}\mathrm{O})} $
答案:D
解析:催化剂能加快反应速率,但不能改变反应限度, $ {\rm \mathrm{A}} $ 错误;恒压下,充入 $ {\rm \mathrm{H}\mathrm{e}} $ ,容器容积增大,反应物浓度降低,化学反应速率减小, $ {\rm \mathrm{B}} $ 错误;恒容下,充入 $ {\rm \mathrm{H}\mathrm{e}} $ ,反应物浓度不变,化学反应速率不变, $ {\rm \mathrm{C}} $ 错误;平衡时,正、逆反应速率之比等于化学计量数之比,则达到化学平衡时, $ {\rm 4{v}_{正}({\mathrm{O}}_{2})=5{v}_{逆}(\mathrm{N}\mathrm{O})} $ , $ {\rm \mathrm{D}} $ 正确。
二、刷提升
1.一定温度下,在容积恒为 $ {\rm 2\mathrm{L}} $ 的刚性密闭容器中发生反应: $ {\rm 3\mathrm{A}(\mathrm{g})+\mathrm{B}(\mathrm{s})⇌3\mathrm{C}(\mathrm{g})} $ 。开始时加入 $ {\rm 4\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{A}} $ 、 $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{B}} $ ,反应在 $ 2 \min $ 末恰好达到平衡状态,测得平衡时B的物质的量为 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ 。下列说法正确的是( )
A. 当 $ 3{v}_{正} {\rm (A)} $ $ =4{v}_{逆} {\rm (C)} $ 时,反应达到平衡状态
B. $ 2 \min $ 末,C的浓度为 $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $
C. 当容器中的压强不再变化时,反应达到平衡状态
D. 当混合气体的平均摩尔质量不再变化时,反应达到平衡状态
答案:D
解析:平衡时,不同物质表示的正、逆反应速率比等于化学计量数比,根据反应式, $ {\rm 3{v}_{正}(\mathrm{A})=4{v}_{逆}(\mathrm{C})} $ 不满足 $ {v}_{正}={v}_{逆} $ ,反应不平衡, $ {\rm \mathrm{A}} $ 错误; $ 2 \min $ 末平衡时 $ {\rm \mathrm{B}} $ 的物质的量为 $ 2\mathrm{m}\mathrm{o}\mathrm{l} $ ,则消耗 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{B}} $ 、生成 $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}\mathrm{C}} $ , $ {\rm \mathrm{C}} $ 的浓度为 $ {\rm \dfrac{3\mathrm{m}\mathrm{o}\mathrm{l}}{2\mathrm{L}}=1.5\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ , $ {\rm \mathrm{B}} $ 错误;反应前后气体总物质的量均为 $ 4\mathrm{m}\mathrm{o}\mathrm{l} $ ,压强始终不变,不能作为平衡标志, $ {\rm \mathrm{C}} $ 错误;混合气体的平均摩尔质量 $ {\rm \bar{M}=\dfrac{m}{n}} $ ,反应前后气体总物质的量不变,但是气体的质量随反应进行而改变,所以 $ {\rm \bar{M}} $ 会发生改变,当 $ {\rm \bar{M}} $ 不变时,反应达到平衡, $ {\rm \mathrm{D}} $ 正确。
2.在恒温恒容容器中加入一定量的氮气和氢气,发生反应 $ {\rm {\mathrm{N}}_{2}(\mathrm{g})+3{\mathrm{H}}_{2}(\mathrm{g})⇌2{\mathrm{N}\mathrm{H}}_{3}(\mathrm{g})} $ ,可以证明反应已达到平衡状态的是( )
①1个 $ {\rm \mathrm{N}\equiv \mathrm{N}} $ 断裂的同时,有3个 $ {\rm \mathrm{H}—\mathrm{H}} $ 键断裂
② 1个 $ {\rm \mathrm{N}\equiv \mathrm{N}} $ 断裂的同时,有6个 $ {\rm \mathrm{N}—\mathrm{H}} $ 键断裂
$ {\rm ③{\mathrm{N}\mathrm{H}}_{3}} $ 、 $ {\rm {\mathrm{N}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 的物质的量百分含量都不再改变
④气体密度保持不变 ⑤混合气体平均相对分子质量不再改变 ⑥体系压强不再改变 ⑦正反应速率 $ {\rm v({\mathrm{N}}_{2})=0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,逆反应速率 $ {\rm v({\mathrm{N}\mathrm{H}}_{3})=0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
A. 全部
B. 只有②③④⑤
C. 只有①③④⑤⑦
D. 只有②③⑤⑥⑦
答案:D
解析:①无论反应是否达到平衡状态,消耗 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ 的同时都会消耗 $ {\rm 3\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{H}}_{2}} $ ,即1个 $ {\rm \mathrm{N}\equiv \mathrm{N}} $ 断裂的同时,有3个 $ {\rm \mathrm{H}—\mathrm{H}} $ 断裂,不能说明反应已达到平衡状态,错误; $ ②1 $ 个 $ {\rm \mathrm{N}\equiv \mathrm{N}} $ 断裂的同时,有6个 $ {\rm \mathrm{N}—\mathrm{H}} $ 断裂,即消耗 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}}_{2}} $ 的同时消耗 $ {\rm 2\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}\mathrm{H}}_{3}} $ ,正、逆反应速率相等,说明反应已达到平衡状态,正确;③反应中各组分的浓度保持不变,说明反应达到平衡状态,故 $ {\rm {\mathrm{N}\mathrm{H}}_{3}} $ 、 $ {\rm {\mathrm{N}}_{2}} $ 、 $ {\rm {\mathrm{H}}_{2}} $ 的物质的量百分含量都不再改变,说明反应已达到平衡状态,正确;④该反应的反应物和产物全部为气体,依据质量守恒定律,气体的总质量一直不变,恒容容器中,气体总体积不变,则气体密度一直不变,气体密度保持不变,不能说明反应已达到平衡状态,错误;⑤依据质量守恒定律,气体的总质量一直不变,该反应为气体分子数变化的反应,反应达到平衡时,气体分子数不再改变,气体总物质的量不再改变,则混合气体平均相对分子质量不再改变,说明反应已达到平衡状态,正确;⑥该反应为气体分子数变化的反应,恒温恒容条件下,压强与气体分子数成正比,反应达到平衡时,气体分子数不再改变,则体系压强不再改变说明反应已达到平衡状态,正确;⑦同一反应,相同时间内不同物质的化学反应速率之比等于相应的化学计量数之比,正反应速率 $ {\rm v({\mathrm{N}}_{2})=0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,即正反应速率 $ {\rm v({\mathrm{N}\mathrm{H}}_{3})=0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,而逆反应速率 $ {\rm v({\mathrm{N}\mathrm{H}}_{3})=0.2\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ ,正、逆反应速率相等,说明反应已达到平衡状态,正确。选 $ {\rm \mathrm{D}} $ 。
3.已知汽车尾气无害化处理反应为 $ {\rm 2\mathrm{N}\mathrm{O}(\mathrm{g})+2\mathrm{C}\mathrm{O}(\mathrm{g})⇌{\mathrm{N}}_{2}(\mathrm{g})+2{\mathrm{C}\mathrm{O}}_{2}(\mathrm{g})} $ 。下列说法不正确的是( )
A. 升高温度可使该反应的逆反应速率降低
B. 使用高效催化剂可有效提高反应速率
C. 反应达到平衡后, $ {\rm \mathrm{N}\mathrm{O}} $ 的反应速率保持恒定
D. 单位时间内消耗 $ {\rm \mathrm{C}\mathrm{O}} $ 和消耗 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 的物质的量相等时,反应达到平衡
答案:A
解析:对于可逆反应,升高温度使正、逆反应速率都增大, $ {\rm \mathrm{A}} $ 错误;使用高效催化剂可增大反应速率, $ {\rm \mathrm{B}} $ 正确;反应达到平衡后,正、逆反应速率相等且不变,所以反应达到平衡后, $ {\rm \mathrm{N}\mathrm{O}} $ 的反应速率保持恒定, $ {\rm \mathrm{C}} $ 正确;由 $ {\rm 2\mathrm{N}\mathrm{O}(\mathrm{g})+2\mathrm{C}\mathrm{O}(\mathrm{g})⇌{\mathrm{N}}_{2}(\mathrm{g})+2{\mathrm{C}\mathrm{O}}_{2}(\mathrm{g})} $ 可知,单位时间内消耗 $ {\rm \mathrm{C}\mathrm{O}} $ 和消耗 $ {\rm {\mathrm{C}\mathrm{O}}_{2}} $ 的物质的量相等时,正、逆反应速率相等,反应达到平衡, $ {\rm \mathrm{D}} $ 正确。
4.某温度时,在 $ {\rm 2\mathrm{L}} $ 的恒容密闭容器中,A、B、C三种无色气体的物质的量随时间的变化曲线如图所示。下列说法正确的是( )
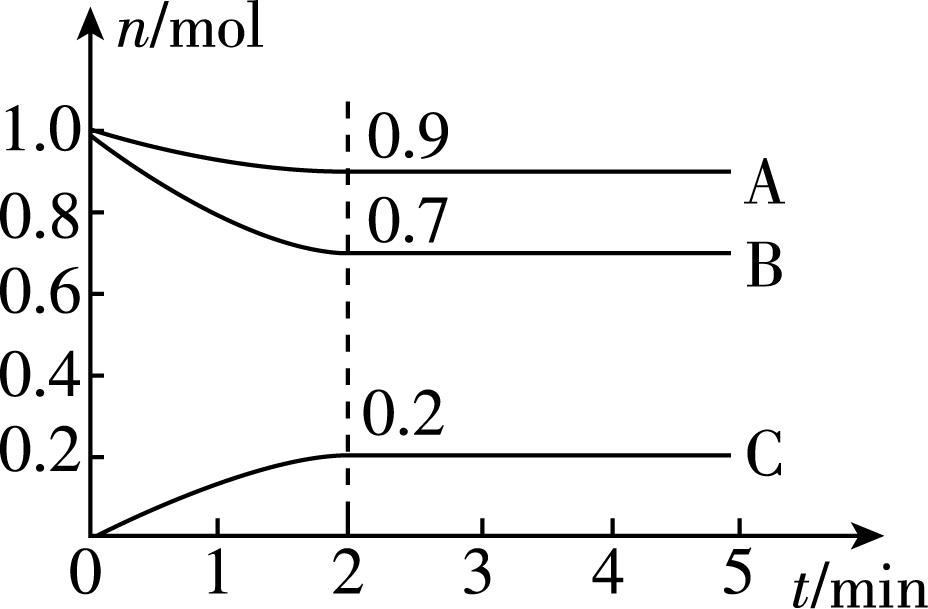
A. 反应从开始至 $ 2 \min $ 末,B的转化率为 $ {\rm \alpha (\mathrm{B})=70\%} $
B. 用C的浓度变化表示 $ 0\sim 2 \min $ 内的平均反应速率为 $ {\rm v(\mathrm{C})=0.1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
C. 由图中所给数据进行分析,该反应的化学方程式为 $ {\rm \mathrm{A}(\mathrm{g})+3\mathrm{B}(\mathrm{g})\xlongequal{}2\mathrm{C}(\mathrm{g})} $
D. 平衡时体系的压强是开始时的 $ \dfrac{9}{10} $
答案:D
解析:反应从开始至 $ 2 \min $ 末, $ {\rm \mathrm{B}} $ 的转化率 $ {\rm \alpha (\mathrm{B})=\dfrac{(1.0-0.7)\mathrm{m}\mathrm{o}\mathrm{l}}{1.0\mathrm{m}\mathrm{o}\mathrm{l}}×100\%=30\%} $ , $ {\rm \mathrm{A}} $ 错误;用 $ {\rm \mathrm{C}} $ 的浓度变化表示 $ 0\sim 2 \min $ 内的平均反应速率 $ {\rm v(\mathrm{C})=\dfrac{0.2\mathrm{m}\mathrm{o}\mathrm{l}}{2\mathrm{L}×2 \min }=0.05\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ , $ {\rm \mathrm{B}} $ 错误;根据图像, $ 0\sim 2 \min $ 内 $ {\rm \mathrm{A}} $ 、 $ {\rm \mathrm{B}} $ 、 $ {\rm \mathrm{C}} $ 三种气体的变化量分别为 $ 0.1\mathrm{m}\mathrm{o}\mathrm{l} $ 、 $ 0.3\mathrm{m}\mathrm{o}\mathrm{l} $ 和 $ 0.2\mathrm{m}\mathrm{o}\mathrm{l} $ ,则三者化学计量数之比为 $ 1:3:2 $ , $ 2 \min $ 末反应达到平衡时 $ {\rm \mathrm{A}} $ 、 $ {\rm \mathrm{B}} $ 、 $ {\rm \mathrm{C}} $ 三种气体同时存在,说明该反应为可逆反应,因此反应的化学方程式为 $ {\rm \mathrm{A}(\mathrm{g})+3\mathrm{B}(\mathrm{g})⇌2\mathrm{C}(\mathrm{g})} $ , $ {\rm \mathrm{C}} $ 错误;恒温恒容条件下,气体的压强之比等于物质的量之比,故 $ \dfrac{{p}_{平}}{{p}_{始}}=\dfrac{(0.9+0.7+0.2)\mathrm{m}\mathrm{o}\mathrm{l}}{(1+1)\mathrm{m}\mathrm{o}\mathrm{l}}=\dfrac{9}{10} $ , $ {\rm \mathrm{D}} $ 正确。
5.利用 $ {\rm {\mathrm{C}\mathrm{H}}_{4}(\mathrm{g})+2{\mathrm{N}\mathrm{O}}_{2}(\mathrm{g})⇌{\mathrm{N}}_{2}(\mathrm{g})+{\mathrm{C}\mathrm{O}}_{2}(\mathrm{g})+2{\mathrm{H}}_{2}\mathrm{O}(\mathrm{g})} $ 可消除 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的污染。在 $ {\rm 1\mathrm{L}} $ 的密闭容器中,控制不同温度,分别加入 $ {\rm 0.50\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{C}\mathrm{H}}_{4}(\mathrm{g})} $ 和 $ {\rm 1.00\mathrm{m}\mathrm{o}\mathrm{l}{\mathrm{N}\mathrm{O}}_{2}(\mathrm{g})} $ 进行上述反应,测得 $ {\rm n({\mathrm{C}\mathrm{H}}_{4})} $ (单位: $ \mathrm{m}\mathrm{o}\mathrm{l} $ )随时间变化的实验数据如表。下列说法错误的是( )
实验 | 温度 | $ 0 \min $ | $ 10 \min $ | $ 20 \min $ | $ 40 \min $ | $ 50 \min $ |
① | $ {\rm {T}_{1}} $ | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | $ {\rm {T}_{2}} $ | 0.50 | 0.30 | 0.18 | $ x $ | 0.15 |
A. 由实验数据可知,该反应在 $ 40 \min $ 时已达到平衡状态
B. 由实验数据可知温度: $ {\rm {T}_{1} > {T}_{2}} $
C. 实验②中, $ 0\sim 10 \min $ 内, $ {\rm {\mathrm{C}\mathrm{H}}_{4}} $ 的反应速率为 $ {\rm 0.02\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $
D. 表格中 $ x $ 为0.15
答案:B
解析:根据表格数据可知: $ 0~10 \min $ , $ {\rm {T}_{2}} $ 温度下 $ {\rm \mathrm{\Delta }n({\mathrm{C}\mathrm{H}}_{4})} $ 比 $ {\rm {T}_{1}} $ 温度下大,说明实验②中反应速率快; $ {\rm {T}_{1}} $ 温度下, $ {\rm {n}_{40 \min }({\mathrm{C}\mathrm{H}}_{4})={n}_{50 \min }({\mathrm{C}\mathrm{H}}_{4})} $ ,则实验①在 $ 40 \min $ 时已经达到平衡状态,实验②达到平衡状态所需时间小于 $ 40 \min $ ,故在 $ 40 \min $ 时,实验②中反应也已达平衡状态, $ {\rm \mathrm{A}} $ 正确;由 $ {\rm \mathrm{A}} $ 项分析知, $ {\rm {T}_{2}} $ 时反应速率快,其他外界条件相同,温度越高,反应速率越快,则温度: $ {\rm {T}_{2} > {T}_{1}} $ , $ {\rm \mathrm{B}} $ 错误;实验②中, $ 0~10 \min $ 内, $ {\rm \mathrm{\Delta }n({\mathrm{C}\mathrm{H}}_{4})=0.50\mathrm{m}\mathrm{o}\mathrm{l}-0.30\mathrm{m}\mathrm{o}\mathrm{l}=0.20\mathrm{m}\mathrm{o}\mathrm{l}} $ ,容器的容积是 $ {\rm 1\mathrm{L}} $ ,所以 $ {\rm v({\mathrm{C}\mathrm{H}}_{4})=\dfrac{0.20}{1×10}\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}=0.02\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\cdot { \min }^{-1}} $ , $ {\rm \mathrm{C}} $ 正确;由 $ {\rm \mathrm{A}} $ 项分析可知,该反应在 $ 40 \min $ 时已达到平衡状态, $ {\rm n({\mathrm{C}\mathrm{H}}_{4})} $ 与 $ 50 \min $ 时相同,即 $ x $ 为 $ 0.15 $ , $ {\rm \mathrm{D}} $ 正确。
6.一定温度下,在 $ {\rm 2\mathrm{L}} $ 的恒容密闭容器中,固体A、三种气态物质 $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Y}} $ 、 $ {\rm \mathrm{Z}} $ 的物质的量随时间变化曲线如图所示:
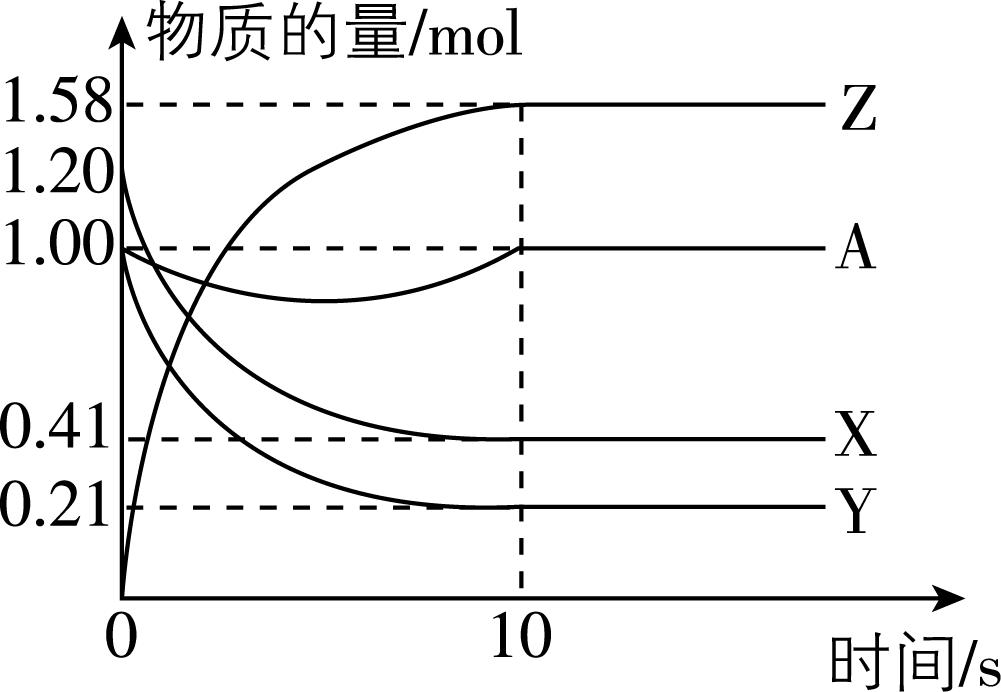
(1) 该反应的化学方程式是 。
(2) 平衡时容器内气体压强与初始时之比为 。
(3) 反应进行到 $ 5\mathrm{s} $ 时 $ {\rm {v}_{正}(\mathrm{Z})} $ (填“ $ > $ ”“ $ < $ ”或“ $ = $ ”) $ 10\mathrm{s} $ 时 $ {\rm {v}_{逆}(\mathrm{Z})} $ 。
(4) 如该反应改为在恒容绝热密闭容器中进行,该反应达到平衡状态的标志是 (填序号)。
A. $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Z}} $ 的反应速率比为 $ 1:2 $
B. 容器内混合气体的压强保持不变
C. 容器内混合气体的密度保持不变
D. 容器内温度保持不变
答案:(1) $ {\rm \mathrm{Y}(\mathrm{g})+\mathrm{X}(\mathrm{g})\stackrel{\mathrm{A}}{⇌}2\mathrm{Z}(\mathrm{g})} $
(2) $ 1:1 $
(3) $ > $
(4) BD
解析:(1) 由题图知, $ {\rm \mathrm{A}} $ 在反应过程中先减少后增加,而在反应前后,质量并没有损耗,因此 $ {\rm \mathrm{A}} $ 是反应的催化剂;随着反应的进行, $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Y}} $ 物质的量逐渐减小,为反应物;物质的量逐渐增大的 $ {\rm \mathrm{Z}} $ 是生成物;该反应为可逆反应,同一反应中,参与反应的 $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Y}} $ 、 $ {\rm \mathrm{Z}} $ 的化学计量数之比等于其物质的量的变化量之比,为 $ 0.79:0.79:1.58=1:1:2 $ ,则反应的化学方程式为 $ {\rm \mathrm{Y}(\mathrm{g})+\mathrm{X}(\mathrm{g})\stackrel{\mathrm{A}}{⇌}2\mathrm{Z}(\mathrm{g})} $ 。
(2) 由 $ {\rm pV=nRT} $ 可知,同温、同体积的条件下,气体物质的量之比等于压强之比,平衡时容器内气体压强与初始时之比为 $ 1:1 $ 。
(3) 由题图可知, $ 5\mathrm{s} $ 时反应未达到平衡,正反应速率大于逆反应速率, $ 10\mathrm{s} $ 时反应达到平衡,正、逆反应速率相等,随着反应的进行,反应物浓度不断减小,生成物浓度不断增大,达到平衡时 $ {\rm {v}_{正}(\mathrm{Z})} $ 最小、 $ {\rm {v}_{逆}(\mathrm{Z})} $ 最大,所以 $ 5\mathrm{s} $ 时 $ {\rm \mathrm{Z}} $ 的正反应速率大于 $ 10\mathrm{s} $ 时 $ {\rm \mathrm{Z}} $ 的逆反应速率。
(4) 没有说明反应进行的方向, $ {\rm \mathrm{X}} $ 、 $ {\rm \mathrm{Z}} $ 的反应速率比为 $ 1:2 $ 不能说明正、逆反应速率相等,无法判断反应是否达到平衡状态, $ {\rm \mathrm{A}} $ 错误;反应前后容器内气体总物质的量不变,反应时绝热容器中温度会发生改变,压强会发生改变,则容器内压强保持不变能说明反应已达到平衡状态, $ {\rm \mathrm{B}} $ 正确;由质量守恒定律可知,反应前后容器内气体的总质量保持不变,体积不变,则恒容密闭容器中混合气体的密度始终不变,不能根据混合气体的密度保持不变判断反应是否达到平衡状态, $ {\rm \mathrm{C}} $ 错误;在绝热容器中反应时,容器内温度会发生改变,则容器内温度保持不变说明反应达到平衡状态, $ {\rm \mathrm{D}} $ 正确。
7.某兴趣小组设计以下两种方案,验证 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 与 $ {\rm {\mathrm{I}}^{-}} $ 发生的反应为可逆反应。
方案 | 实验操作及现象 |
方案一 | ①向 $ {\rm 5\mathrm{m}\mathrm{L}1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\mathrm{K}\mathrm{I}} $ 溶液中,加入 $ {\rm 10\mathrm{m}\mathrm{L}1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ $ {\rm \mathrm{F}\mathrm{e}\mathrm{C}{\mathrm{l}}_{3}} $ 溶液,充分反应后加入 $ {\rm 5\mathrm{m}\mathrm{L}{\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ ,振荡静置; ②取上层清液于试管中,加入3滴试剂 $ {\rm \mathrm{X}} $ ,溶液变为红色 |
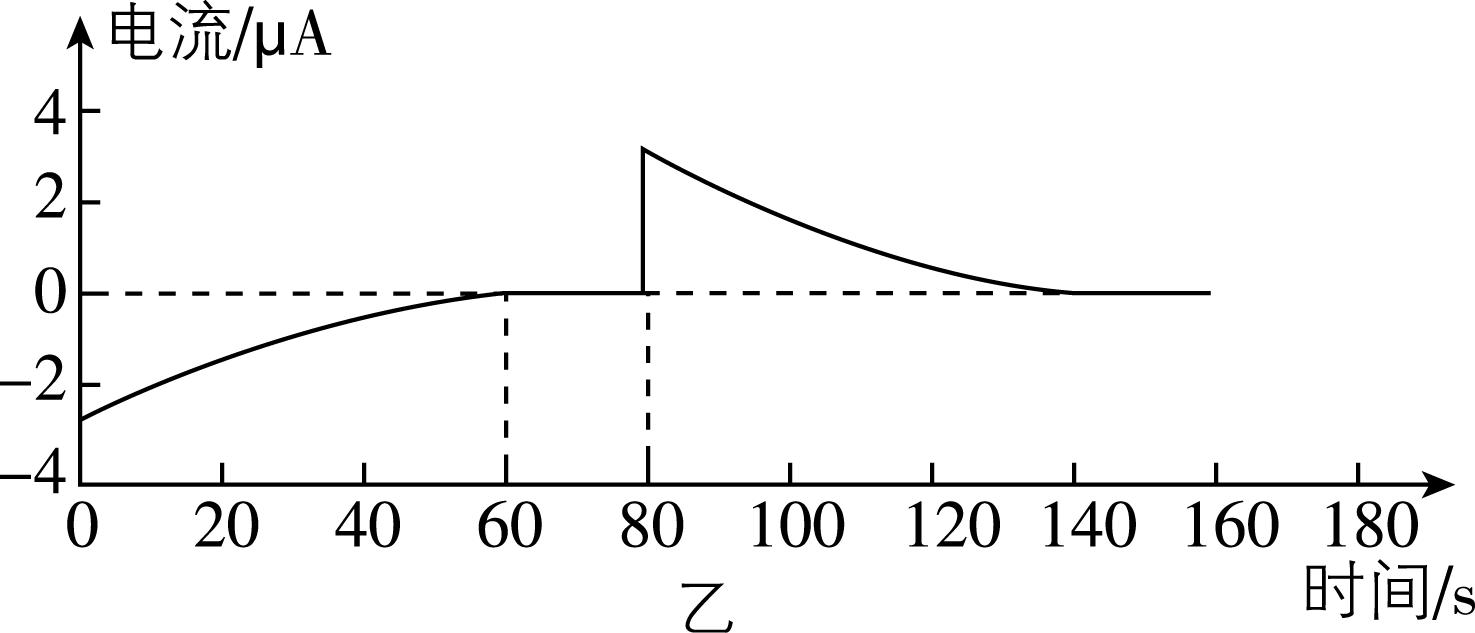
方案二 | 用图甲所示装置及试剂进行实验。 $ 80\mathrm{s} $ 时,向 $ {\rm \mathrm{U}} $ 形管左侧加入约1滴管 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 试剂 $ {\rm \mathrm{Y}} $ 。实验过程中电流的变化如图乙 |
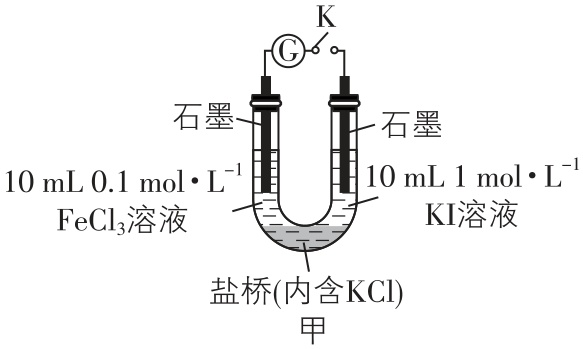
资料在线 盐桥中通常装有琼脂凝胶,内含氯化钾或硝酸铵。 盐桥中的离子能够定向移动,通过盐桥可将两个相互隔离的电解质溶液连接起来,传导电流。 |
回答下列问题:
(1) 方案一,振荡静置后溶液分层,下层为 色。试剂 $ {\rm \mathrm{X}} $ 为 (填化学式)溶液,该方案 (填“能”或“不能”)达到实验目的。
(2) 方案二,实验开始时, $ {\rm \mathrm{U}} $ 形管左侧发生 (填“氧化”或“还原”)反应,盐桥中 (填离子符号)移向左侧。
(3) 方案二能验证 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 与 $ {\rm {\mathrm{I}}^{-}} $ 发生的是可逆反应。结合图乙电流变化可知,试剂 $ {\rm \mathrm{Y}} $ 为 (填化学式)溶液;加入试剂 $ {\rm \mathrm{Y}} $ 后,正极的电极反应式为 。
(4) 方案二,电流为0时,下列说法正确的是 (填序号)。
A. $ {\rm c({\mathrm{F}\mathrm{e}}^{3+})} $ 保持不变 B. 反应停止
C. $ {\rm 2{v}_{正}({\mathrm{F}\mathrm{e}}^{3+})={v}_{逆}({\mathrm{I}}_{2})} $ D. $ {\rm {v}_{正}({\mathrm{I}}^{-})={v}_{逆}({\mathrm{F}\mathrm{e}}^{2+})} $
答案:(1) 紫红(或紫); $ {\rm \mathrm{K}\mathrm{S}\mathrm{C}\mathrm{N}} $ ;不能
(2) 还原; $ {\rm {\mathrm{K}}^{+}} $
(3) $ {\rm {\mathrm{F}\mathrm{e}\mathrm{C}\mathrm{l}}_{2}} $ ; $ {\rm {\mathrm{I}}_{2}+2{\mathrm{e}}^{-}\xlongequal{}2{\mathrm{I}}^{-}} $
(4) AD
解析:(1) 由得失电子守恒知, $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 与 $ {\rm {\mathrm{I}}^{-}} $ 反应的离子方程式为 $ {\rm 2{\mathrm{F}\mathrm{e}}^{3+}+2{\mathrm{I}}^{-}⇌2{\mathrm{F}\mathrm{e}}^{2+}+{\mathrm{I}}_{2}} $ , $ {\rm 5\mathrm{m}\mathrm{L}1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}\mathrm{K}\mathrm{I}} $ 溶液中 $ {\rm n({\mathrm{I}}^{-})=5×{10}^{-3}\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm 10\mathrm{m}\mathrm{L}1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}{\mathrm{F}\mathrm{e}\mathrm{C}\mathrm{l}}_{3}} $ 溶液中 $ {\rm n({\mathrm{F}\mathrm{e}}^{3+})={10}^{-2}\mathrm{m}\mathrm{o}\mathrm{l}} $ , $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 过量,充分反应后加入 $ {\rm 5\mathrm{m}\mathrm{L}{\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ ,振荡静置, $ {\rm {\rho }_{{\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} > {\rho }_{水}} $ ,则 $ {\rm {\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ 层在下层, $ {\rm {\mathrm{I}}_{2}} $ 在 $ {\rm {\mathrm{C}\mathrm{C}\mathrm{l}}_{4}} $ 中的溶解度大于在水中的溶解度,则下层为紫红色。反应后取上层清液于试管中,加入3滴 $ {\rm \mathrm{K}\mathrm{S}\mathrm{C}\mathrm{N}} $ 溶液,溶液变为红色,证明有 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 存在,但不能证明 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 与 $ {\rm {\mathrm{I}}^{-}} $ 发生可逆反应,因为 $ {\rm {\mathrm{F}\mathrm{e}}^{3+}} $ 本来就过量。
(2) 图甲左侧电极发生还原反应: $ {\rm 2{\mathrm{F}\mathrm{e}}^{3+}+2{\mathrm{e}}^{-}\xlongequal{}2{\mathrm{F}\mathrm{e}}^{2+}} $ ,为正极,右侧为负极,发生氧化反应: $ {\rm 2{\mathrm{I}}^{-}-2{\mathrm{e}}^{-}\xlongequal{}{\mathrm{I}}_{2}} $ ,盐桥通过离子迁移来平衡电荷,故盐桥中 $ {\rm {\mathrm{K}}^{+}} $ 移向左侧, $ {\rm {\mathrm{C}\mathrm{l}}^{-}} $ 移向右侧。
(3) 开始时原电池总反应为 $ {\rm 2{\mathrm{F}\mathrm{e}}^{3+}+2{\mathrm{I}}^{-}⇌2{\mathrm{F}\mathrm{e}}^{2+}+{\mathrm{I}}_{2}} $ ,由题图知,随着反应进行,电流计读数逐渐趋向零,最后读数变为零,反应达到平衡;当指针读数变为零后,向 $ {\rm \mathrm{U}} $ 形管左侧加入约1滴管 $ {\rm 1\mathrm{m}\mathrm{o}\mathrm{l}\cdot {\mathrm{L}}^{-1}} $ 试剂 $ {\rm \mathrm{Y}} $ ,电流方向逆转,则原电池反应变为 $ {\rm 2{\mathrm{F}\mathrm{e}}^{2+}+{\mathrm{I}}_{2}⇌2{\mathrm{F}\mathrm{e}}^{3+}+2{\mathrm{I}}^{-}} $ ,即试剂 $ {\rm \mathrm{Y}} $ 为 $ {\rm {\mathrm{F}\mathrm{e}\mathrm{C}\mathrm{l}}_{2}} $ 溶液,电流逆转后左侧电极(负极)发生氧化反应: $ {\rm 2{\mathrm{F}\mathrm{e}}^{2+}-2{\mathrm{e}}^{-}\xlongequal{}2{\mathrm{F}\mathrm{e}}^{3+}} $ ,右侧电极(正极)发生还原反应: $ {\rm {\mathrm{I}}_{2}+2{\mathrm{e}}^{-}\xlongequal{}2{\mathrm{I}}^{-}} $ 。
(4) 电流为0,说明反应达到平衡, $ {\rm c({\mathrm{F}\mathrm{e}}^{3+})} $ 保持不变,但反应并未停止,是动态平衡, $ {\rm \dfrac{{v}_{正}({\mathrm{F}\mathrm{e}}^{3+})}{{v}_{逆}({\mathrm{I}}_{2})}=\dfrac{2}{1}} $ ,则 $ {\rm {v}_{正}({\mathrm{F}\mathrm{e}}^{3+})=2{v}_{逆}({\mathrm{I}}_{2})} $ , $ {\rm \dfrac{{v}_{逆}({\mathrm{F}\mathrm{e}}^{2+})}{{v}_{正}({\mathrm{I}}^{-})}=\dfrac{2}{2}} $ ,则 $ {\rm {v}_{正}({\mathrm{I}}^{-})={v}_{逆}({\mathrm{F}\mathrm{e}}^{2+})} $ ,故选 $ {\rm \mathrm{A}\mathrm{D}} $ 。
8.向绝热恒容密闭容器中通入 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 和 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ ,在一定条件下发生反应: $ {\rm {\mathrm{S}\mathrm{O}}_{2}(\mathrm{g})+{\mathrm{N}\mathrm{O}}_{2}(\mathrm{g})⇌{\mathrm{S}\mathrm{O}}_{3}(\mathrm{g})+\mathrm{N}\mathrm{O}(\mathrm{g})} $ ,正反应速率随时间变化的示意图如图所示,下列结论中正确的有( )
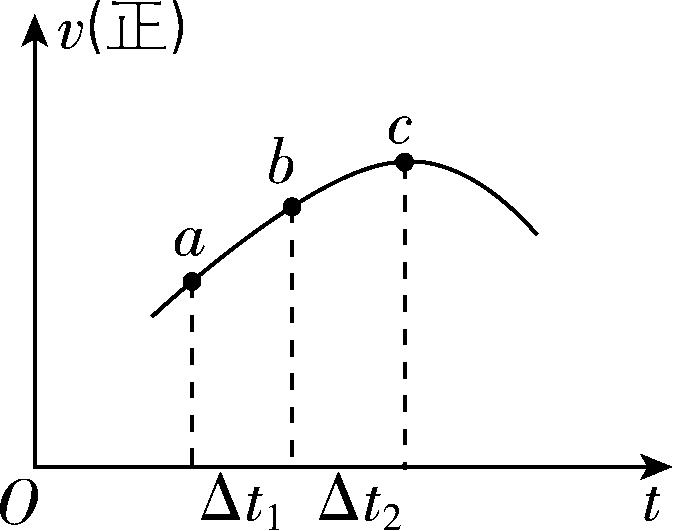
①反应在 $ c $ 点达到平衡
$ {\rm ②{\mathrm{S}\mathrm{O}}_{2}} $ 浓度: $ a $ 点小于 $ c $ 点
③反应物的总能量高于生成物的总能量
$ {\rm ④\mathrm{\Delta }{t}_{1}=\mathrm{\Delta }{t}_{2}} $ , $ ab $ 段 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的消耗量小于 $ bc $ 段 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的消耗量
⑤混合物颜色不再变化,说明反应达到平衡
⑥逆反应速率图像在此时间段内和题图趋势相同
⑦混合气体的平均相对分子质量 $ {\rm ({\overline{M}}_{\mathrm{r}})} $ 不再变化,说明反应达到平衡
A. 3个
B. 4个
C. 5个
D. 6个
答案:A
解析:当正反应速率不变时,达到化学平衡状态,由题图可知, $ c $ 点正反应速率开始减小,所以 $ c $ 点未达平衡,①错误; $ a $ 点时反应向正反应方向进行,随着反应的进行,反应物浓度逐渐减小,所以 $ {\rm {\mathrm{S}\mathrm{O}}_{2}} $ 浓度: $ a $ 点大于 $ c $ 点,②错误;随反应进行反应物浓度不断减小,但从 $ a $ 点到 $ c $ 点正反应速率不断增大,说明反应刚开始时温度升高,且温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,即该反应为放热反应,反应物的总能量高于生成物的总能量,③正确; $ {\rm v\mathrm{\Delta }t=\mathrm{\Delta }c} $ , $ {\rm \mathrm{\Delta }{t}_{1}=\mathrm{\Delta }{t}_{2}} $ 时,因为 $ ab $ 段平均反应速率小于 $ bc $ 段平均反应速率,则 $ ab $ 段反应物浓度变化 $ {\rm \mathrm{\Delta }c} $ 小于 $ bc $ 段,即 $ ab $ 段 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的消耗量小于 $ bc $ 段 $ {\rm {\mathrm{N}\mathrm{O}}_{2}} $ 的消耗量,④正确;混合物颜色不再变化,说明二氧化氮浓度不再变化,可以说明反应达到平衡,⑤正确;该时间段内,在达到平衡之前,生成物浓度一直在变大,逆反应速率应该一直变大,⑥错误;该反应前后气体分子数相等,混合气体的总物质的量不变,恒容容器内混合气体的总质量不变,则混合气体的平均相对分子质量不变,不能说明反应达到平衡,⑦错误。③④⑤正确,选 $ {\rm \mathrm{A}} $ 。





